Clear Sky Science · es
Guía para nefrostomía percutánea mediante un endoscopio de tomografía de coherencia óptica basado en redes neuronales convolucionales
Por qué importa un acceso renal más seguro
La enfermedad de los cálculos renales es cada vez más frecuente y muchos pacientes necesitan que se coloque un pequeño tubo directamente en el riñón para drenar la orina o extraer los cálculos. Este procedimiento, llamado nefrostomía percutánea, se realiza guiando una aguja desde la espalda del paciente hasta el centro hueco del riñón. Aunque la punción es diminuta, elegir la trayectoria equivocada puede desgarrar estructuras renales delicadas o dañar vasos sanguíneos, provocando hemorragias y otras complicaciones. Este estudio presenta una nueva sonda de imagen de alta resolución, integrada con inteligencia artificial, que se desliza dentro de la punta de la aguja para ayudar a los médicos a ver exactamente hacia dónde se dirigen y evitar daños.
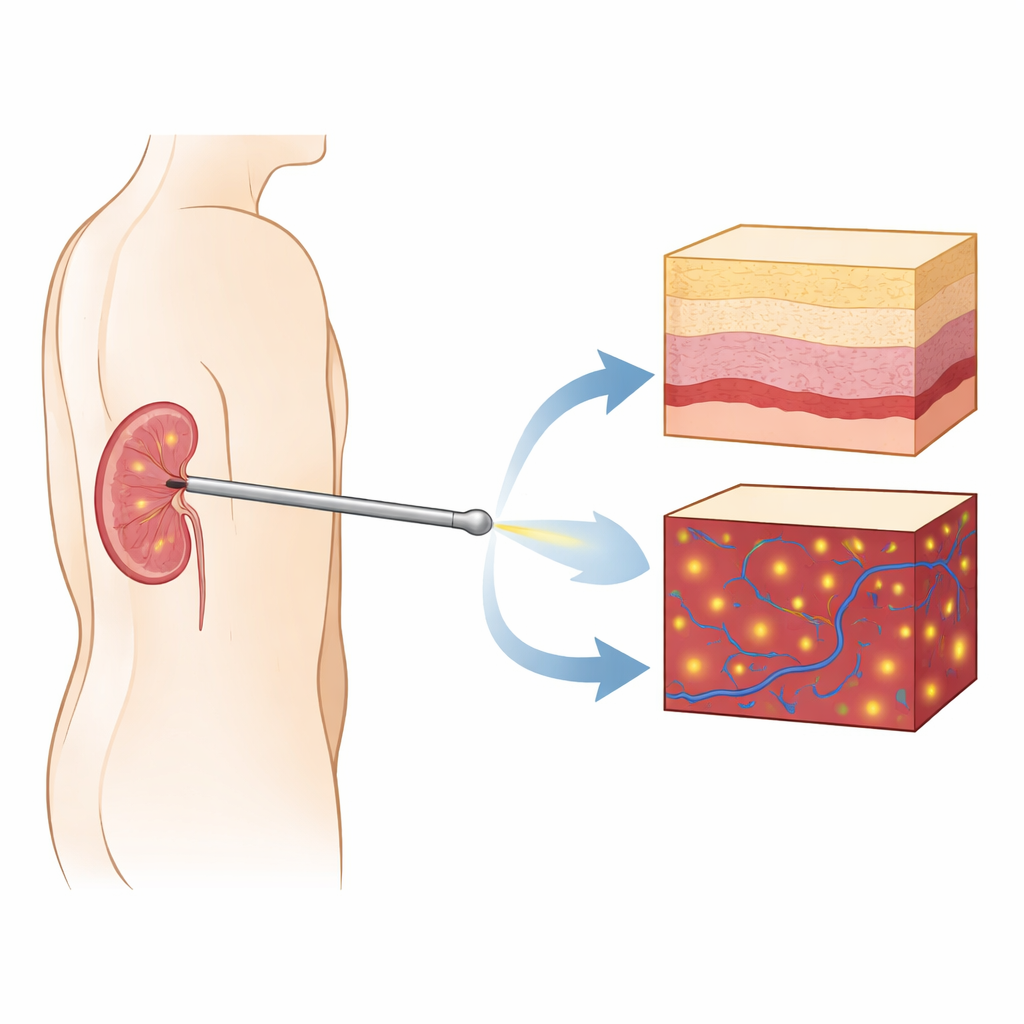
Una cámara diminuta para el interior de la aguja
Los investigadores construyeron una sonda de imagen orientada hacia adelante basada en tomografía de coherencia óptica (OCT), un método óptico que puede captar “rebanadas” seccionales del tejido con resolución micrométrica—aproximadamente diez veces más fina que la ecografía médica convencional. Integraron una lente de índice de gradiente delgada dentro de una aguja de nefrostomía estándar para que, durante la inserción, la sonda pueda mirar directamente hacia delante dentro del riñón. A diferencia de los endoscopios habituales que muestran principalmente vistas de la superficie, este sistema proporciona imágenes con resolución en profundidad, revelando cómo cambia la estructura tisular bajo la punta. La misma sonda también puede operar en modo Doppler, que resalta los glóbulos rojos en movimiento y así pone de manifiesto los vasos sanguíneos frente a la aguja antes de que sean perforados.
Reconocer las capas renales en tiempo real
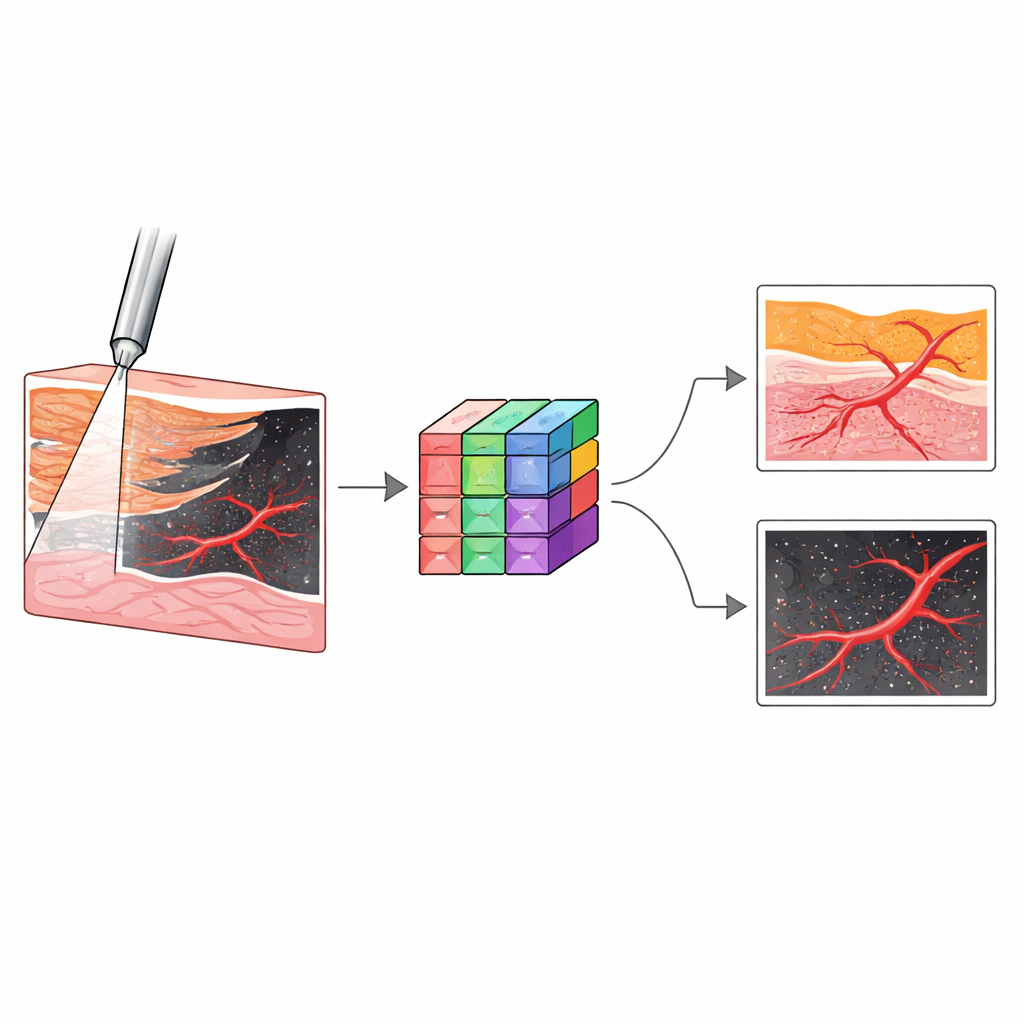
Para comprobar si el sistema podía distinguir distintos tejidos renales, el equipo realizó experimentos en 31 riñones humanos donados mantenidos en condiciones casi normales. En los procedimientos reales, la aguja debe atravesar la corteza externa y la médula interna, entrar en una región en forma de copa llamada cáliz y, finalmente, emerger en la pelvis —la cavidad central colectora de orina. Salirse del trayecto puede implicar pasar por espacios grasos entre estructuras y desgarrar paredes delgadas. Los investigadores tocaron sistemáticamente la sonda contra cinco tipos de tejido—corteza, médula, cáliz, grasa del seno renal y pelvis—y capturaron millones de imágenes OCT que mostraban sus patrones distintivos. Por ejemplo, corteza y médula se veían lisas pero diferían en profundidad, el cáliz mostraba transiciones tipo franjas, la grasa del seno producía redes brillantes moteadas y la pelvis aparecía como un espacio vacío debajo de la sonda.
Enseñar a un sistema inteligente a detectar el peligro
Dado que a los expertos humanos les llevaría tiempo y entrenamiento interpretar estas nuevas imágenes durante una operación, el equipo recurrió al aprendizaje profundo. Entrenaron varias redes neuronales convolucionales para clasificar cada fotograma OCT en uno de los cinco tipos de tejido y luego seleccionaron una arquitectura llamada Inception como la de mejor rendimiento. En pruebas internas, este modelo identificó correctamente los tejidos con una precisión de aproximadamente 99,6% y mantuvo un rendimiento alto en riñones adicionales que nunca había visto. En una tarea separada, usaron otro diseño de red neuronal, nnU‑Net, para delinear vasos sanguíneos en imágenes Doppler OCT. Este modelo aprendió a distinguir la sangre en flujo del tejido de fondo con una superposición muy alta respecto a etiquetas dibujadas a mano por expertos, incluso para vasos menores de 0,2 milímetros de diámetro que son difíciles de ver con herramientas estándar.
Cómo se compara con las herramientas actuales
Actualmente, los médicos suelen basarse en ecografía o en fluoroscopia por rayos X para guiar las agujas de nefrostomía. Estas técnicas muestran la posición general del riñón y la trayectoria aproximada de la aguja, pero su resolución relativamente tosca dificulta saber exactamente qué tejido está en la punta o cuán cerca se encuentra un vaso sanguíneo. En experimentos de control, radiólogos experimentados que usaron ecografía estructural y Doppler tuvieron dificultades para identificar el tejido preciso en la punta de la aguja y no pudieron visualizar de forma fiable vasos diminutos. En contraste, el sistema OCT ofreció una vista local detallada más un análisis automatizado que se ejecuta en una fracción de segundo en GPUs modernas, lo bastante rápido como para proporcionar retroalimentación mientras la aguja avanza.
Qué podría significar esto para los pacientes
El estudio sugiere que combinar una sonda OCT montada en la aguja con aprendizaje profundo podría hacer que los procedimientos de acceso renal sean más seguros y eficientes. En el futuro, un médico podría insertar la aguja habitual con la sonda en su interior, ver imágenes a escala fina en tiempo real y confiar en el software para señalar cuándo la punta ha entrado en la cavidad correcta o se aproxima a un vaso sanguíneo. Menos intentos de punción significarían menos traumatismo tisular, menor riesgo de hemorragia y potencialmente procedimientos y estancias hospitalarias más cortas. Aunque el trabajo se realizó sobre riñones donados y no en pacientes vivos, sienta las bases para sistemas clínicos que también podrían ayudar a guiar otras intervenciones con aguja, desde biopsias y bloqueos anestésicos hasta la administración dirigida de fármacos.
Cita: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
Palabras clave: cirugía de cálculos renales, guía de aguja, tomografía de coherencia óptica, IA en imágenes médicas, detección de vasos sanguíneos