Clear Sky Science · es
Perspectivas a célula única sobre la heterogeneidad trofoblástica y la disfunción adaptativa en el retraso selectivo del crecimiento fetal
Cuando un gemelo se queda atrás
Para los padres que esperan gemelos, puede ser profundamente angustioso cuando un bebé deja de crecer tan bien como el otro, pese a compartir el mismo útero y placenta. Esta condición, denominada retraso selectivo del crecimiento fetal, no solo pone en riesgo la salud del gemelo más pequeño antes del nacimiento, sino que también puede influir en su desarrollo a largo plazo. Este estudio emplea análisis unicelular de vanguardia para mirar dentro de la placenta compartida en embarazos gemelares de este tipo, revelando cómo pequeños cambios en células placentarias específicas y en las respuestas inmunitarias pueden inclinar la balanza entre un crecimiento saludable y una peligrosa escasez.
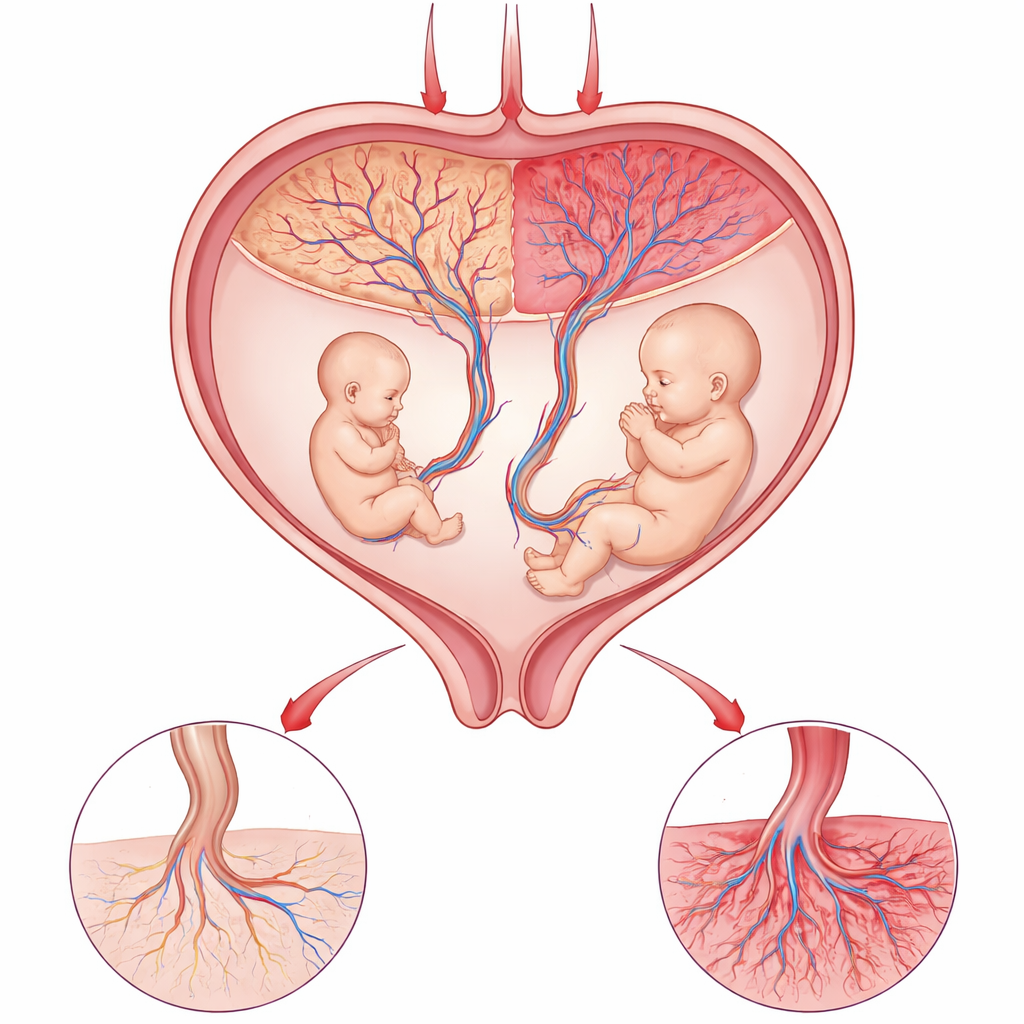
El delicado acto de equilibrio de la placenta
La placenta es el cordón vital entre la madre y el bebé, proporcionando oxígeno y nutrientes mientras elimina desechos. En ciertos embarazos de gemelos idénticos, ambos bebés comparten una sola placenta pero ocupan territorios diferentes dentro de ella. Cuando un gemelo queda mucho más pequeño que el otro, los médicos saben que algo ha fallado de forma localizada en ese órgano compartido. Dado que los gemelos tienen la misma madre y genes casi idénticos, constituyen un experimento natural potente: cualquier diferencia importante en el crecimiento probablemente provenga de cómo funcionan las respectivas zonas de la placenta, más que de diferencias entre los propios bebés.
Acercándose a las células placentarias individuales
Los investigadores recolectaron muestras placentarias de tres embarazos en los que un gemelo era significativamente más pequeño que el otro. Usando secuenciación de ARN unicelular —un método que lee la actividad de miles de genes en células individuales— caracterizaron más de 175.000 células de las distintas regiones placentarias. Esto les permitió clasificar las células en tipos distintos, incluidos células de sostén, células vasculares y varios tipos de células inmunitarias. Se centraron en un grupo clave denominado citotrofoblastos villosos, una capa de células que recubre las pequeñas proyecciones en forma de dedo donde la sangre materna se encuentra con la circulación fetal y que se renueva continuamente para reparar y mantener la superficie de la placenta.
Dos estados celulares clave: estructura frente a modo supervivencia
Dentro de estos citotrofoblastos villosos, el equipo identificó dos estados principales con funciones muy distintas. Un grupo, marcado por una molécula llamada TP63, actuaba como cuidadores estructurales: apoyaban la barrera entre madre y bebé, mantenían las conexiones entre células y ayudaban a conservar la organización del tejido. El otro grupo, marcado por una enzima llamada LDHA, estaba orientado a una intensa producción de energía y a la gestión del estrés, activando vías relacionadas con las mitocondrias, el estrés oxidativo y el control de la calidad proteica. En los territorios placentarios de los gemelos más pequeños, las células protectoras TP63 estaban agotadas, mientras que las células orientadas al estrés LDHA se expandían y proliferaban con mayor actividad. Un análisis computacional de “trayectorias” sugirió que las células eran empujadas a lo largo de un camino desde roles estructurales saludables hacia un modo de supervivencia, con menos células alcanzando el estado fusionado que normalmente mantiene una superficie de intercambio lisa y eficiente.
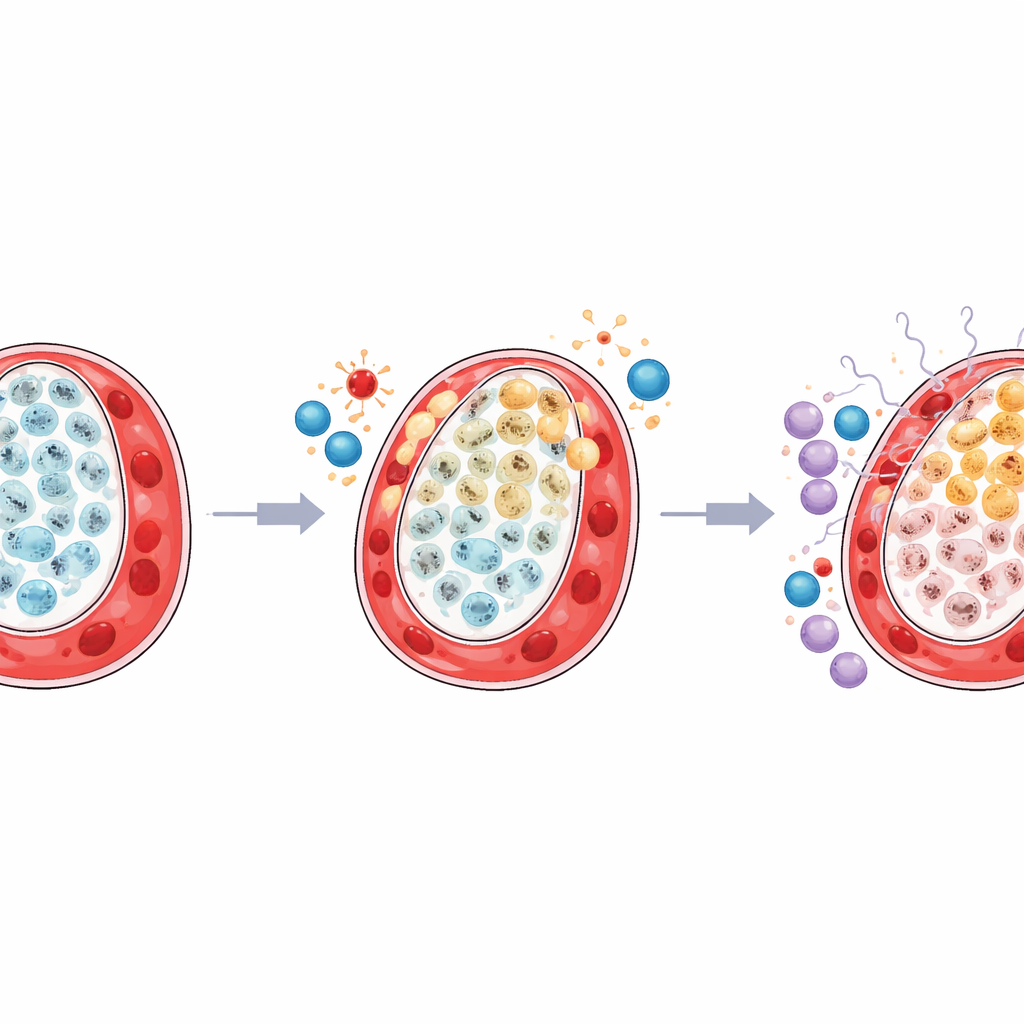
Barrio inflamado alrededor de las células estresadas
El estudio también observó que el entorno inmunitario circundante en el territorio placentario del gemelo más pequeño se transformó de forma perjudicial. Un tipo útil de macrófago residente, conocido como células de Hofbauer, que normalmente apoya la salud del tejido y regula el metabolismo, estaba reducido. Al mismo tiempo, ciertas células asesinas naturales, preparadas para respuestas antivirales e inflamatorias, se volvieron más abundantes y más activas. El mapeo detallado de las señales intercambiadas entre células mostró que los trofoblastos estresados de tipo LDHA interactuaban con más intensidad con las células inmunitarias a través de vías impulsadas por interferones y moléculas de alarma relacionadas. Mientras tanto, la comunicación entre las células estructurales TP63 y las células estromales y vasculares de apoyo se debilitó, lo que sugiere la pérdida tanto del soporte físico como de la regulación inmunitaria calmada.
Un colapso en tres vías que limita el crecimiento fetal
En conjunto, el trabajo traza una imagen clara y accesible de lo que falla en la placenta cuando un gemelo se queda atrás. Las células de soporte estructural que mantienen la superficie de intercambio firme y ordenada se agotan, las células estresadas con alta demanda energética se imponen y el sistema inmunitario cambia hacia un estado más inflamatorio. Estos tres hilos —pérdida de estructura, sobrecarga metabólica e inflamación crónica— se refuerzan mutuamente y socavan gradualmente la capacidad de la placenta para aportar suficiente oxígeno y nutrientes al bebé más pequeño. Al identificar los tipos celulares y las vías de señalización específicas implicadas, este estudio ofrece una hoja de ruta para futuras pruebas y tratamientos destinados a detectar problemas placentarios antes y, quizá, reorientar estas células hacia un equilibrio más saludable.
Cita: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Palabras clave: placenta, embarazo gemelar, retraso del crecimiento fetal, secuenciación de ARN unicelular, células trofoblásticas