Clear Sky Science · es
Análisis proteómico de vesículas extracelulares derivadas de tejido muestra cambios moleculares específicos por región en un modelo de rata del síndrome de takotsubo
Cuando el estrés deja una marca temporal en el corazón
La mayoría de la gente piensa en un infarto como un daño permanente, pero existe una afección desconcertante en la que el corazón se debilita de forma súbita y luego se recupera en días o semanas. Esto se conoce como síndrome de takotsubo, con frecuencia desencadenado por un estrés emocional o físico intenso. El estudio resumido aquí examina las pequeñas “burbujas mensajeras” biológicas liberadas por las células cardíacas en un modelo de rata de este síndrome, revelando cómo diferentes partes del corazón responden de manera distinta a una oleada repentina de hormonas del estrés.
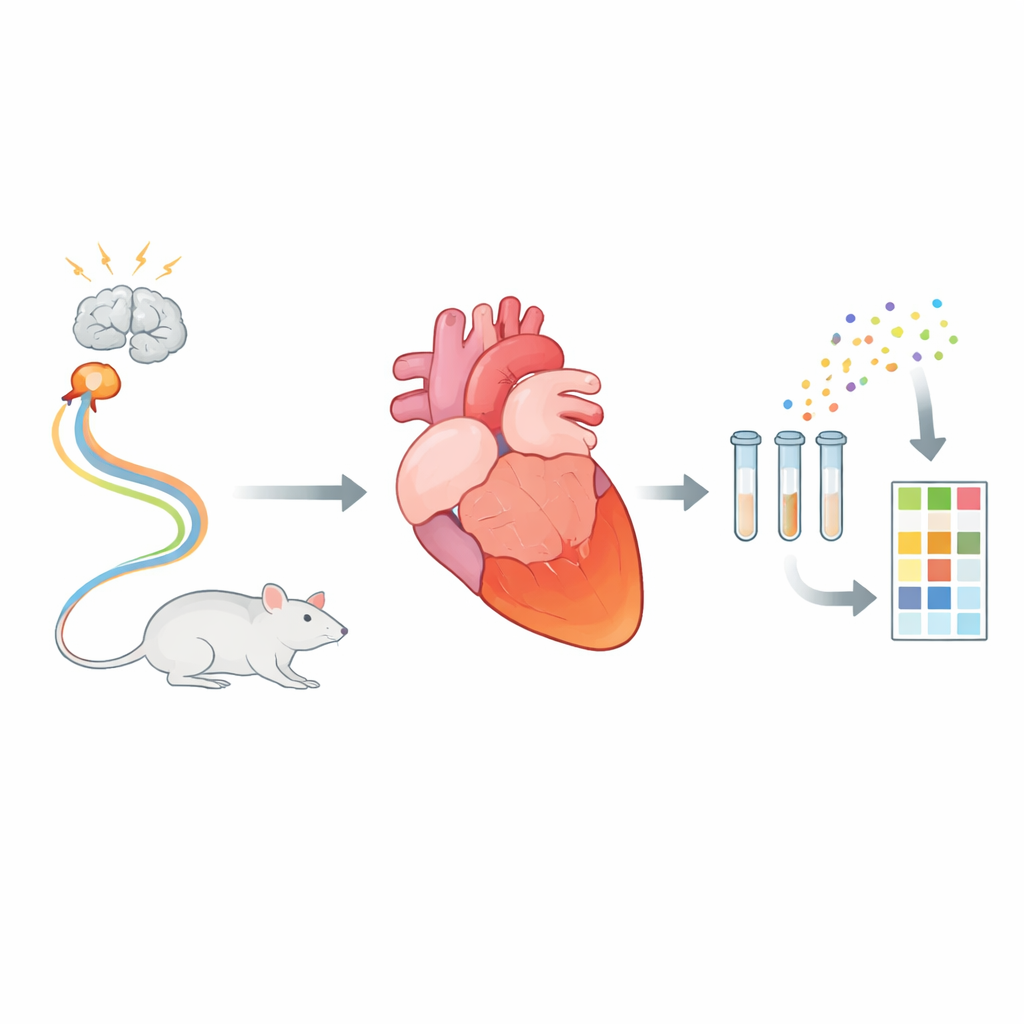
Una insuficiencia cardíaca temporal con preguntas persistentes
El síndrome de takotsubo imita un infarto clásico: los pacientes llegan con dolor torácico, electrocardiogramas alarmantes y función de bombeo reducida. Sin embargo, sus arterias coronarias no están bloqueadas y las regiones cardíacas afectadas suelen recuperarse. Un patrón característico es que la punta (ápice) del ventrículo izquierdo queda casi inmóvil, mientras que la base sigue contrayéndose. A pesar de su creciente reconocimiento, la “conversación” biológica entre las células cardíacas estresadas—cómo señalan angustia, daño y reparación—sigue siendo poco conocida. Los investigadores usaron un modelo de rata bien establecido que reproduce de cerca las características humanas del takotsubo tras una dosis controlada de un fármaco que imita el estrés, capturando el corazón 24 horas después, en la fase temprana de recuperación.
Pequeñas burbujas que transportan mensajes del corazón
Cada célula del cuerpo libera paquetes a nanoescala llamados vesículas extracelulares. Estas burbujas envueltas en membrana llevan proteínas, lípidos y material genético que pueden alterar el comportamiento de células vecinas o distantes. En la enfermedad cardíaca, tales vesículas pueden agravar el daño fomentando la inflamación o favorecer la curación apoyando el crecimiento de vasos sanguíneos y la reparación del tejido. En este trabajo, los científicos aislaron cuidadosamente vesículas directamente del ápice y la base de corazones de rata, en lugar de hacerlo a partir de sangre. Mediante microscopía electrónica, seguimiento de partículas y marcadores proteicos, confirmaron que tenían preparaciones limpias de vesículas típicas, con tamaños que oscilaban entre unos 50 y 400 nanómetros. De forma importante, solo la región apical estresada en corazones con takotsubo produjo menos vesículas, mientras que la base no afectada y los corazones normales liberaron cantidades similares, lo que sugiere una respuesta específica por región al estrés.
Dos mitades del corazón, dos historias moleculares
El equipo aplicó después proteómica de alta resolución, una técnica que cataloga y cuantifica miles de proteínas a la vez. En todas las muestras identificaron algo más de 2.000 proteínas dentro de las vesículas. En corazones sanos, las vesículas del ápice y de la base eran notablemente similares, lo que sugiere un perfil de comunicación “base” uniforme. Tras el estrés, sin embargo, las vesículas del segmento apical cambiaron drásticamente, mientras que las de la base apenas variaron. Cientos de proteínas se alteraron en las vesículas apicales en comparación con el ápice sano y con la base estresada. Muchas de las proteínas aumentadas con más fuerza se asociaron al sistema inmune y a la inflamación, mientras que muchas de las proteínas disminuidas respaldaban la función mitocondrial—las fábricas de energía de la célula. Los análisis de redes y vías avanzados apuntaron de forma consistente a un patrón organizado: metabolismo energético reducido junto con una mayor actividad inmunitaria y de remodelado tisular en el segmento dañado.
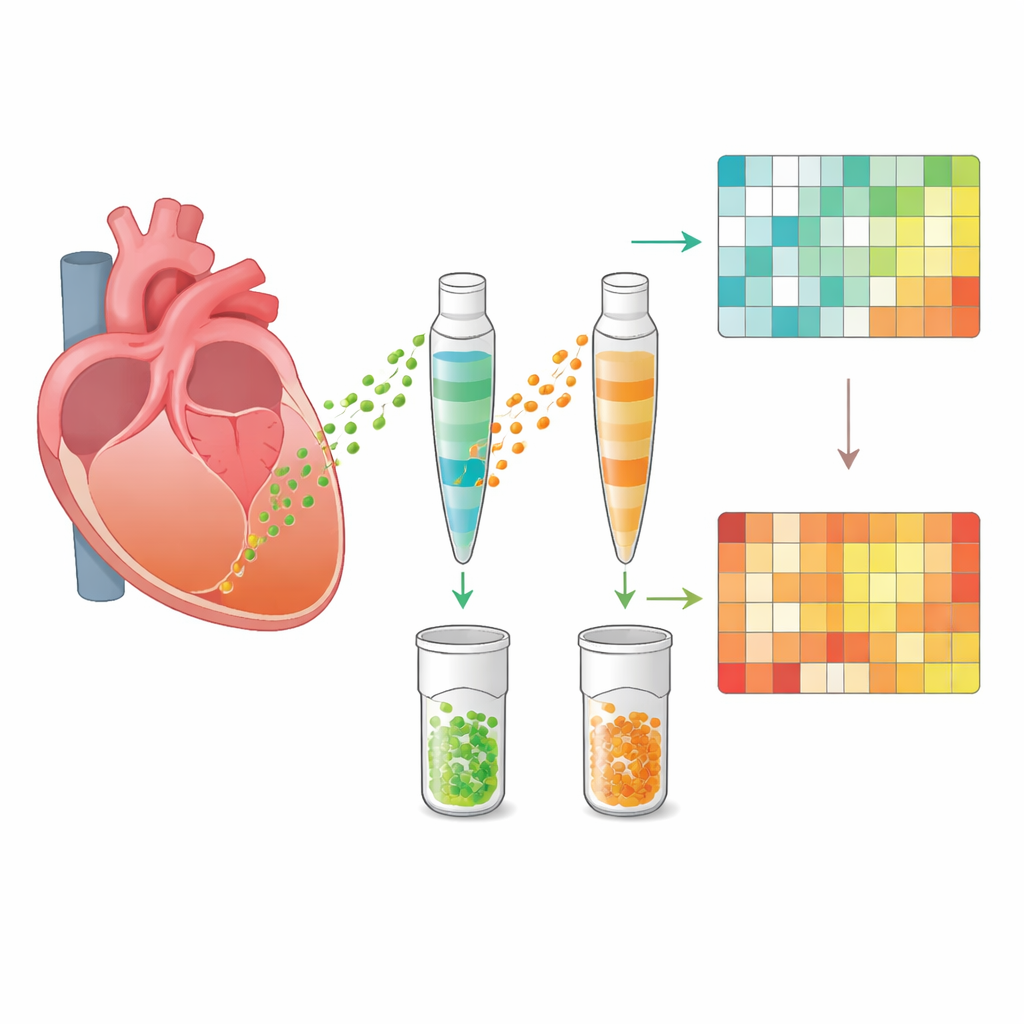
Inflamación, lípidos y señales de reparación
Al observar más de cerca las redes proteicas interconectadas, los investigadores vieron que las proteínas implicadas en el manejo de lípidos (grasas) estaban fuertemente ligadas a las que impulsan la inflamación. Esto concuerda con observaciones previas de que aparecen gotas lipídicas e hinchazón en el corazón poco después del estrés, seguidas por infiltración de células inmunitarias y más tarde cambios parecidos a cicatrices. Las vesículas del ápice afectado estaban enriquecidas en proteínas asociadas con la coagulación sanguínea, el crecimiento de vasos y la formación de colágeno—características tanto de la reparación como de la cicatrización. Al mismo tiempo, contenían proteínas pertenecientes a vías clave de señalización de supervivencia, especialmente las rutas MAPK, que ayudan a las células a resistir la lesión y pueden favorecer la capacidad del corazón para recuperar su fuerza de bombeo. En conjunto, la carga de las vesículas dibujó el panorama de una región cardíaca que atraviesa un déficit energético, inflamación activa, remodelado estructural e intentos de autoprotección.
Qué significa esto para los pacientes y la atención futura
Este estudio es el primero en mapear con detalle la carga proteica de vesículas liberadas desde diferentes regiones del corazón en el síndrome de takotsubo. Para un público general, el mensaje central es que la punta aturdida del corazón no está esperando en silencio a recuperarse; está llena de actividad molecular, enviando pequeños paquetes que señalan estrés energético, inflamación, reparación tisular y supervivencia. Estas vesículas podrían algún día servir como marcadores sensibles en sangre para diagnosticar takotsubo, distinguirlo de un infarto o identificar a pacientes con riesgo de recuperación más lenta. También podrían señalar nuevas dianas terapéuticas—vías que podrían modularse para reducir la inflamación dañina o apoyar una reparación saludable. Aunque el trabajo se realizó en ratas macho en un único punto temporal y sigue siendo exploratorio, abre una nueva ventana sobre cómo el corazón estresado se comunica consigo mismo durante esta forma misteriosa y, por lo general, reversible de insuficiencia cardíaca.
Cita: Zulfaj, E., Nejat, A., Kalani, M. et al. Proteomic analysis of tissue-derived extracellular vesicles shows region-specific molecular changes in a rat model of takotsubo syndrome. Sci Rep 16, 8731 (2026). https://doi.org/10.1038/s41598-026-42812-5
Palabras clave: síndrome de takotsubo, vesículas extracelulares, estrés cardíaco, proteómica, inflamación cardíaca