Clear Sky Science · es
La influencia de sistemas multisolvente en el proceso de electrohilado
Por qué importan las fibras diminutas y los líquidos sencillos
Desde mascarillas transpirables hasta vendajes inteligentes y envases alimentarios, muchos materiales modernos dependen de mantos de fibras plásticas extremadamente finas. Una de las formas más versátiles de fabricar estas nanofibras es una técnica llamada electrohilado, que extrae filamentos de un líquido mediante alto voltaje. Este artículo plantea una pregunta aparentemente sencilla con grandes consecuencias prácticas: ¿cómo controla la elección y la mezcla de disolventes de laboratorio habituales —los líquidos usados para disolver el plástico— si se forman fibras ordenadas y útiles o si el líquido se transforma de repente en un gel inútil?
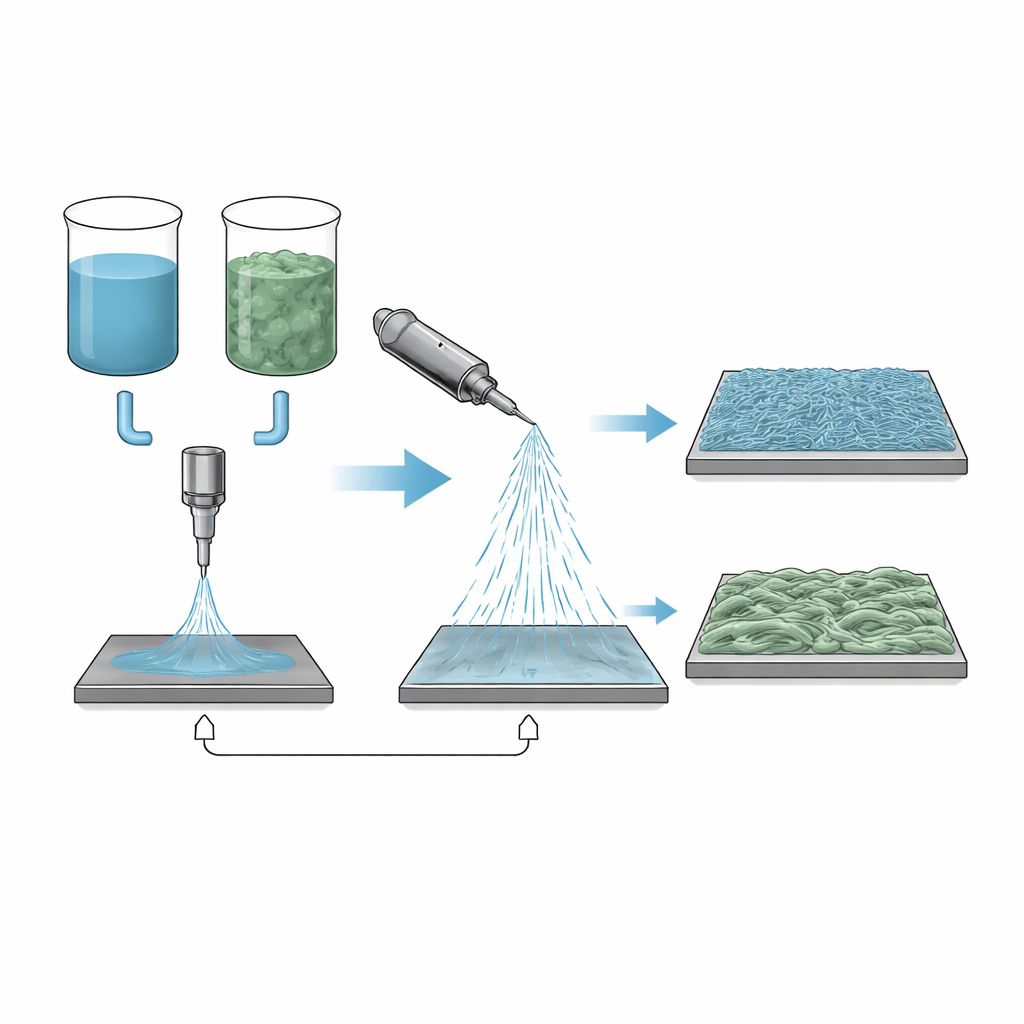
Hilando redes a partir de un líquido cargado
El electrohilado comienza con un polímero disuelto en un disolvente y alimentado a través de una boquilla pequeña. Al aplicarse alto voltaje, un chorro delgado se dirige hacia una placa colectora y se solidifica en una red de fibras más finas que un cabello humano. La ventaja del método es que el diámetro, la suavidad y la porosidad de la fibra pueden ajustarse para distintos usos, desde apósitos que liberan fármacos hasta filtros de aire y agua. Pero el proceso es extremadamente sensible a las propiedades del líquido: su viscosidad, tensión superficial y capacidad de conducir electricidad dependen de qué disolvente, o combinación de disolventes, se utilice. En este estudio los autores se centran en un plástico biodegradable, el succinato de polibutileno (PBS), y exploran qué ocurre cuando se disuelve en cloroformo junto con un segundo líquido de punto de ebullición más alto.
Cuando un líquido claro se convierte de pronto en gel
El equipo mezcló sistemáticamente cloroformo con tres disolventes orgánicos comunes —dimetilformamida (DMF), dimetilsulfóxido (DMSO) y d-limoneno— y disolvió en esas mezclas dos grados comerciales de PBS. Observaron que muchas de estas mezclas de dos disolventes, en lugar de mantenerse claras, se volvieron lentamente turbias y finalmente en una masa gelatinosa o similar a una grasa, sobre todo cuando estaba presente DMF o DMSO. Calentando y enfriando cuidadosamente las soluciones y registrando cuándo cambiaban entre líquido y gel, los investigadores mapearon las temperaturas de transición y estimaron la barrera de energía para este cambio. Su análisis de las formas moleculares de los disolventes y de las distribuciones de carga sugiere que los muy polares DMF y DMSO se asocian fuertemente tanto entre sí como con sitios específicos en las cadenas de PBS. Estos contactos bloquean efectivamente partes de la cadena, reducen la movilidad y empujan a la mezcla hacia la precipitación local y la gelificación.
Pequeñas diferencias en el plástico, grandes diferencias en el comportamiento
Curiosamente, los dos productos de PBS, aunque casi idénticos en peso molecular, respondieron de forma bastante distinta. Un grado (BioPBS FD 92) gelificó solo cuando el contenido del cosolvente polar era relativamente alto, mientras que el otro (PBE 003) comenzó a volverse turbio con adiciones mucho menores. Los autores relacionan este contraste con diferencias sutiles en densidad, arquitectura de las cadenas y aditivos de procesamiento añadidos en fábrica, que cambian la facilidad con la que las moléculas de disolvente pueden colarse entre los segmentos poliméricos. Las mediciones de viscosidad mostraron que las soluciones de BioPBS eran más espesas, lo que ayudó a estabilizar el chorro cargado durante el electrohilado y produjo fibras más uniformes. En contraste, las soluciones de PBE 003, de menor viscosidad, fueron más proclives a inestabilidades, generando fibras con una distribución de diámetros más amplia y más defectos en forma de huso, especialmente a medida que la gelificación progresaba con el tiempo.
De filamentos lisos a fibras porosas e inestables
Usando microscopios electrónicos, los investigadores compararon las fibras producidas con cada combinación de disolventes. Con DMF como segundo disolvente obtuvieron fibras lisas y continuas. Cuando en su lugar se empleó DMSO, las fibras desarrollaron una superficie porosa. Los autores atribuyen esto a una separación de fases inducida por vapor: el muy higroscópico DMSO absorbe humedad del aire circundante, provocando que el PBS disuelto precipite en la superficie de la fibra antes de que los disolventes se evaporen por completo, dejando pequeños vacíos. Para las mezclas que gelificaron rápidamente, la ventana de procesamiento útil se redujo a aproximadamente media hora. Más allá de eso, el chorro se rompía, los diámetros de las fibras se volvían erráticos y aparecían husos gruesos, lo que muestra cómo la gelificación dependiente del tiempo socava directamente la calidad del producto y la escalabilidad.
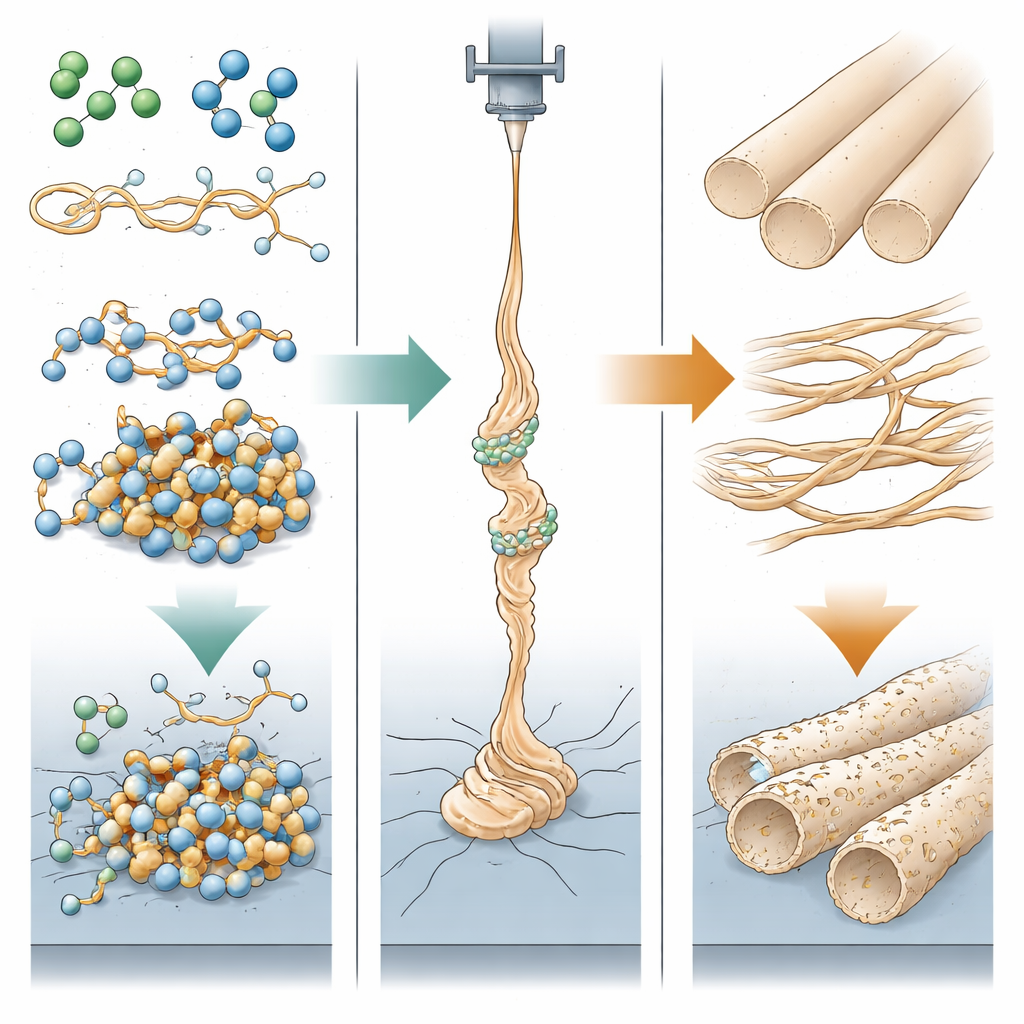
Qué significa esto para materiales de fibra más sostenibles
En términos cotidianos, este trabajo demuestra que disolver un plástico en “cualquier” mezcla compatible de líquidos no basta si se quieren nanofibras fiables y finamente ajustadas. La pareja exacta de disolventes y la proporción de mezcla pueden conducir silenciosamente el líquido desde un estado agradable y hilable hacia una gelatina rígida que obstruye el proceso, o hacia una solución que forma fibras lisas o porosas. Para el PBS biodegradable, socios polares como DMF y DMSO ofrecen un control útil sobre el tamaño y la textura de la fibra, pero también pueden desencadenar la gelificación a menos que su contenido y la temperatura se gestionen cuidadosamente. Al identificar estas interacciones ocultas y su impacto en el tiempo de procesamiento, este estudio aporta una hoja de ruta práctica para diseñar productos de nanofibras más seguros y ecológicos para medicina, envasado y filtración, sin sorpresas desagradables en la línea de hilado.
Cita: Borowczak, M., Sobczyk, K. & Leluk, K. The influence of multi-solvent systems on the electrospinning process. Sci Rep 16, 8666 (2026). https://doi.org/10.1038/s41598-026-42574-0
Palabras clave: electrospinning, nanofibers, biodegradable polymers, solvent mixtures, gelation