Clear Sky Science · es
Cuantificación de micronúcleos en imágenes hematológicas de portaobjetos completos mediante IA como biomarcador farmacodinámico traducible para inhibidores de la respuesta al daño del ADN
Por qué puntos diminutos en la sangre pueden contar grandes historias
Los médicos y los científicos buscan siempre formas sencillas de comprobar si un fármaco contra el cáncer hace lo que debe en el organismo. Este estudio muestra que pequeñas motas dentro de los glóbulos rojos, llamadas micronúcleos, pueden actuar como marcadores naturales del daño en el ADN provocado por ciertos tratamientos contra el cáncer. Al combinar el escaneo de portaobjetos completos al estilo microscópico con inteligencia artificial (IA), los investigadores convirtieron unas gotas de sangre en una lectura automatizada y rica sobre la intensidad con la que operan los fármacos dirigidos al ADN.
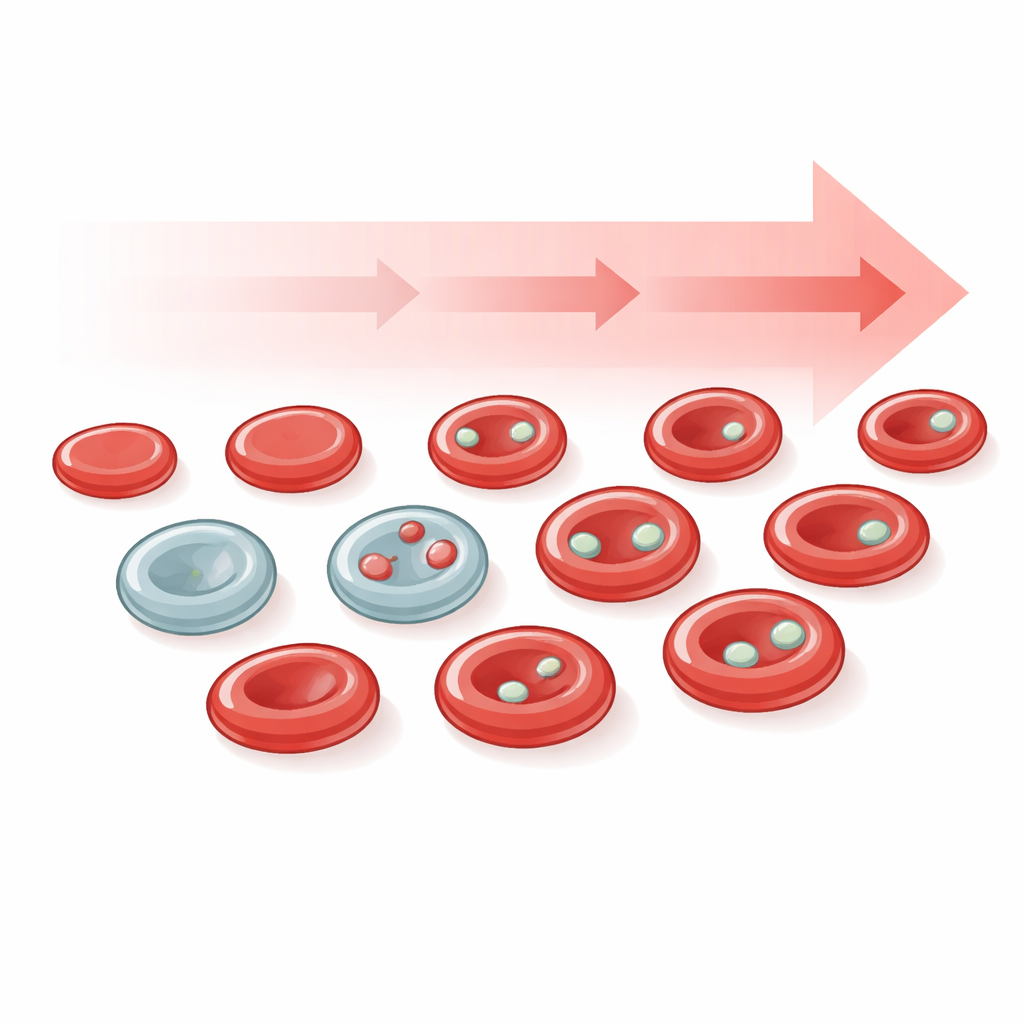
Pequeñas islas de ADN en los glóbulos rojos
Los micronúcleos son pequeñas burbujas de ADN que quedan separadas del núcleo principal de la célula. Se forman cuando los cromosomas se rompen o se distribuyen incorrectamente durante la división celular, sucesos comunes en el cáncer y tras la exposición a agentes que dañan el ADN. En la mayoría de los tejidos, detectar micronúcleos reales al microscopio es difícil porque los cortes finos pueden engañar a la vista. Los glóbulos rojos ofrecen una solución: al madurar, normalmente expulsan su núcleo principal, pero cualquier micronúcleo formado antes puede quedar atrás como diminutos puntos bien definidos. Estas estructuras conocidas desde hace tiempo, históricamente llamadas cuerpos de Howell–Jolly, son por tanto micronúcleos auténticos y convenientes que circulan en el torrente sanguíneo y pueden revelar cuánto daño en el ADN ha ocurrido recientemente.
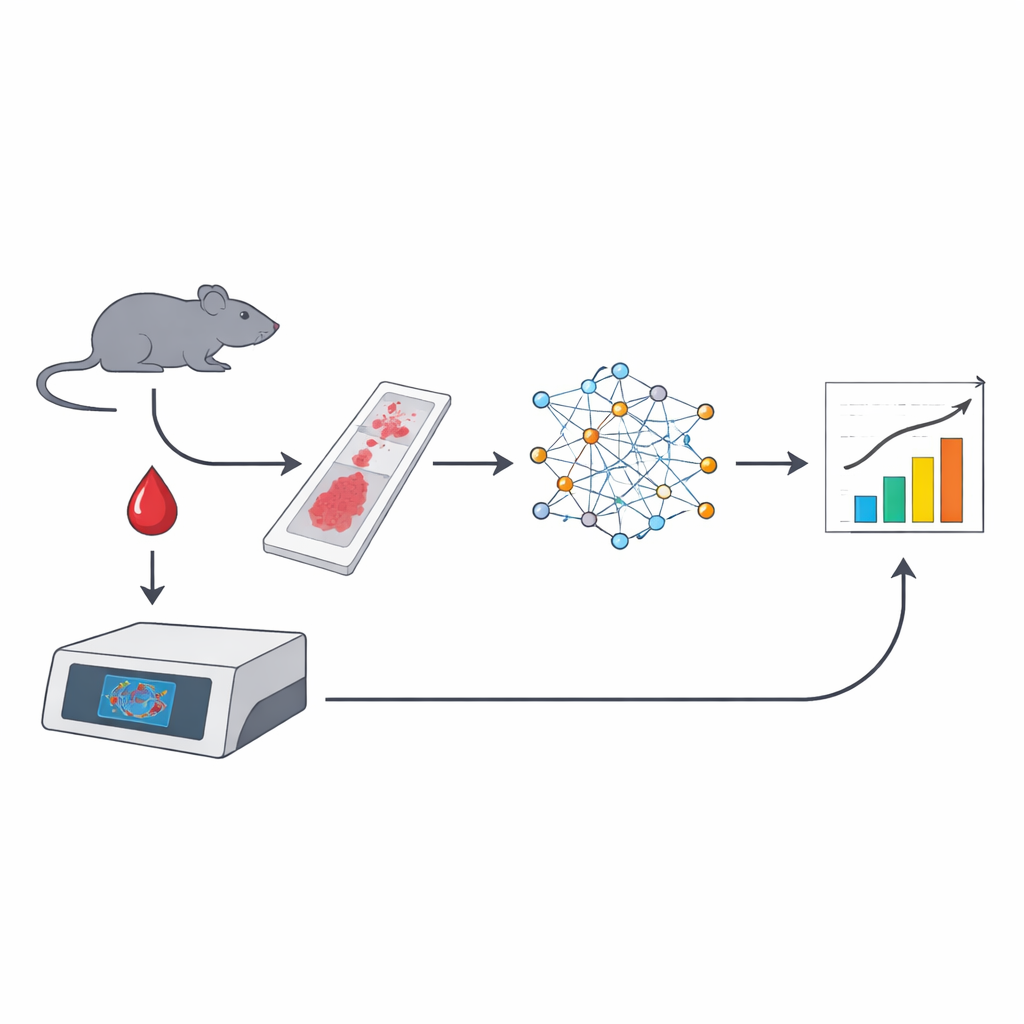
Convertir frotis de sangre en datos con IA
El equipo construyó una tubería automatizada que parte de frotis sanguíneos estándar de ratones, teñidos bien con un colorante fluorescente para ADN o con los tintes May–Grünwald Giemsa habituales en los laboratorios hospitalarios. Se escanearon portaobjetos completos a alta resolución, y se entrenaron modelos supervisados de aprendizaje profundo para reconocer glóbulos rojos, detectar micronúcleos y distinguir reticulocitos inmaduros de eritrocitos maduros a partir de sutiles diferencias de tamaño y color. A partir de una sola imagen, el sistema pudo analizar más de 100.000 células, marcar las que llevaban micronúcleos e incluso contar células que contenían más de un micronúcleo, algo que la citometría de flujo convencional no puede hacer fácilmente.
Relacionar pequeños cambios en la sangre con la potencia del fármaco
Los investigadores preguntaron luego si la frecuencia de glóbulos rojos positivos para micronúcleos se correlacionaba con la exposición a quimioterapia que daña el ADN y con fármacos que bloquean la respuesta al daño del ADN, como los inhibidores de PARP. En ratones tratados con cisplatino o paclitaxel, los recuentos basados en IA captaron los aumentos esperados de células micronucleadas. En ratones con tumores tratados con los inhibidores de PARP olaparib o saruparib, dosis mayores produjeron incrementos mayores de células portadoras de micronúcleos y una mayor reducción tumoral. Tras varias semanas de dosificación diaria, pequeñas muestras sanguíneas seriadas (de solo unos 5 microlitros cada una) permitieron al equipo seguir cómo los micronúcleos se acumulaban lentamente y luego disminuían al detener el tratamiento. Al comparar su método basado en portaobjetos con la citometría de flujo estándar, ambos enfoques concordaron estrechamente, mostrando que el nuevo flujo de trabajo es preciso y robusto.
Enfocarse en las células sanguíneas jóvenes para señales más nítidas
Como las células rojas jóvenes (reticulocitos) son especialmente propensas a contener micronúcleos recientes, los investigadores entrenaron sus algoritmos para dividir la población de eritrocitos en células inmaduras y maduras en portaobjetos teñidos de rutina. Esta refinación reveló que los micronúcleos estaban mucho más enriquecidos y eran más dinámicos en los reticulocitos que en las células más viejas, aportando una señal de actividad del fármaco más sensible y de respuesta más rápida. Las imágenes de portaobjetos completos también permitieron monitorizar la calidad de la muestra en sí —por ejemplo, detectando glóbulos rojos que se habían deformado por un almacenamiento deficiente— de modo que los portaobjetos de mala calidad podían señalarse antes del análisis, un paso importante para el uso clínico eventual.
Qué podría significar esto para la atención del cáncer en el futuro
El estudio demuestra que una minúscula muestra de sangre, una tinción de portaobjetos estándar y una tubería de imagen impulsada por IA pueden, en conjunto, ofrecer una medida escalable y mínimamente invasiva de la intensidad con la que los fármacos que apuntan al ADN afectan al organismo. Aunque el trabajo se realizó en ratones y los glóbulos rojos solo son un sustituto de lo que ocurre dentro de los tumores, la fuerte relación entre las señales de micronúcleos y la respuesta tumoral sugiere que este enfoque podría convertirse en una herramienta práctica en el desarrollo de fármacos y, eventualmente, en ensayos clínicos. En términos sencillos, contar estos microscópicos “puntos” de ADN en la sangre puede ayudar a investigadores y clínicos a ajustar dosis, comparar nuevos medicamentos y seguir los efectos del tratamiento a lo largo del tiempo, sin biopsias repetidas e invasivas.
Cita: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Palabras clave: micronúcleos, glóbulos rojos, inhibidores de PARP, patología digital, respuesta al daño del ADN