Clear Sky Science · es
Posible efecto gonadal beneficioso de la sitagliptina frente a la disfunción testicular inducida por paclitaxel mediante la modulación de la vía de señalización PERK/CHOP/NLRP3/Sestrin2
Por qué este estudio importa para los pacientes con cáncer
La quimioterapia salva vidas pero puede dañar la fertilidad de forma silenciosa, sobre todo en los hombres. Un fármaco oncológico muy utilizado, el paclitaxel, es conocido por perjudicar los testículos y reducir la calidad espermática. Este estudio en ratas plantea una pregunta práctica con clara relevancia humana: ¿puede una pastilla para la diabetes ya aprobada, la sitagliptina, reutilizarse para proteger el sistema reproductor masculino frente a los efectos secundarios del paclitaxel sin interferir con su papel anticáncer?
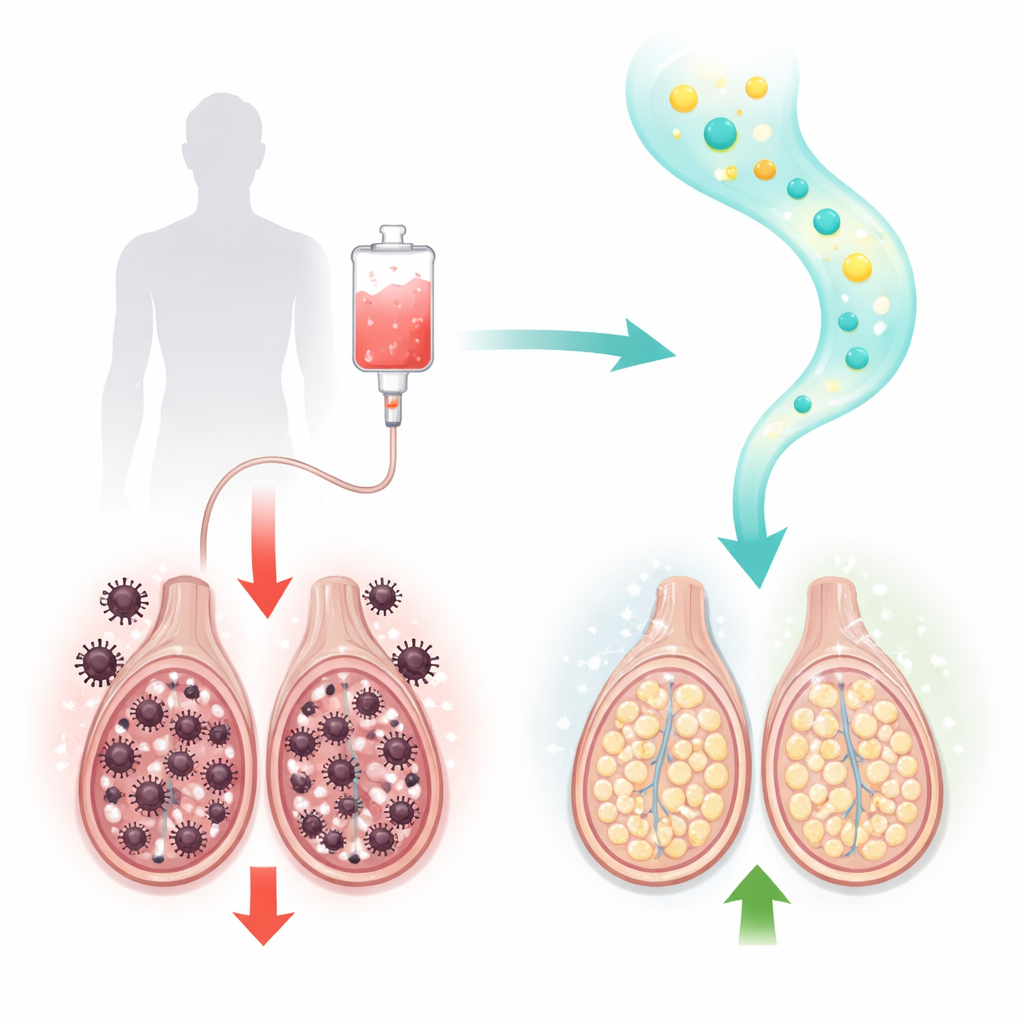
Un fármaco habitual contra el cáncer con un coste oculto
El paclitaxel es un tratamiento básico para el cáncer de mama, ovario, pulmón y otros tumores sólidos. Actúa bloqueando la maquinaria de división celular de las células cancerosas de crecimiento rápido. Desafortunadamente, las células en división de órganos sanos también son vulnerables. En ratas macho, el tratamiento con paclitaxel provocó signos clásicos de lesión testicular: el recuento, la motilidad y la viabilidad espermática cayeron bruscamente, mientras aumentaron los espermatozoides con morfología anormal. Al microscopio, los investigadores observaron túbulos seminíferos dañados (donde se producen los espermatozoides) y células de Leydig productoras de hormonas lesionadas, junto con adelgazamiento de las capas tisulares. Los análisis sanguíneos confirmaron que la testosterona y una enzima clave necesaria para su síntesis, la 17β‑hidroxiesteroide deshidrogenasa, se redujeron notablemente.
Un fármaco para la diabetes como protector inesperado
La sitagliptina se prescribe ampliamente para controlar la glucemia en personas con diabetes tipo 2. Trabajos previos sugirieron que, más allá de sus efectos metabólicos, la sitagliptina puede atenuar el estrés oxidativo nocivo, la inflamación y la muerte celular en órganos como el hígado, el riñón y el cerebro. Sobre esa base, los investigadores dividieron a las ratas macho en cuatro grupos: controles sin tratar, un grupo solo con paclitaxel y dos grupos que recibieron paclitaxel más una dosis baja o alta de sitagliptina durante dos semanas. Luego compararon la calidad del semen, los niveles hormonales, la estructura tisular y un conjunto de “sistemas de alarma” moleculares dentro de los testículos que detectan estrés y desencadenan inflamación y suicidio celular.
Cómo la sitagliptina calmó el estrés celular y la inflamación
El paclitaxel llevó a los testículos a un estado de estrés oxidativo y estrés interno: aumentaron los subproductos dañinos (medidos como malondialdehído), mientras que las defensas naturales como el glutatión reducido y la enzima catalasa disminuyeron. En el interior de las células, la fábrica de plegamiento de proteínas conocida como retículo endoplásmico activó una vía de peligro llamada PERK–CHOP, una señal de que el estrés prolongado está orientando a las células hacia la muerte. Al mismo tiempo, un complejo proteico inflamatorio (NLRP3) se volvió altamente activo, elevando mediadores inflamatorios como la interleucina‑1β y activando una cascada de proteínas implicadas en la muerte celular, como la citocromo c y la caspasa‑3. La sitagliptina revirtió gran parte de esto. Ambas dosis redujeron el daño oxidativo y restauraron las defensas antioxidantes. Disminuyeron notablemente la activación de la vía de estrés PERK–CHOP y frenaron la inflamación y la apoptosis mediadas por NLRP3. Una proteína protectora llamada Sestrin2, que ayuda a eliminar especies reactivas y se ha asociado con una mejor calidad espermática, aumentó con la sitagliptina tanto a nivel de gen como de proteína.
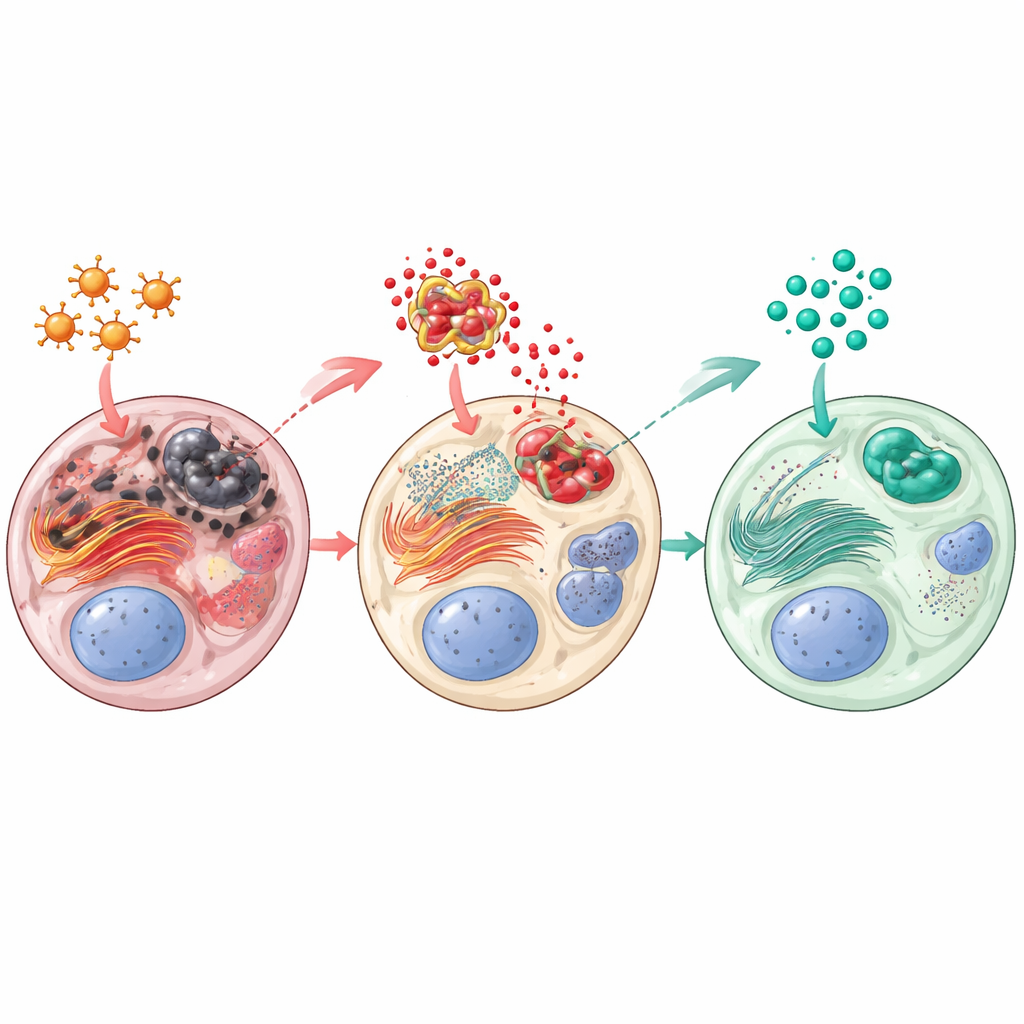
Mejor esperma, tejido más sano, hormonas más fuertes
Las mejoras bioquímicas se tradujeron en beneficios funcionales tangibles. Las ratas tratadas con sitagliptina tras el paclitaxel presentaron mayor recuento espermático, mejor motilidad y menos espermatozoides anómalos que los animales que recibieron solo paclitaxel, siendo la dosis más alta de sitagliptina la que se acercó más a la normalidad. La testosterona y la 17β‑hidroxiesteroide deshidrogenasa se recuperaron, lo que sugiere que la producción de esteroides por las células de Leydig se estaba restableciendo. Tanto en microscopía óptica como electrónica, los testículos tratados con sitagliptina mostraron túbulos seminíferos más ordenados, más células de Leydig, capas celulares más gruesas y saludables y menos distorsiones estructurales. En conjunto, el fármaco ayudó a preservar la arquitectura y la función necesarias para la producción continua de espermatozoides.
Qué podría significar esto para los hombres que reciben quimioterapia
Este trabajo en animales sugiere que la sitagliptina puede atenuar de forma significativa el daño testicular inducido por paclitaxel al silenciar una red de señales perjudiciales: estrés oxidativo, estrés por plegamiento de proteínas, inflamación y muerte celular programada —principalmente a través del aumento de Sestrin2 y la inhibición del eje PERK/CHOP/NLRP3. Dado que la sitagliptina ya se usa en clínica para la diabetes, destaca como un candidato realista para evaluar como coadyuvante protector de la fertilidad en hombres que reciben paclitaxel, en especial aquellos que también son diabéticos. Los autores subrayan que aún son necesarios estudios en humanos, pero sus hallazgos abren una posibilidad esperanzadora: una pastilla conocida podría, algún día, ayudar a los pacientes con cáncer a preservar no solo la vida sino también las posibilidades de tener hijos.
Cita: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Palabras clave: paclitaxel, sitagliptina, fertilidad masculina, estrés oxidativo, toxicidad testicular