Clear Sky Science · es
La disrupción de la homeostasis de neutrófilos se asocia con alteraciones funcionales en las mitocondrias de pacientes críticamente enfermos por COVID-19
Por qué esto importa para los pacientes con COVID-19
La mayoría sabe ya que el COVID-19 es más que una infección pulmonar, pero todavía se están desvelando los mecanismos por los que el virus convierte las propias defensas del cuerpo en un problema. Este estudio examina detenidamente a los neutrófilos, un tipo común de glóbulo blanco, en pacientes con COVID-19 potencialmente mortales ingresados en cuidados intensivos. Al estudiar cómo estas células viven, mueren y usan sus pequeñas “centrales” internas (mitocondrias), los investigadores revelan un patrón de neutrófilos persistentes y sobreactivados que puede ayudar a explicar la inflamación sostenida, el daño vascular y la lesión orgánica en la enfermedad grave.
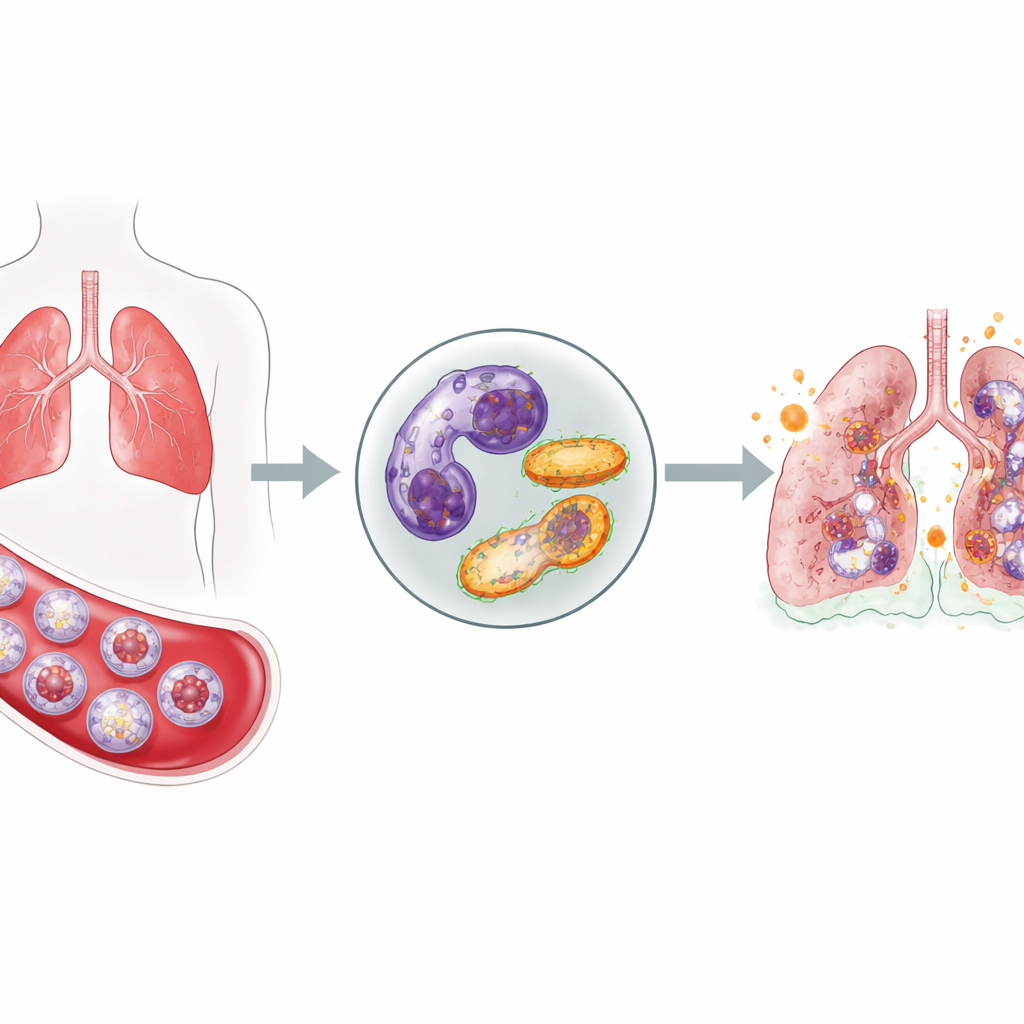
Células de primera línea que no se retiran
Los neutrófilos son de los primeros en responder a una infección: llegan rápido al torrente sanguíneo, penetran en los tejidos y liberan moléculas tóxicas para matar microbios invasores. Normalmente, tras cumplir su función, se autodestruyen de forma ordenada y son eliminados, lo que evita que dañen el tejido sano. En los pacientes críticamente enfermos por COVID-19, el equipo observó un panorama muy distinto. En comparación con voluntarios sanos, estos pacientes presentaban un aumento de neutrófilos en sangre y, de forma significativa, muchos de ellos eran células inmaduras que habían sido expulsadas apresuradamente de la médula ósea. Al mismo tiempo, múltiples pruebas indicaron que menos neutrófilos estaban sufriendo su muerte programada habitual, lo que sugiere que estas células agresivas persisten más tiempo del debido.
Señales genéticas sutiles pero un patrón claro de supervivencia
Los investigadores también analizaron pequeñas moléculas reguladoras llamadas microARN en neutrófilos de supervivientes y no supervivientes de la UCI. Algunas de estas moléculas estaban alteradas de maneras que, sobre el papel, apuntan a vías alteradas que controlan la muerte celular y el equilibrio del calcio. Sin embargo, al medir marcadores directos de muerte celular no observaron diferencias importantes entre supervivientes y no supervivientes: ambos grupos mostraron una reducción similar de la autodestrucción de neutrófilos en comparación con personas sanas. Esto significa que los patrones de microARN son más bien pistas para estudios futuros que indicadores firmes de pronóstico, y subrayan que la incapacidad general de los neutrófilos para apagarse es una característica compartida de la COVID-19 grave.
Desplazamientos de calcio y centrales sobrecargadas
Para entender por qué los neutrófilos no morían a tiempo, el equipo se centró en dos sistemas estrechamente vinculados dentro de las células: las señales de calcio y las mitocondrias. Los iones calcio actúan como pequeños interruptores para muchas decisiones celulares, incluida la autodestrucción. Los investigadores encontraron que los neutrófilos de pacientes con COVID-19 grave tenían menos calcio libre en su interior, junto con niveles reducidos de proteínas clave que normalmente ayudan a trasladar el calcio a las mitocondrias y a abrir una válvula de seguridad que puede desencadenar la muerte celular. Al mismo tiempo, las propias mitocondrias estaban inusualmente «sobrecargadas», con un gradiente eléctrico mayor a través de sus membranas y un consumo de oxígeno incrementado, especialmente a través de una vía respiratoria principal. En lugar de apagarse, estas mitocondrias hiperactivas producían más moléculas reactivas de oxígeno, que pueden dañar los tejidos circundantes y alimentar la inflamación.
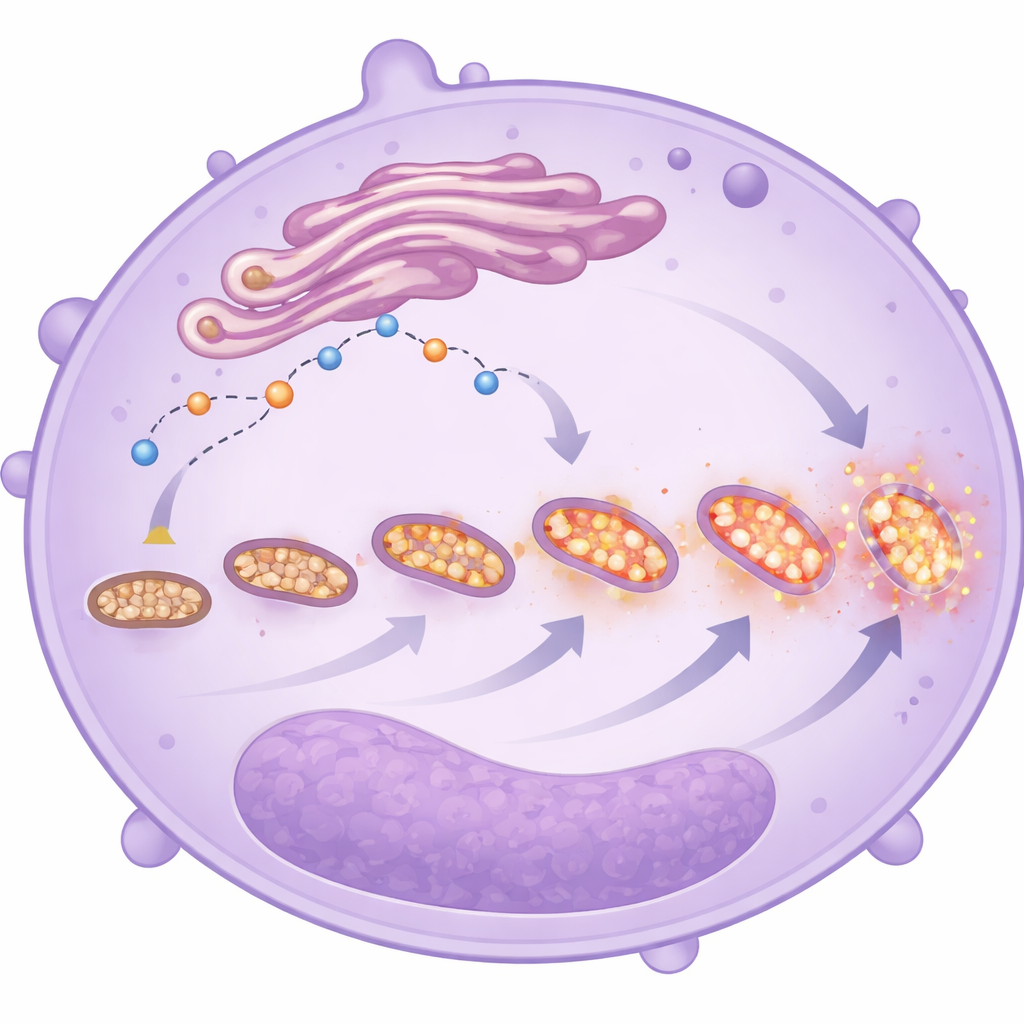
Mitocondrias estresadas y fragmentadas
Imágenes de microscopía electrónica y colorantes fluorescentes ofrecieron una visión más cercana de la forma y el comportamiento de estas mitocondrias. En los neutrófilos de los pacientes más graves, las mitocondrias eran más numerosas pero más pequeñas y más fragmentadas —rasgos que suelen señalar estrés—. Estas células también mostraron niveles superiores de especies reactivas de oxígeno mitocondriales, independientemente de si el paciente finalmente sobrevivió. Junto con el manejo alterado del calcio y la muerte celular retrasada, estos cambios dibujan la imagen de neutrófilos que han cambiado su estrategia energética: en lugar de depender principalmente de la descomposición simple de azúcar, se apoyan más en el metabolismo mitocondrial, sobre todo en células inmaduras. Este cambio puede mejorar su capacidad para migrar, persistir y liberar moléculas dañinas en los pulmones y otros órganos, aunque el estudio no puede demostrar que sean la causa directa de peores resultados.
Qué podría significar esto para la atención futura
En términos sencillos, el estudio sugiere que en la COVID-19 crítica los neutrófilos se vuelven demasiados, demasiado jóvenes y demasiado difíciles de apagar. Sus señales internas de calcio y sus mitocondrias se reconfiguran de un modo que los mantiene vivos y muy activos, produciendo ráfagas de compuestos oxigenados dañinos. Aunque el trabajo es observacional y no establece causalidad, destaca varios posibles «mandos de control» en estas células —como reguladores del calcio y puntos de control mitocondriales— que algún día podrían ser diana para reconducir suavemente a los neutrófilos hacia un comportamiento normal. Si investigaciones futuras confirman estas ideas, tratamientos que restauren el cierre adecuado de los neutrófilos o calmen sus mitocondrias sobrecargadas podrían ayudar a reducir el daño colateral que estas células cruciales causan durante la COVID-19 grave y posiblemente en otras enfermedades críticas.
Cita: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Palabras clave: COVID-19, neutrófilos, mitocondrias, inflamación, enfermedad crítica