Clear Sky Science · es
Síntesis y evaluación biológica de complejos de base de Schiff de ibuprofeno/o‑vanilina con actividades antiinflamatoria, antiproliferativa y anti‑SARS‑CoV‑19
Por qué tiene importancia mejorar un analgésico conocido
El ibuprofeno es uno de los medicamentos más utilizados en el mundo para el dolor y la fiebre, pero su uso prolongado puede irritar el estómago y nunca fue diseñado para combatir infecciones, cánceres o nuevos virus. En este estudio, los químicos reingenierizan el ibuprofeno fijándolo a una molécula natural similar a la vainilla y luego enlazándola con distintos metales. El resultado es una familia de nuevos compuestos que actúan no solo como analgésicos, sino como potenciales antibióticos, agentes anticancerígenos, fármacos antiinflamatorios e incluso inhibidores de una enzima clave del SARS‑CoV‑2, a la vez que aportan pistas sobre cómo diseñar medicamentos más inteligentes a partir de fármacos cotidianos.
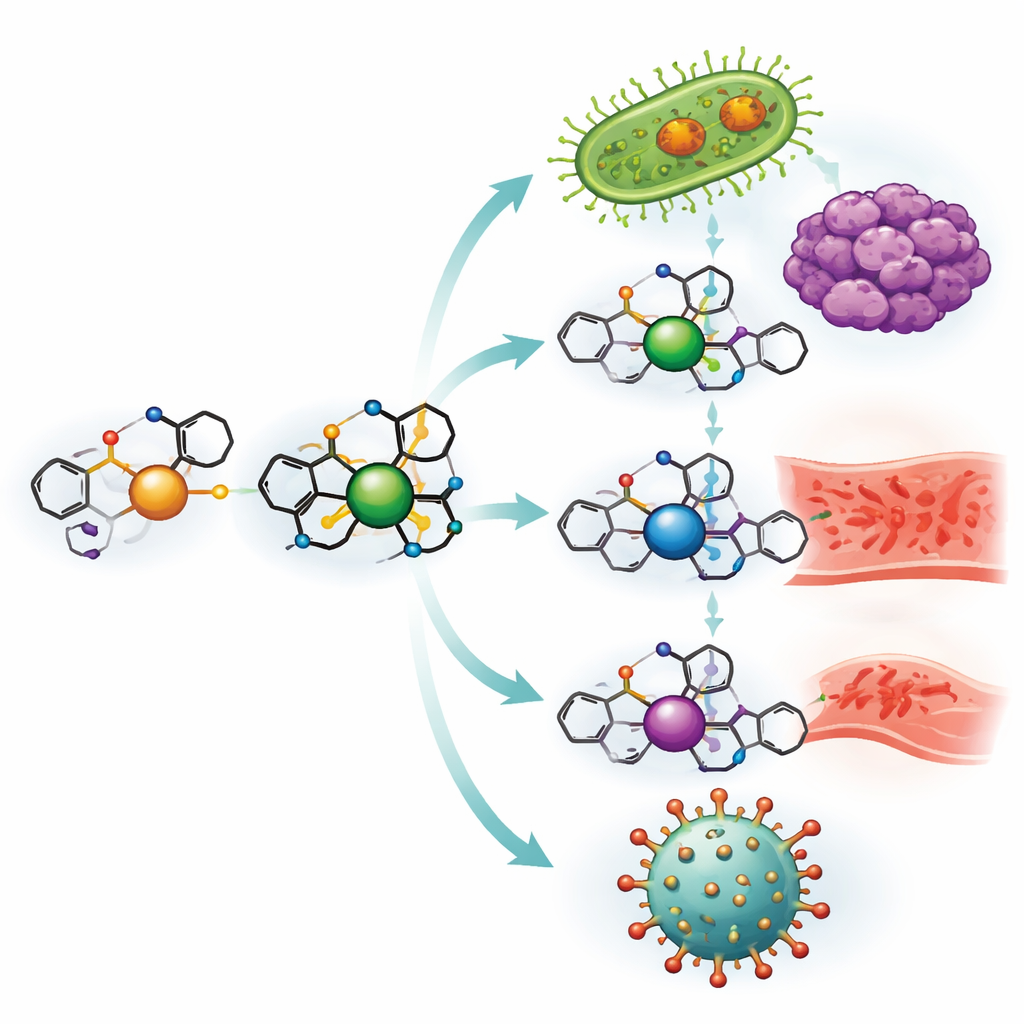
Construyendo nuevas moléculas con carácter farmacológico a partir del ibuprofeno
El equipo comenzó transformando el ibuprofeno en un bloque de construcción más versátil y luego lo unió a o‑vanilina, un pariente químico cercano del compuesto responsable del aroma de la vainilla. Juntos forman una ligadura tipo “base de Schiff”, esencialmente una garra a medida que puede sujetar iones metálicos. Esta ligadura se combinó por separado con sales de cobre, níquel, zinc y vanadio para producir cuatro complejos metálicos distintos. Pruebas de laboratorio cuidadosas, incluidas medidas del comportamiento al fundir, absorción de luz, propiedades magnéticas y estructura cristalina, confirmaron cómo la ligadura envuelve a cada metal y cuán estables son los complejos resultantes, incluso a altas temperaturas y a lo largo de un amplio rango de acidez.
Cómo interactúan los complejos con células y ADN
Puesto que la potencia de un fármaco a menudo depende de cómo se encuentra con dianas biológicas, los investigadores exploraron cómo estos nuevos complejos interactúan con el ADN y con células vivas. En experimentos de tubo de ensayo, el complejo de cobre en particular se unió fuertemente a hebras de ADN y fue capaz de dañarlas o “cortarlas”, un comportamiento observado con frecuencia en agentes anticancerígenos y antibacterianos potentes. Al probarlos frente a líneas celulares humanas de cáncer de mama, colon e hígado, los cuatro complejos resultaron más tóxicos para las células cancerosas que la ligadura a base de ibuprofeno sola, con el complejo de cobre aproximándose a la potencia del quimioterápico vinblastina a dosis similares.
Combatiendo microbios, hongos e inflamación
Esos mismos compuestos se sometieron a pruebas contra microbios causantes de enfermedades comunes, incluidas bacterias Gram‑positivas y Gram‑negativas y dos hongos problemáticos. De nuevo, los complejos metálicos superaron a la ligadura libre, y el cobre lideró el grupo, inhibiendo con fuerza tanto bacterias como hongos. Los autores interpretan esto mediante la teoría de la quelación: una vez que el metal está retenido por la ligadura, su carga queda parcialmente enmascarada y el complejo completo se vuelve más lipófilo, lo que le permite penetrar en las membranas microbianas y alterar enzimas vitales. En una prueba simple de inflamación basada en la desnaturalización de proteína de huevo por calor, los nuevos complejos también redujeron la desnaturalización proteica con más eficacia que el propio ibuprofeno, lo que sugiere que podrían atenuar procesos inflamatorios a dosis más bajas.
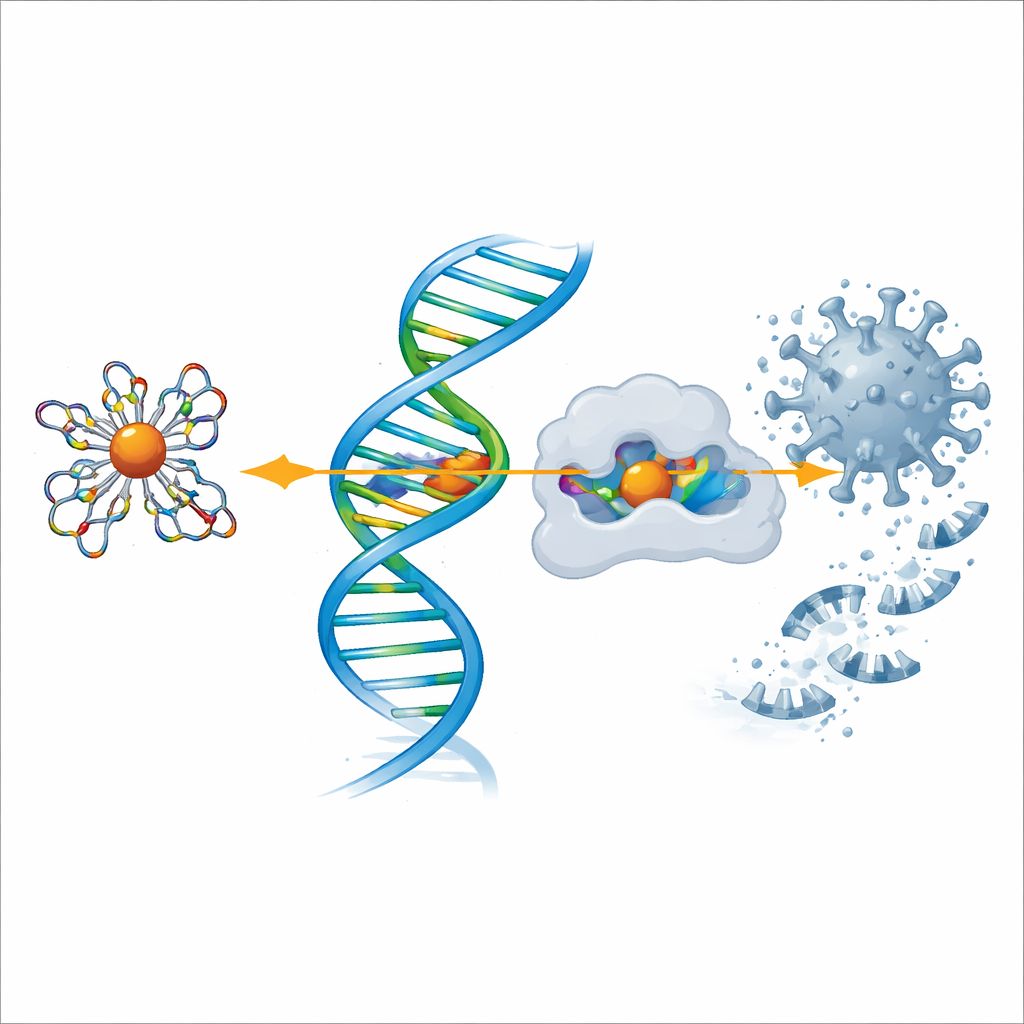
Investigando la acción contra enzimas del COVID‑19 y del dolor
Para explorar el potencial antiviral, el equipo empleó modelado por ordenador para acoplar la ligadura y cada complejo metálico en las formas tridimensionales de dos proteínas clave: la proteasa principal del SARS‑CoV‑2, que el virus usa para cortar sus poliproteínas, y la ciclooxigenasa‑2 (COX‑2), una enzima implicada en el dolor y la inflamación. Las simulaciones mostraron que los complejos, especialmente los de cobre y zinc, encajan bien en los huecos activos de estas proteínas y forman múltiples interacciones estabilizadoras. Cuanto más negativa es la energía de unión calculada, más fuerte se predice que es la unión, y de nuevo el complejo de cobre destacó, seguido de cerca por el zinc y el níquel, apoyando los hallazgos de laboratorio sobre el comportamiento antiinflamatorio y antimicrobiano.
Qué podría significar esto para futuros medicamentos
En conjunto, el trabajo demuestra que un fármaco de venta libre familiar puede convertirse en una herramienta química multiuso al fusionarlo con un socio orgánico cuidadosamente elegido y con el ion metálico adecuado. Entre los cuatro metales probados, el cobre produjo el candidato más prometedor, con potentes actividades antibacteriana, antifúngica, anticancerígena, antiinflamatoria y anti‑SARS‑CoV‑2 predicha por cálculos, mientras que el níquel y el zinc ofrecieron efectos algo más moderados pero aún notables. Aunque estos resultados aún se limitan a fases de laboratorio y modelos por ordenador, apuntan a una estrategia en la que medicamentos cotidianos se “mejoran” convirtiéndolos en complejos metálicos dirigidos que podrían actuar a dosis más bajas y frente a una gama más amplia de enfermedades que los fármacos originales.
Cita: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Palabras clave: derivados de ibuprofeno, complejos metálicos farmacológicos, agentes anticancerígenos, terapia antimicrobiana, proteasa de COVID-19