Clear Sky Science · es
Funcionalización asimétrica catalítica de ésteres borónicos de bicyclo[1.1.0]butano habilitada por migración 1,2 de oxígeno
Por qué importan los anillos cuadrados diminutos
A los químicos les encanta construir nuevos fármacos y materiales ensamblando pequeñas piezas moleculares, como si usaran ladrillos de Lego. Los anillos de carbono de cuatro miembros llamados ciclobutanos son especialmente apreciados porque concentran mucha energía y forma en un espacio reducido, lo que puede modificar el comportamiento de un fármaco en el organismo. Este artículo describe una nueva forma de fabricar esos anillos en una configuración muy controlada y “de una sola mano” (quiral), usando una reacción ingeniosa que obliga a un grupo que contiene oxígeno a saltar de un átomo a otro. El trabajo abre puertas al diseño de moléculas más complejas y precisas para productos farmacéuticos y materiales avanzados.
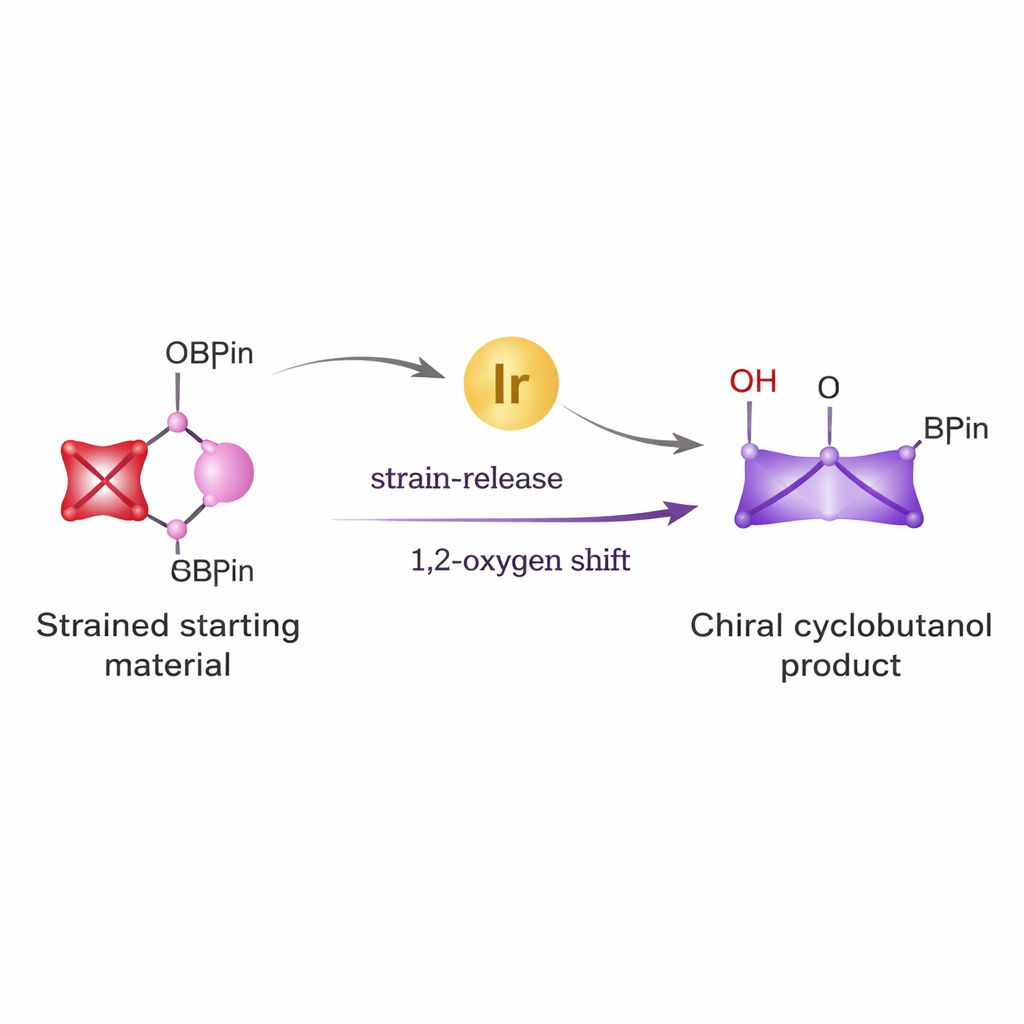
De bloques sencillos a anillos poderosos
Los ciclobutanos aparecen en una variedad de agentes antivirales, candidatos anticancerígenos y otras moléculas bioactivas. Sin embargo, construirlos con la disposición tridimensional exacta necesaria para la medicina ha sido complicado. Las rutas tradicionales a menudo requieren reactivos agresivos y producen mezclas de productos imagen especular que son difíciles de separar. Los autores se propusieron resolver este problema combinando dos ideas potentes: la reactividad inusual de un anillo diminuto y altamente tensionado llamado bicyclo[1.1.0]butano, y la versatilidad de los ésteres borónicos, una familia bien conocida de reactivos ampliamente usada en química de acoplamientos para formar enlaces carbono–carbono.
Convertir una desventaja en una nueva vía reactiva
En las reacciones de acoplamiento catalizadas por metales estándar, los ésteres borónicos forman un complejo intermedio con un alcoxido (una base a base de oxígeno). Este complejo casi siempre sigue una ruta habitual llamada transmetilación, que conduce directamente a nuevos enlaces carbono–carbono o carbono–halógeno. Esa vía “por defecto” ha dificultado explorar otras posibilidades, como desplazar el propio grupo oxígeno. El equipo se dio cuenta de que si partían de un éster borónico de bicyclo[1.1.0]butano, la tensión incorporada del pequeño anillo podría usarse para anular la ruta habitual. Al emparejar este sistema tensionado con un catalizador de iridio y un ligando quiral cuidadosamente seleccionado, esperaban inducir la migración del oxígeno de forma controlada, mientras el anillo se abría y volvía a cerrarse en un ciclobutano.
Un baile por pasos guiado por la tensión
Los experimentos confirmaron que esta estrategia funciona. Usando alcoxidos de litio derivados de una amplia variedad de alcoholes —incluyendo azúcares, terpenos, esteroides y alcoholes alifáticos sencillos— los autores convirtieron ésteres borónicos de bicyclo[1.1.0]butano en ciclobutanoles cis con altos rendimientos y excelente control de la quiralidad. El catalizador de iridio primero forma un complejo alquílico reactivo a partir de una carbonato alílico. Este complejo ataca entonces el sistema tensionado de bicyclo[1.1.0]butano, formando un nuevo enlace carbono–carbono mientras el diminuto anillo se abre. Crucialmente, en lugar de seguir inmediatamente la ruta habitual de transmetilación, el intermedio que contiene boro sufre una sutil rotación del enlace carbono–boro, posicionando el grupo oxígeno unido de modo que pueda desplazarse con limpieza a un átomo de carbono vecino. Esta migración 1,2 de oxígeno fija la disposición cis deseada en el nuevo anillo de ciclobutano.
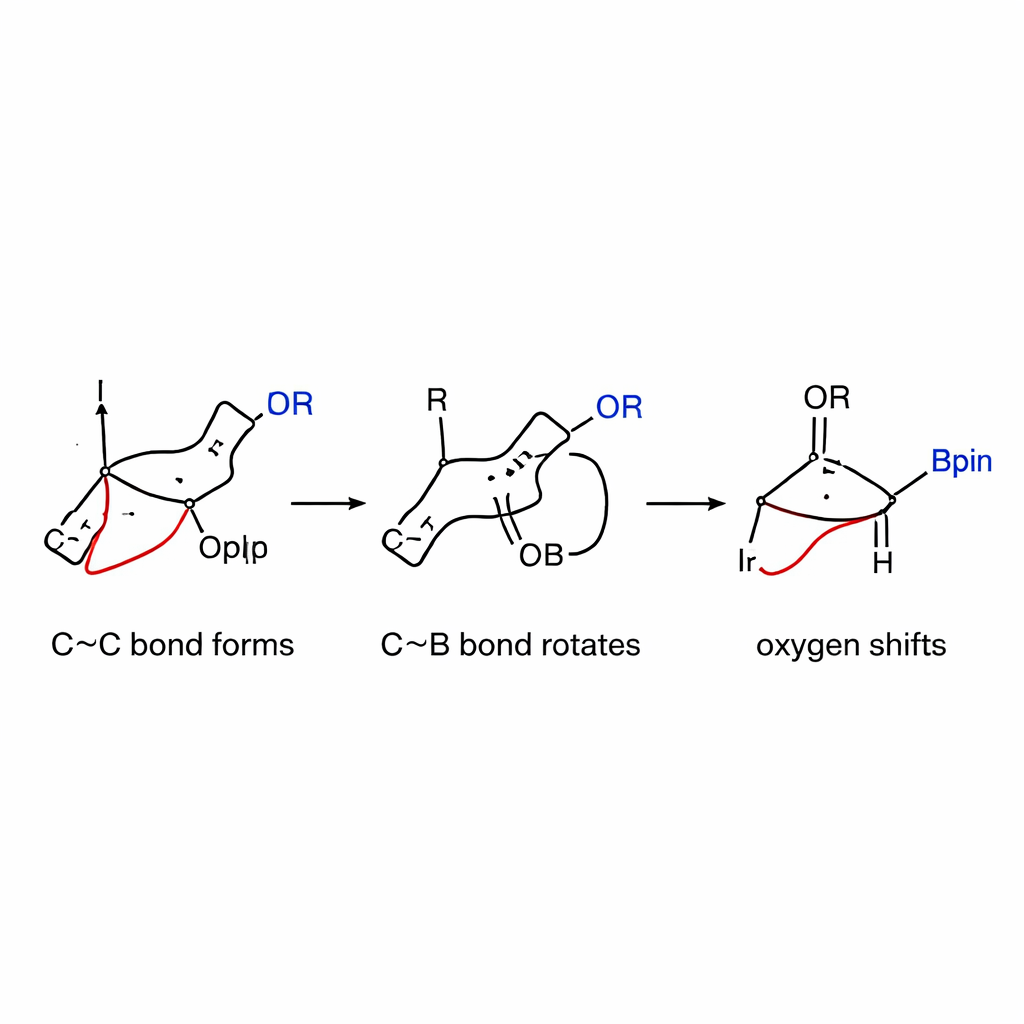
Echando un vistazo al mecanismo
Para entender por qué la reacción es tan selectiva, los autores combinaron mediciones cinéticas con detalladas simulaciones por ordenador. Encontraron que el paso lento y determinante de la velocidad es la formación inicial del enlace carbono–carbono entre la especie iridio–alilo y el complejo boronato tensionado, no la activación previa del carbonato alílico. Pruebas electrónicas mostraron que los socios alílicos que estabilizan carga positiva reaccionan más rápido, lo que respalda un mecanismo en el que se forma un intermedio parcialmente cargado. Los cálculos revelaron además que la rotación alrededor del enlace carbono–boro —anteriormente considerada difícil— presenta una barrera energética sorprendentemente baja en este sistema, gracias a la energía almacenada por la tensión del anillo. Una vez que la rotación ha alineado el grupo oxígeno, el desplazamiento 1,2 progresa con suavidad y de forma preferente para dar el producto cis en lugar de la forma trans más común.
Nuevas herramientas para moldear los medicamentos del futuro
Más allá de probar un punto mecanístico, la reacción produce compuestos versátiles. Los ciclobutanoles conservan una unidad de éster borónico, que puede transformarse en muchos otros grupos funcionales usando química establecida. Los autores mostraron numerosas modificaciones “en etapas tardías”, como hidrogenación, oxidación, metátesis de olefinas y acoplamientos adicionales, todo ello preservando la forma tridimensional precisa del anillo. En términos sencillos, este trabajo convierte una vía colateral que antes era problemática —la migración de oxígeno en complejos boronato— en una poderosa herramienta sintética. Aprovechando la tensión del anillo y un catalizador de iridio finamente afinado, los investigadores proporcionan a los químicos una forma fiable de construir ciclobutanos quirales y complejos que podrían desempeñar papeles clave en fármacos de nueva generación y materiales moleculares avanzados.
Cita: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Palabras clave: ciclobutano, química organoborónica, catálisis asimétrica, bicyclobutano, migración de oxígeno