Clear Sky Science · es
Macrófagos CD19+ asociados a tumores inducen un microambiente inmunosupresor en el carcinoma hepatocelular
Por qué los defensores del cuerpo a veces ayudan al cáncer de hígado
El cáncer de hígado es uno de los más mortales a nivel mundial, en parte porque los tumores pueden convertir al propio sistema inmunitario en un aliado involuntario. Este estudio revela un subconjunto sorprendente de células inmunitarias dentro de los tumores hepáticos que, en lugar de combatir el cáncer, ayudan activamente a que se oculte y crezca. Identificar quiénes son estas células “traidoras” y cómo actúan abre nuevas vías para mejorar la eficacia de la inmunoterapia en personas con carcinoma hepatocelular, la forma más común de cáncer de hígado.
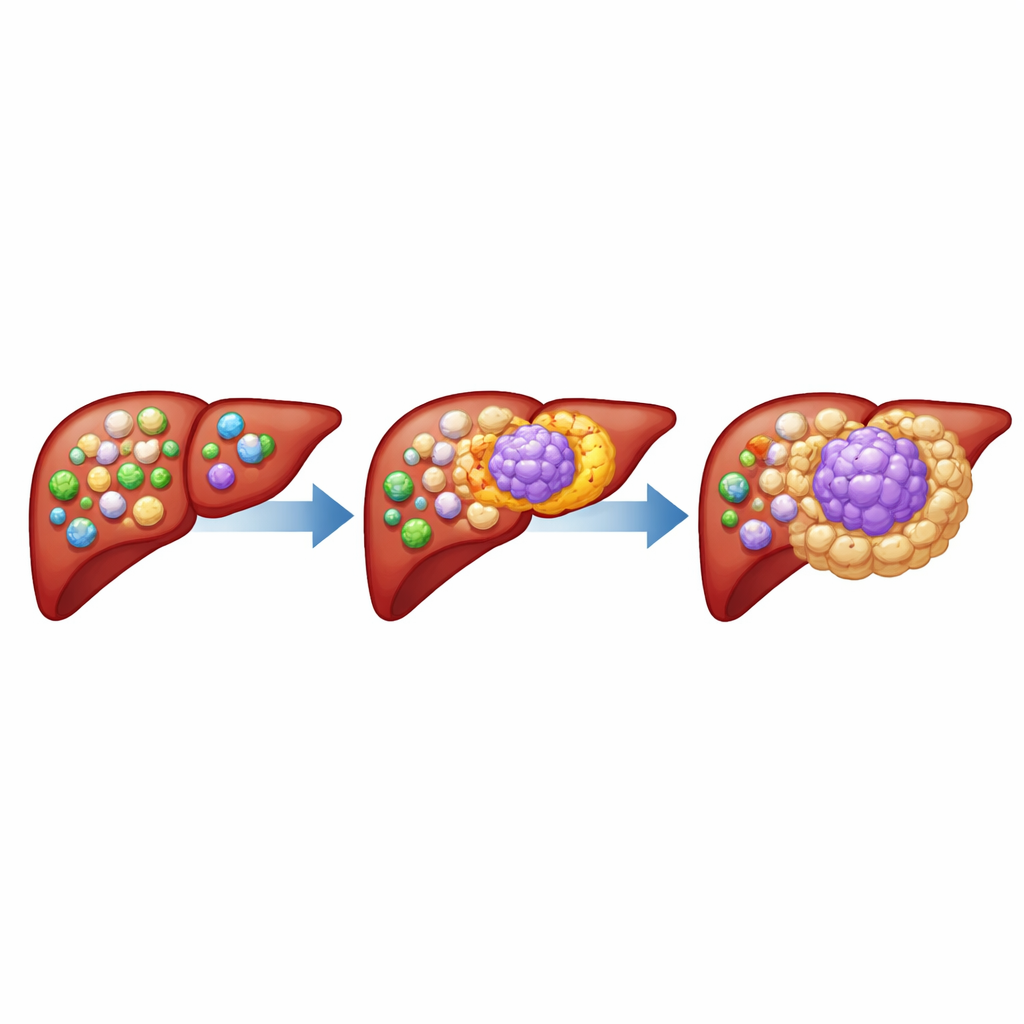
Un grupo especial de células inmunitarias dentro de los tumores
Los autores se centraron en los macrófagos asociados a tumores, células inmunitarias que normalmente fagocitan gérmenes y restos celulares, pero que a menudo se corrompen dentro de los cánceres. Al analizar muestras de tumores hepáticos de numerosos pacientes, descubrieron un subgrupo distinto de macrófagos que presentan en su superficie una molécula llamada CD19, habitualmente propia de las células B y no de los macrófagos. Estos macrófagos CD19-positivos eran mucho más abundantes en los tumores hepáticos que en el hígado sano circundante o en la sangre, y también estaban enriquecidos en varios otros cánceres sólidos. Análisis de una sola célula confirmaron que se trata de verdaderos macrófagos con un perfil genético y proteico único, no de células B mal identificadas.
Cómo estas células configuran un vecindario favorable al tumor
Los pacientes cuyos tumores contenían muchos macrófagos CD19-positivos tendían a presentar cánceres más grandes, más agresivos y una supervivencia más corta. Las muestras tumorales ricas en estas células mostraron menos células CD8 T asesinas y más células T reguladoras, un patrón típico de un entorno altamente inmunosupresor. En modelos murinos, añadir macrófagos CD19-positivos a células de cáncer hepático favoreció el crecimiento tumoral y redujo la presencia de células T útiles, mientras aumentaba otros tipos de células mieloides supresoras. De forma importante, cuando los investigadores emplearon células T diseñadas para reconocer CD19 y eliminar selectivamente estos macrófagos, los tumores hepáticos se redujeron incluso en ratones carentes de células B normales, señalando a los macrófagos como dianas terapéuticas.
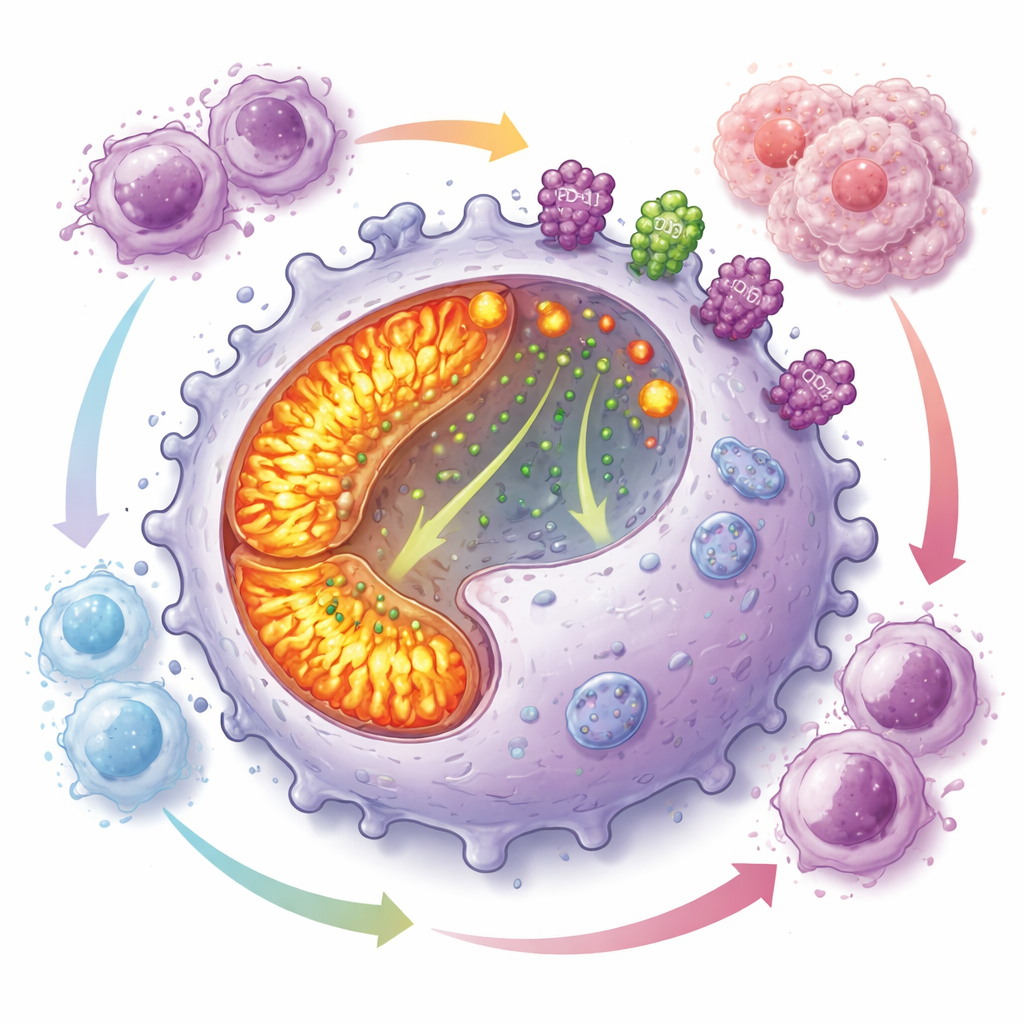
Un programa hambriento de energía que atenúa el ataque inmunitario
Indagando más, el equipo encontró que los macrófagos CD19-positivos mantienen sus “centrales energéticas” internas a toda marcha. Sus mitocondrias, los orgánulos generadores de energía, eran más numerosas y más activas que en otros macrófagos, con mayor fosforilación oxidativa y especies reactivas de oxígeno. A pesar de este estado energético, estas células tenían una pobre capacidad para fagocitar objetivos pero se dividían rápidamente, lo que les permitía acumularse en los tumores. Al mismo tiempo, mostraban altos niveles de PD-L1 y CD73 en su superficie —dos moléculas conocidas por inhibir las respuestas de las células T y generar adenosina, una pequeña molécula que suprime poderosamente la inmunidad. Experimentos de cocultivo demostraron que estos macrófagos inhiben con fuerza el crecimiento de múltiples tipos de células T.
El interruptor maestro detrás de los macrófagos traidores
Los investigadores identificaron un factor de transcripción llamado PAX5 como el impulsor central de este programa nocivo en macrófagos. PAX5 es conocido principalmente por dirigir el desarrollo de las células B, pero aquí estaba altamente activo en macrófagos CD19-positivos. Forzar la expresión de PAX5 en células de tipo macrófago aumentó la biogénesis mitocondrial, incrementó la producción de energía y elevó los niveles de proteína —pero no de ARNm— de PD-L1, CD73 y CD19. Experimentos mecanísticos mostraron que PAX5 facilita la entrada de calcio en las mitocondrias, reduciendo el calcio en el citosol y evitando que un regulador clave llamado TFEB entre en el núcleo. Con TFEB retenido, la producción y función de lisosomas disminuye, por lo que proteínas como PD-L1 y CD73 ya no se degradan eficientemente y, en cambio, se acumulan en la superficie celular, intensificando la supresión inmune.
Convertir el descubrimiento en mejores opciones de tratamiento
Dado que estos macrófagos dependen en gran medida de la actividad de CD73 y del metabolismo mitocondrial, los autores probaron si bloquear estas vías podía mejorar la respuesta a la inmunoterapia. En cáncer hepático murino, combinar el bloqueo de PD-L1 con anticuerpos contra CD73 o con un inhibidor de CD73 condujo a tumores más pequeños, más infiltración de células T y menos proliferación de células cancerosas. De modo similar, asociar anticuerpos contra PD-L1 con un inhibidor de la fosforilación oxidativa mitocondrial mejoró el control tumoral y aumentó la entrada de células inmunitarias en los tumores. De manera llamativa, estos beneficios desaparecieron en ratones cuyos macrófagos carecían de PAX5, confirmando que los efectos de los fármacos estaban ligados a desactivar el programa macrófago CD19-positivo impulsado por PAX5. En conjunto, el trabajo sugiere que dirigir selectivamente este subconjunto de macrófagos —vía terapias celulares dirigidas a CD19, inhibición de CD73 o fármacos metabólicos— podría ayudar a convertir un tumor hepático inmunológicamente “frío” en uno que responda mucho mejor a los tratamientos con inhibidores de puntos de control existentes.
Cita: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Palabras clave: carcinoma hepatocelular, macrófagos asociados a tumores, inmunoterapia, PD-L1 y CD73, metabolismo mitocondrial