Clear Sky Science · es
La expresión tumoral específica de HORMAD1 perturba el arresto mitótico y aumenta la sensibilidad a inhibidores de quinasas mitóticas
Por qué importa esto para el tratamiento del cáncer
Cuando nuestras células se dividen, dependen de complejos controles de seguridad para pasar la correcta dotación de cromosomas. El cáncer con frecuencia secuestra o debilita estas salvaguardas, conduciendo a genomas caóticos que tanto impulsan la enfermedad como determinan la respuesta de los tumores a los fármacos. Este estudio revela cómo una proteína inusual llamada HORMAD1, normalmente activa solo en células reproductoras, se reactiva en muchos cánceres de mama agresivos y en otros tumores. Al sabotear sutilmente un punto de control clave de la división celular, HORMAD1 hace que las células cancerosas sean más inestables, pero también extraordinariamente vulnerables a una nueva clase de fármacos experimentales.
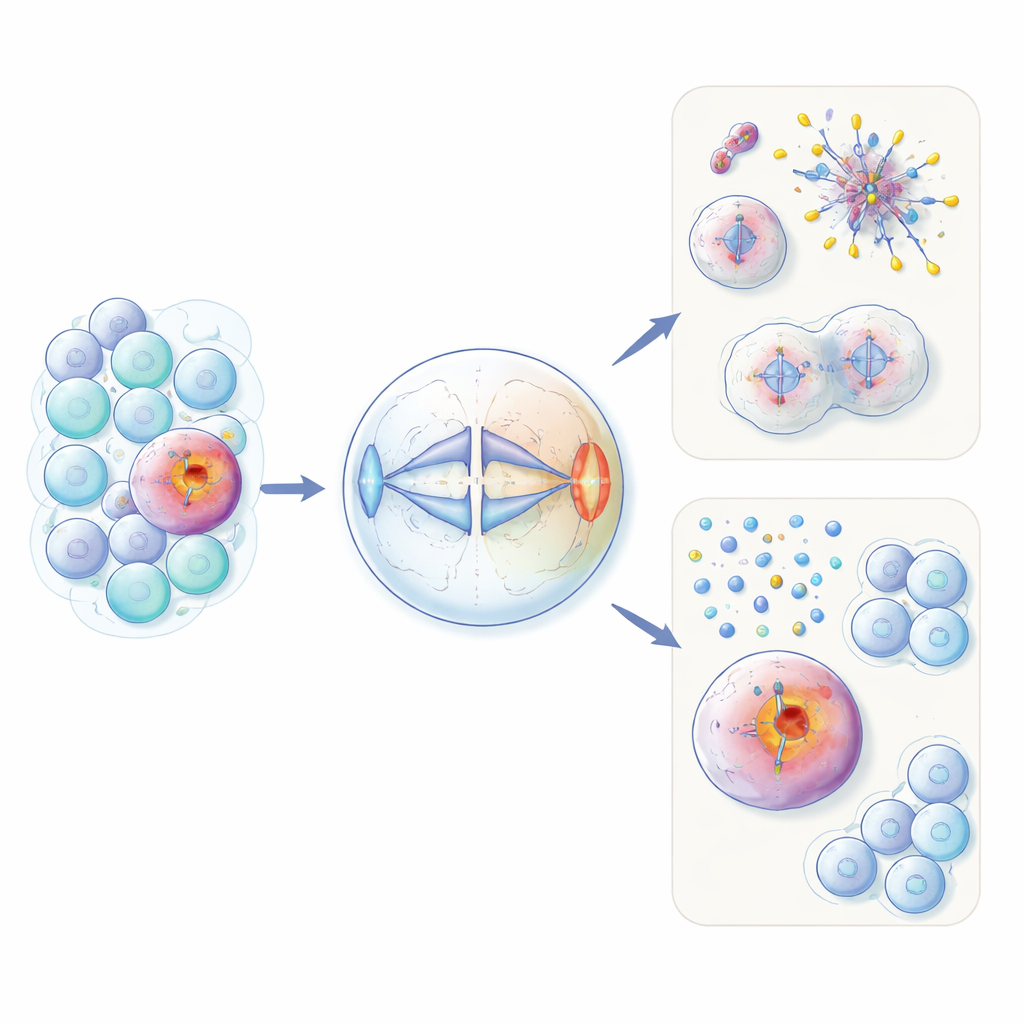
Una proteína de la fertilidad desplazada en células cancerosas
HORMAD1 aparece normalmente solo en células germinales, donde se forman óvulos y espermatozoides. Allí, ayuda a gestionar la recombinación del ADN y el control de calidad durante el tipo especial de división celular llamado meiosis. Los autores muestran que en aproximadamente el 60% de los cánceres de mama triple negativos —y en subgrupos de varios otros tipos tumorales— esta proteína se reactiva de forma inapropiada. Usando tanto células no cancerosas modificadas como líneas celulares tumorales, encontraron que el exceso de HORMAD1 altera la separación pareja de los cromosomas durante la división celular ordinaria. Las células que expresan HORMAD1 desarrollaron más cromosomas rezagados, cromosomas de más o de menos (aneuploidía) y pequeñas “micronúcleos” con ADN, todos rasgos característicos del caos genómico observado en cánceres agresivos.
Cómo funcionan normalmente los controles de seguridad de la división celular
Para dividirse correctamente, una célula construye un huso de fibras de microtúbulos que se unen a cada cromosoma. Un sistema de vigilancia conocido como el punto de control de ensamblaje del huso actúa como un freno sensible a la tensión: si algún cromosoma no está correctamente unido, el freno bloquea la progresión, impidiendo la separación hasta que se corrigen los errores. Varias enzimas llamadas quinasas mitóticas, incluidas MPS1, Aurora B y BUB1, ayudan a detectar uniones defectuosas y a promover la “corrección de errores” para que cada célula hija reciba el juego correcto de cromosomas. La alteración de este sistema puede tanto alimentar el desarrollo del cáncer como crear debilidades especiales que ciertos fármacos pueden explotar.
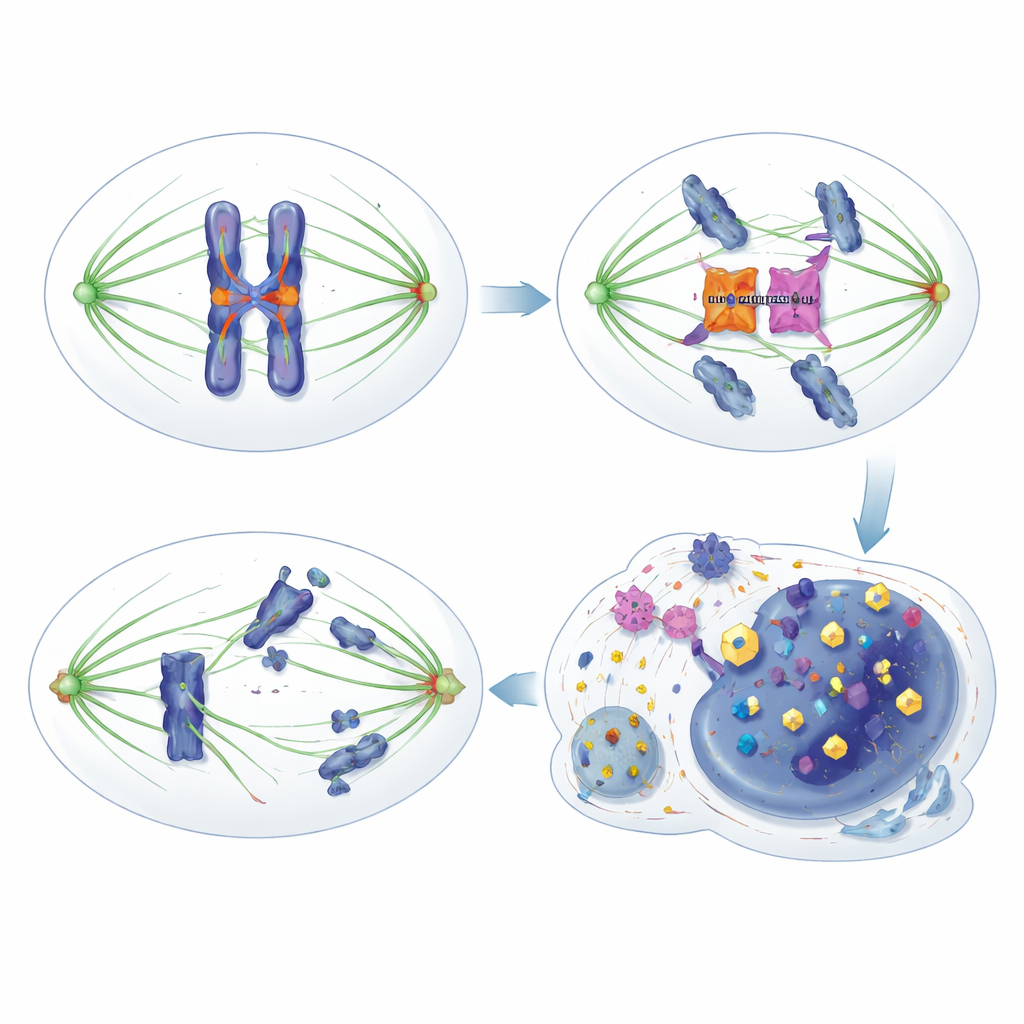
HORMAD1 debilita discretamente el freno
Los investigadores descubrieron que HORMAD1 socava este freno de seguridad de una forma sutil pero importante. En lugar de interferir con componentes clásicos del punto de control como la proteína HORMA MAD2L1, HORMAD1 se une directamente a la quinasa Aurora B. Aurora B normalmente se asocia con otra proteína, INCENP, para activarse completamente y modificar proteínas en centrómeros y cinetocoros—sitios críticos en los cromosomas donde se adhieren las fibras del huso. Cuando HORMAD1 está presente en células tumorales en división, compite con INCENP por el acceso a Aurora B, reduciendo su asociación y atenuando la actividad de Aurora B. Como resultado, las señales habituales de fosforilación de Aurora B en varios dianas se debilitan, la corrección de errores es menos eficaz y el punto de control se vuelve “poroso”: las células salen de la mitosis demasiado pronto, incluso cuando las uniones son defectuosas, lo que conduce a una mala segregación cromosómica e inestabilidad genómica.
De la debilidad a la oportunidad terapéutica
Dado que HORMAD1 solo desactiva parcialmente a Aurora B y a las salvaguardas relacionadas, las células cancerosas permanecen lo bastante viables para crecer, pero dependen en gran medida de la función restante de las quinasas mitóticas para sobrevivir a divisiones defectuosas repetidas. El equipo probó esto exponiendo células positivas y negativas para HORMAD1 a inhibidores experimentales de MPS1, Aurora B y BUB1. En múltiples modelos, la expresión de HORMAD1 hizo a las células mucho más sensibles a estos fármacos, reduciendo drásticamente su capacidad de proliferar o formar colonias. La depleción genética de BUB1 fue especialmente letal únicamente en presencia de HORMAD1, revelando una dependencia selectiva y fuerte. En modelos de ratón con tumores de mama triple negativos derivados de pacientes, aquellos con altos niveles de HORMAD1 se redujeron o crecieron más lentamente al tratarse con una formulación nanoparticulada de un inhibidor de Aurora B, mientras que los tumores sin HORMAD1 resistieron en gran medida el mismo tratamiento.
Qué significa esto para los pacientes
Para un observador no experto, HORMAD1 actúa como una espada de doble filo en el cáncer: empuja a las células tumorales hacia un mayor desorden cromosómico, lo que puede impulsar la enfermedad, pero al hacerlo también las hace peligrosamente dependientes de unas pocas salvaguardas de la división celular que quedan. El estudio muestra que esta proteína de la fertilidad desplazada debilita un punto de control clave al desviar a Aurora B, dejando a los tumores positivos para HORMAD1 particularmente vulnerables a fármacos que apuntan a Aurora B, MPS1 o BUB1. Dado que HORMAD1 está en gran medida ausente en tejidos normales pero presente en un subconjunto claro de cánceres, podría servir como biomarcador para identificar a los pacientes con mayor probabilidad de beneficiarse de estos emergentes inhibidores de quinasas mitóticas, abriendo potencialmente nuevas vías de tratamiento dirigidas para cánceres difíciles de tratar como el cáncer de mama triple negativo.
Cita: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Palabras clave: HORMAD1, cáncer de mama triple negativo, inestabilidad cromosómica, quinasa Aurora B, inhibidores del punto de control mitótico