Clear Sky Science · es
Polímeros proteomiméticos heterobifuncionales para la degradación dirigida de MYC y KRAS
Nuevas herramientas para tumbar las proteínas más difíciles del cáncer
Muchas de las proteínas que impulsan el cáncer y son más peligrosas, como MYC y KRAS, llevan tiempo calificadas como “no diana” porque los medicamentos no pueden adherirse a ellas con facilidad. Este estudio revela un nuevo tipo de material sintético blando, denominado polímeros HYDRAC, que puede atrapar estas proteínas resbaladizas y enviarlas al sistema de eliminación de la célula. Para los lectores, este trabajo ofrece una ventana sobre cómo la química y la nanotecnología podrían abrir opciones terapéuticas para cánceres que han resistido los fármacos tradicionales.
Un andamiaje flexible en lugar de una sola pastilla
La mayoría de los fármacos dirigidos contra el cáncer son moléculas pequeñas que encajan en cavidades de la superficie de una proteína, como una llave en una cerradura. Pero proteínas como MYC son flexibles y carecen de buenos bolsillos, mientras que KRAS suele mutar de formas que frustran los fármacos clásicos. Los autores diseñaron en su lugar polímeros largos, en forma de cadenas, formados por unidades repetidas. A lo largo de estas cadenas incorporaron dos tipos de componentes: fragmentos cortos que se unen a proteínas y reconocen un objetivo como MYC o RAS, y segmentos “degrón” que reclutan la maquinaria de eliminación de la célula. Puesto que muchas copias de cada componente decoran la misma cadena, una sola molécula HYDRAC puede alcanzar múltiples proteínas y enzimas a la vez, algo difícil de lograr con una única molécula fármaco rígida.
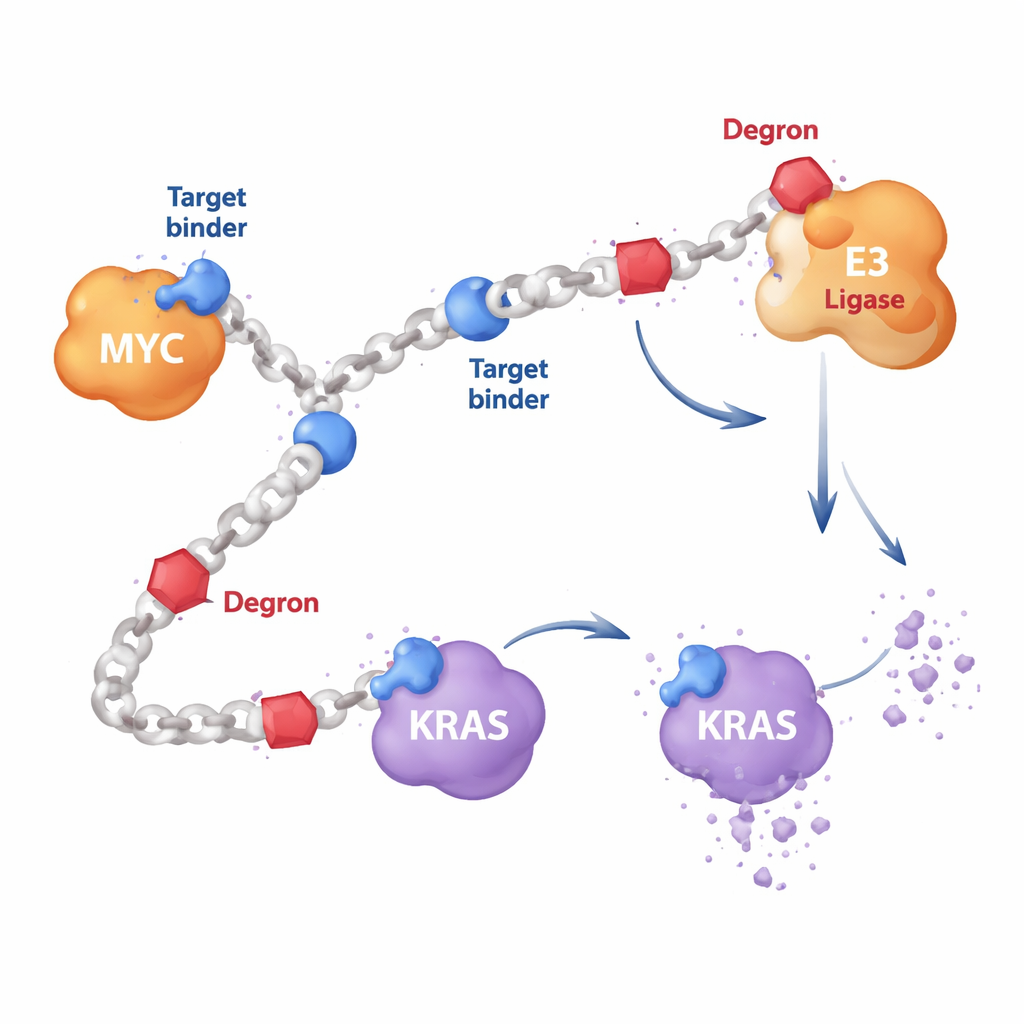
Enseñar a las células a destruir MYC
Como primera prueba, los investigadores se centraron en MYC, un interruptor maestro que impulsa el crecimiento en muchos cánceres pero que ha resistido el ataque directo durante décadas. Construyeron polímeros HYDRAC que muestran un péptido conocido por unirse a MYC junto con un motivo degrón simple que marca proteínas para su destrucción por el proteasoma celular, su principal trituradora de proteínas. En experimentos in vitro, estos polímeros se plegaron en formas compactas, semejantes a proteínas, y se unieron con alta afinidad a MYC pero no a proteínas no relacionadas. En células cancerosas, los HYDRAC entraron con facilidad, alteraron los programas génicos controlados por MYC y desencadenaron la muerte celular, efectos que dependieron de que las partes de reconocimiento y el degrón estuvieran presentes en la misma cadena polimérica.
De cultivos celulares a la reducción de tumores
Dentro de las células, el tratamiento con HYDRAC provocó una caída pronunciada en los niveles de proteína MYC sin reducir el ARN de MYC, lo que indica destrucción real en lugar de un simple apagado. Bloquear el proteasoma o enzimas clave que activan ciertas vías de degradación rescató los niveles de MYC, mostrando que los polímeros actúan redirigiendo los sistemas de eliminación de la célula. Los análisis a nivel proteómico revelaron que muy pocas otras proteínas se vieron afectadas, lo que sugiere una selectividad notable. En modelos de ratón con tumores impulsados por MYC, los HYDRAC marcados con fluorescencia se acumularon preferentemente en los tumores tras la inyección y permanecieron allí durante días. Dosis repetidas ralentizaron el crecimiento tumoral sin pérdida de peso importante ni daños tisulares evidentes, y las muestras tumorales mostraron menos células en división y más señales de muerte celular programada.
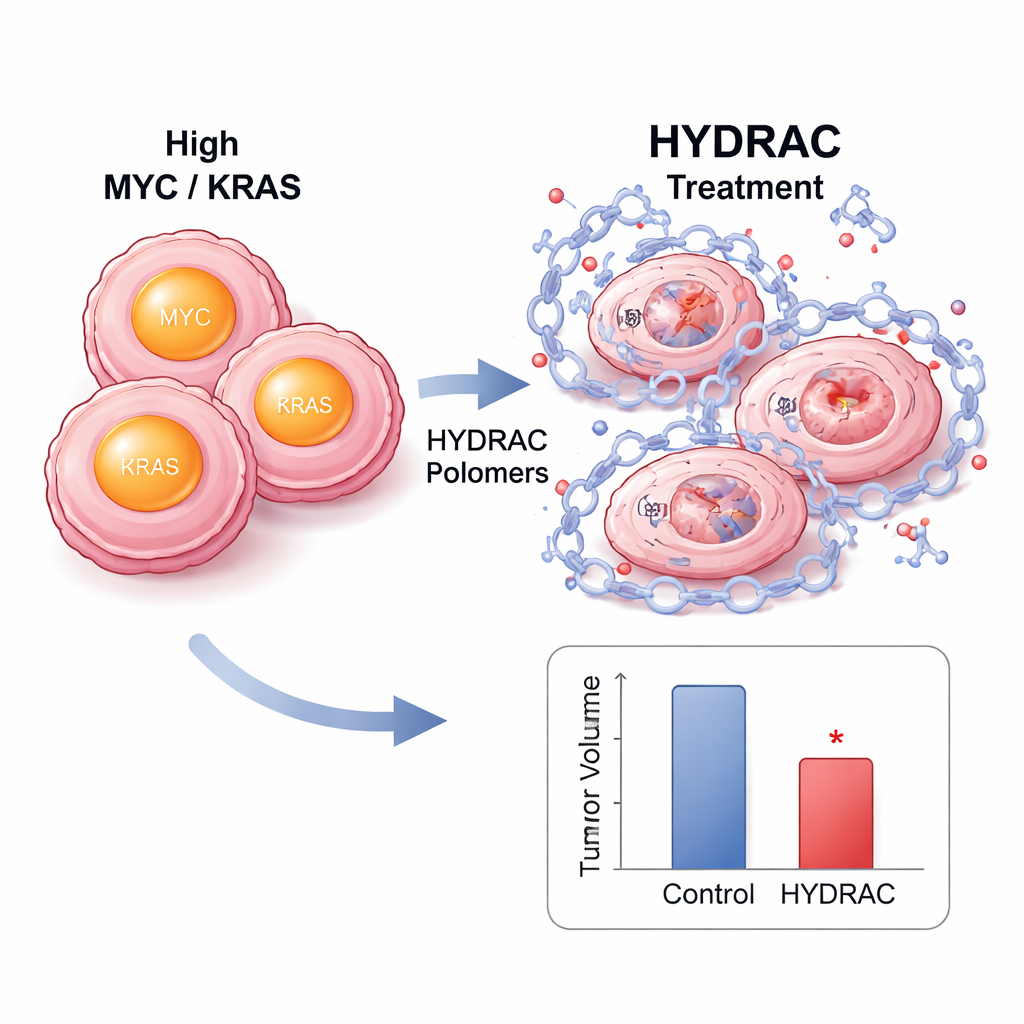
Una plataforma enchufable para muchos blancos de enfermedad
Una de las fortalezas del enfoque HYDRAC es que sus grupos laterales se pueden intercambiar como piezas modulares. El equipo sustituyó el degrón original por otros elementos que reclutan distintas enzimas celulares, incluidas las que reconocen el fármaco talidomida. Cada versión degradó MYC solo cuando la enzima prevista estaba presente y funcional, lo que confirma que los polímeros pueden ajustarse para usar rutas celulares distintas. Para probar la generalidad, los investigadores construyeron luego HYDRACs dirigidos a RAS usando un péptido que reconoce las proteínas RAS. Estos constructos degradaron con éxito KRAS mutante en dos líneas celulares cancerosas distintas, apuntando a un potencial “pan-KRAS” que no depende de una mutación concreta, un paso importante para cánceres donde coexisten muchas variantes de KRAS.
Por qué esto importa para el futuro del tratamiento del cáncer
Este trabajo presenta los HYDRACs como una nueva clase de materiales programables que no solo bloquean proteínas problemáticas, sino que ayudan a las células a borrarlas. Al combinar muchas unidades de reconocimiento y degradación en un polímero flexible, los HYDRACs sortean los límites de diseño de fármacos pequeños tradicionales y de los PROTAC, que normalmente solo pueden llevar una de cada una. Aunque queda mucho por hacer antes de que estos materiales lleguen a la clínica, los resultados en modelos impulsados por MYC y KRAS sugieren que proteínas cancerígenas consideradas durante mucho tiempo “no diana” pueden, de hecho, ser vulnerables cuando la medicina se parece más a un cepillo molecular a medida que a una única pastilla pequeña.
Cita: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Palabras clave: degradación proteica dirigida, MYC, KRAS, terapéuticas basadas en polímeros, nanomedicina contra el cáncer