Clear Sky Science · es
Paisaje epigenómico integrador de cerebros con enfermedad de Alzheimer revela alteraciones moleculares en oligodendrocitos asociadas con tau
Por qué importa esta investigación cerebral
La enfermedad de Alzheimer es más conocida por la pérdida de memoria y la acumulación de dos proteínas problemáticas en el cerebro: amiloide y tau. Sin embargo, las personas con Alzheimer pueden presentar patrones de daño muy distintos, incluso con el mismo diagnóstico. Este estudio plantea una pregunta clave: ¿qué interruptores dentro de las células cerebrales ayudan a determinar cuánto se acumulan estas proteínas dañinas y cómo afectan a distintos tipos celulares? Al examinar marcas químicas en el ADN de cientos de cerebros, los investigadores descubren un vínculo sorprendente entre la tau y las células que permiten funcionar el cableado cerebral.
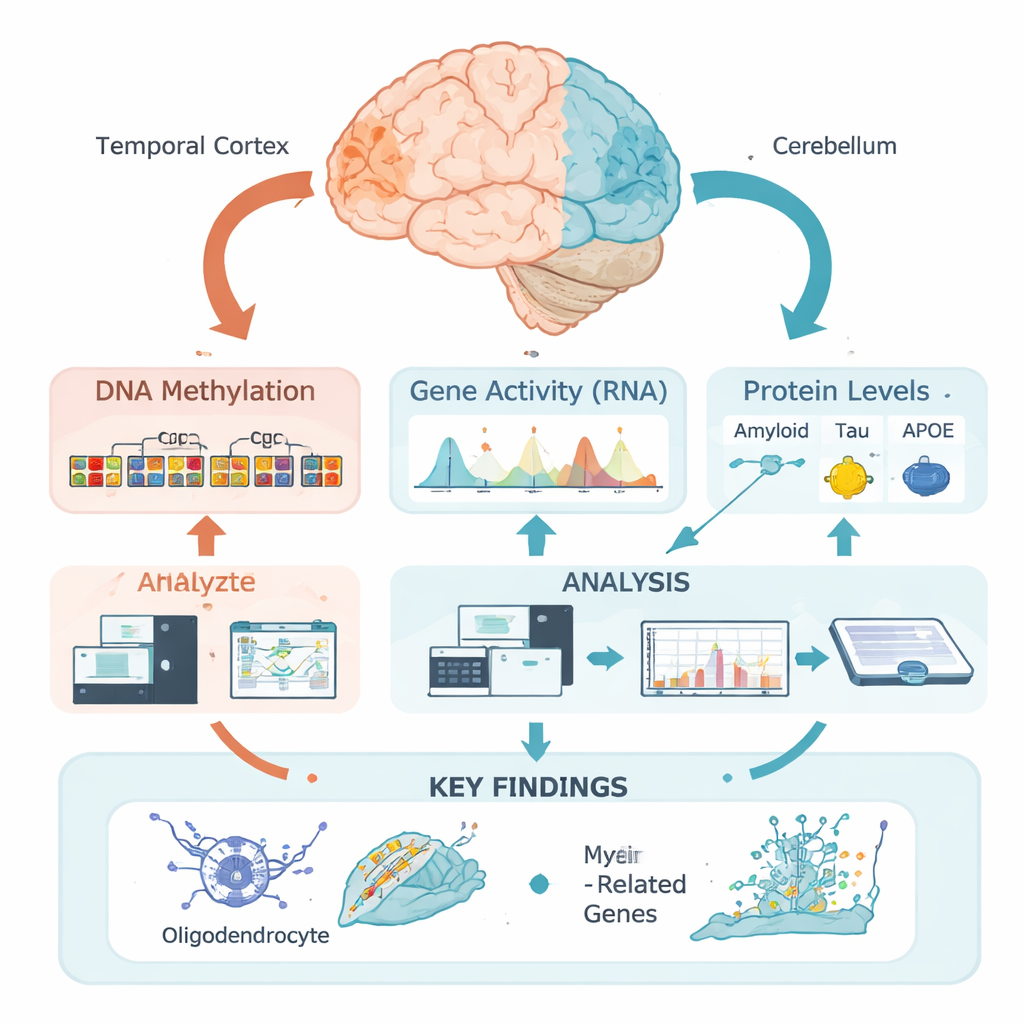
Marcas químicas en el ADN como interruptores ocultos
Nuestro ADN contiene las instrucciones básicas para construir y mantener las células cerebrales, pero esas instrucciones se regulan mediante marcas epigenéticas: etiquetas químicas que pueden aumentar o disminuir la actividad de genes cercanos sin cambiar el código genético. Una de las etiquetas más importantes es la metilación del ADN, en la que pequeños grupos químicos se unen a sitios específicos del ADN. En lugar de examinar sitios aislados, este equipo usó un enfoque “regional” nuevo: agruparon muchos sitios cercanos en zonas funcionales según cómo está empaquetado el ADN en la corteza temporal, una región muy afectada en Alzheimer, y en el cerebelo, que queda relativamente preservado. Esto les permitió preguntar dónde, en un sentido biológico, cambian los patrones de metilación en relación con las características de la enfermedad.
Conectando las marcas del ADN con las proteínas del Alzheimer
Los investigadores analizaron tejido cerebral de 472 personas con Alzheimer confirmado tras la muerte. Para cada muestra de corteza temporal midieron niveles detallados de amiloide, tau y proteínas APOE en distintas formas bioquímicas, además de las puntuaciones microscópicas clásicas de placas amiloides y ovillos de tau. Luego realizaron estudios de asociación epigenómica a gran escala, probando si los niveles regionales de metilación del ADN se correlacionaban con estas mediciones. De manera llamativa, casi todas las asociaciones fuertes que encontraron estaban relacionadas no con el amiloide, sino con la tau—especialmente con la tau soluble total y una forma fosforilada (modificada químicamente) ligada a la membrana que se cree que es particularmente tóxica.
Una señal fuerte en las células del cableado cerebral
Muchas de las regiones de ADN vinculadas a la tau se ubicaban en partes “activas” del genoma que influyen en genes vecinos. Al combinar los datos de metilación con mediciones de actividad génica de los mismos cerebros, el equipo mostró que estas regiones con frecuencia regulaban genes usados por los oligodendrocitos—las células que envuelven las fibras nerviosas con mielina, permitiendo que las señales eléctricas viajen de forma rápida y fiable. Genes clave relacionados con la mielina, como MBP, MAG y MYRF, junto con el gen de riesgo de Alzheimer BIN1 y un gen candidato más reciente llamado LDB3, aparecieron en este conjunto. Niveles más altos de tau fosforilada tóxica tendían a coincidir con mayor metilación en estas regiones y menor expresión de los genes asociados con oligodendrocitos y mielina, mientras que el conjunto más benigno de tau soluble total mostraba el patrón opuesto.
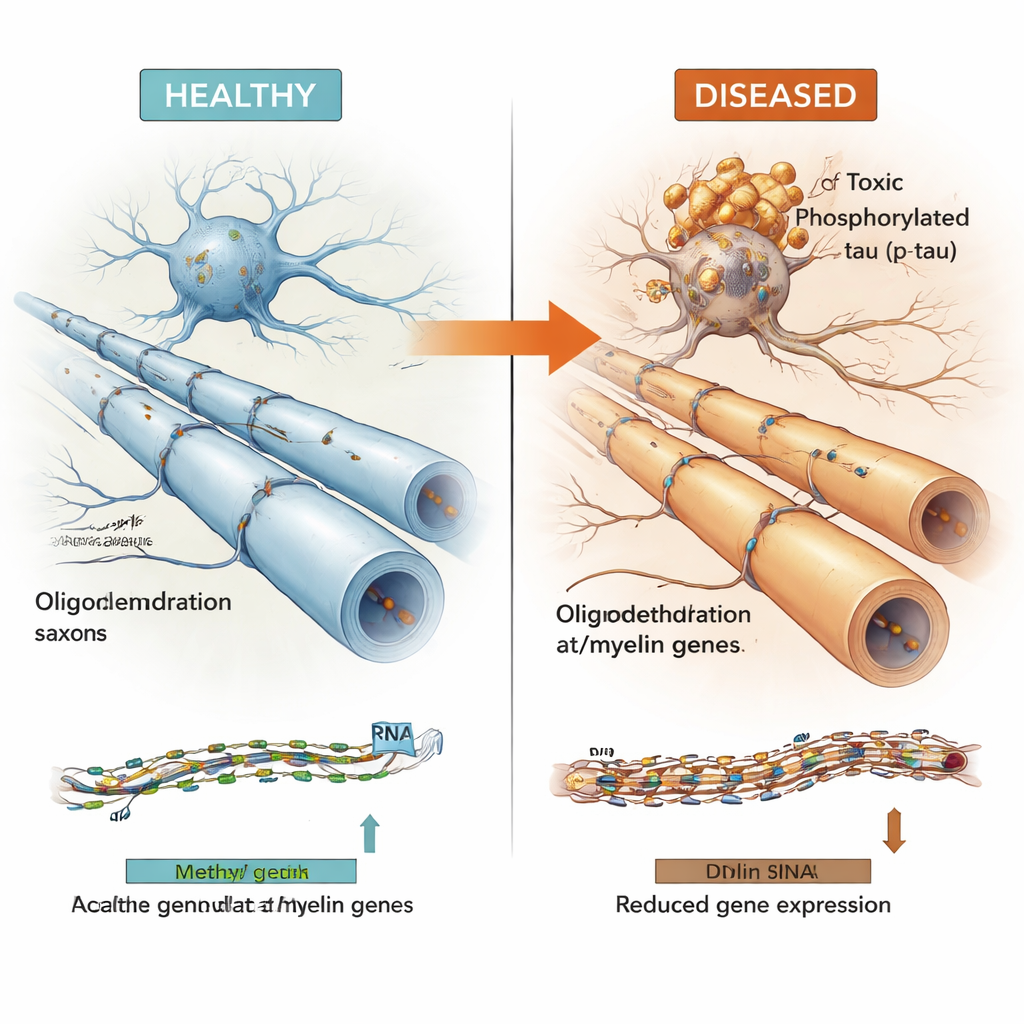
Un patrón observado en múltiples enfermedades cerebrales
Para comprobar si estos hallazgos eran sólidos y generales, los autores examinaron grandes conjuntos de datos independientes de otras colecciones de cerebros con Alzheimer y de cerebros afectados por tauopatías primarias como la parálisis supranuclear progresiva y la enfermedad de Pick. Aunque estas cohortes se midieron con distintas tecnologías y a menudo en regiones cerebrales diferentes, muchas de las mismas regiones de ADN y genes de oligodendrocitos mostraron un comportamiento coherente: sus niveles de metilación se relacionaban con la carga de ovillos de tau, y su expresión se reducía en cerebros enfermos y en estudios de una sola célula centrados específicamente en oligodendrocitos. Es importante que estos patrones no parecían explicarse simplemente por la genética o por la pérdida global de células, lo que sugiere un cambio epigenético genuino en la función de los oligodendrocitos.
Qué significa esto para comprender el Alzheimer
En conjunto, los resultados apoyan un modelo en el que el incremento de niveles de tau dañina está estrechamente vinculado a cambios epigenéticos en oligodendrocitos que reprimen genes relacionados con la mielina, lo que podría debilitar el cableado cerebral y contribuir al deterioro cognitivo. Aún no está claro qué ocurre primero—la acumulación de tau o la alteración de estos genes de mielina—pero las asociaciones sólidas y repetidas a lo largo de miles de muestras y varias enfermedades señalan un mecanismo compartido. Al mapear estos interruptores del ADN e integrarlos en un “Atlas Multiómico” público, este trabajo pone de relieve a los oligodendrocitos y su regulación epigenética como objetivos prometedores para futuras terapias destinadas a estabilizar los circuitos cerebrales, en vez de centrarse únicamente en las neuronas o las placas amiloides.
Cita: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Palabras clave: enfermedad de Alzheimer, proteína tau, metilación del ADN, oligodendrocitos, mielina