Clear Sky Science · es
Base estructural de la señalización y modulación del canal activado por zinc humano (ZAC)
Cómo un metal traza ayuda a las neuronas a comunicarse
El zinc es más conocido como nutriente en los comprimidos multivitamínicos, pero en el interior del cuerpo este metal también actúa como un mensajero químico rápido en el cerebro. El estudio descrito aquí revela, a resolución atómica, cómo una proteína poco conocida llamada canal activado por zinc (ZAC) detecta el zinc fuera de las células y convierte esa señal en una respuesta eléctrica. Comprender esta puerta especial en la membrana celular podría aclarar cómo el zinc moldea la actividad cerebral y sugerir nuevas formas de ajustar las señales nerviosas en la salud y la enfermedad.
Una puerta especial para las señales de zinc
Muchos mensajes rápidos entre neuronas son transmitidos por químicos familiares como la serotonina o la acetilcolina, que abren canales en forma de anillo en la membrana celular. ZAC es un pariente lejano de estos receptores, pero en lugar de responder a una molécula orgánica, se activa por iones metálicos como el zinc, el cobre y protones. ZAC está presente en muchos tejidos humanos, incluido el cerebro, aunque falta en animales de laboratorio habituales como ratones y ratas, lo que ha ralentizado el progreso. Este trabajo utiliza criomicroscopía electrónica de alta resolución para capturar varias instantáneas tridimensionales del ZAC humano: en su forma de reposo, con zinc unido y con dos fármacos diferentes que cierran el canal. En conjunto, estas estructuras muestran cómo el zinc se acopla en la parte superior del canal, cómo pasan los iones y cómo los bloqueadores cierran la puerta o la abren en un estado no conductor.
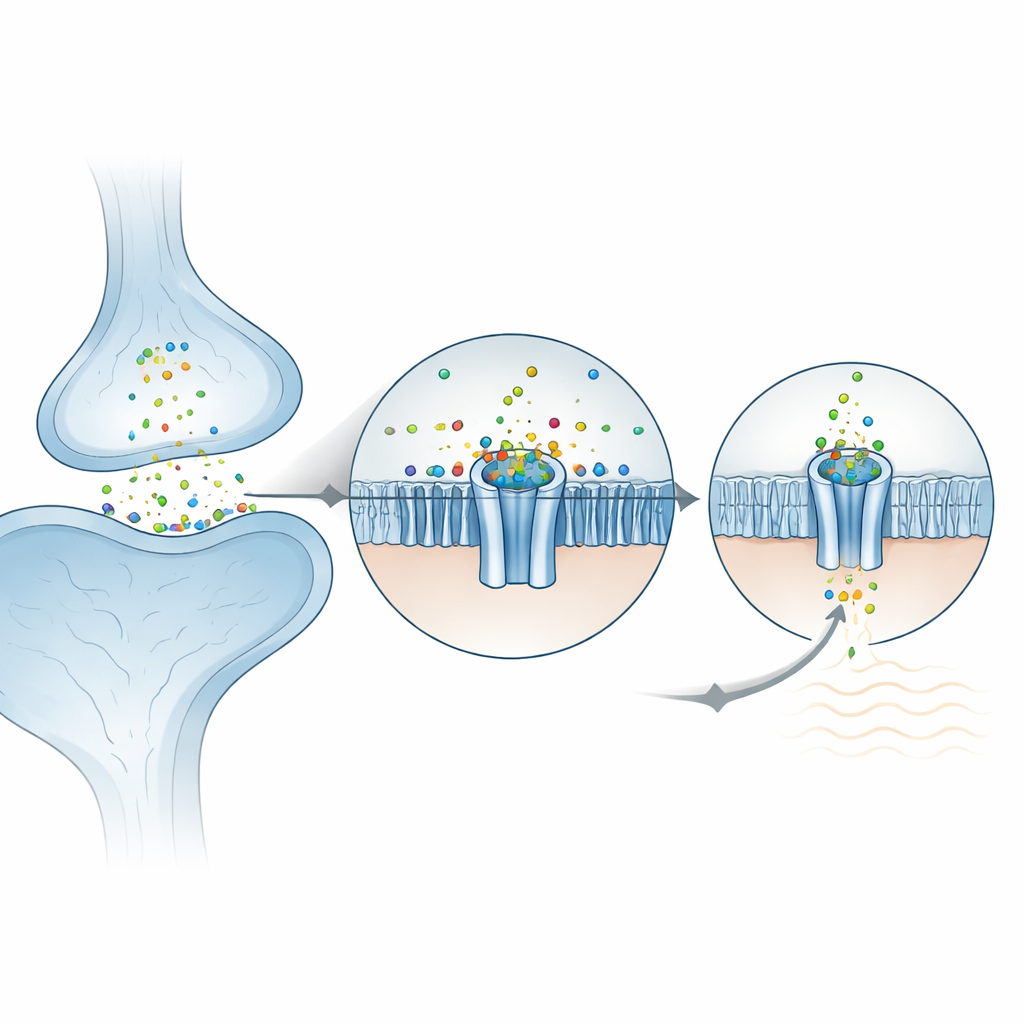
Cómo el zinc encaja en el canal
En la superficie exterior de la célula, ZAC está formado por cinco subunidades idénticas que conforman una roseta. Los investigadores encontraron que los iones de zinc se alojan en cinco bolsillos equivalentes, cada uno situado entre dos subunidades vecinas en el dominio externo. Sorprendentemente, el zinc no es retenido por los aminoácidos “agarradores” habituales que comúnmente unen metales (como histidina o cisteína). En cambio, queda sostenido principalmente por dos cadenas laterales aromáticas en forma de anillo que estabilizan el ion cargado positivamente mediante las llamadas interacciones catión–π. Cuando estos residuos clave se mutaron en ovocitos de rana usados para registros eléctricos, el canal dejó de responder al zinc, confirmando su papel central. El entorno circundante ya está preorganizado, lo que ayuda a explicar por qué ZAC muestra una actividad espontánea notable incluso sin zinc: la proteína está cerca del punto de equilibrio entre cerrado y abierto y el zinc simplemente inclina la balanza.
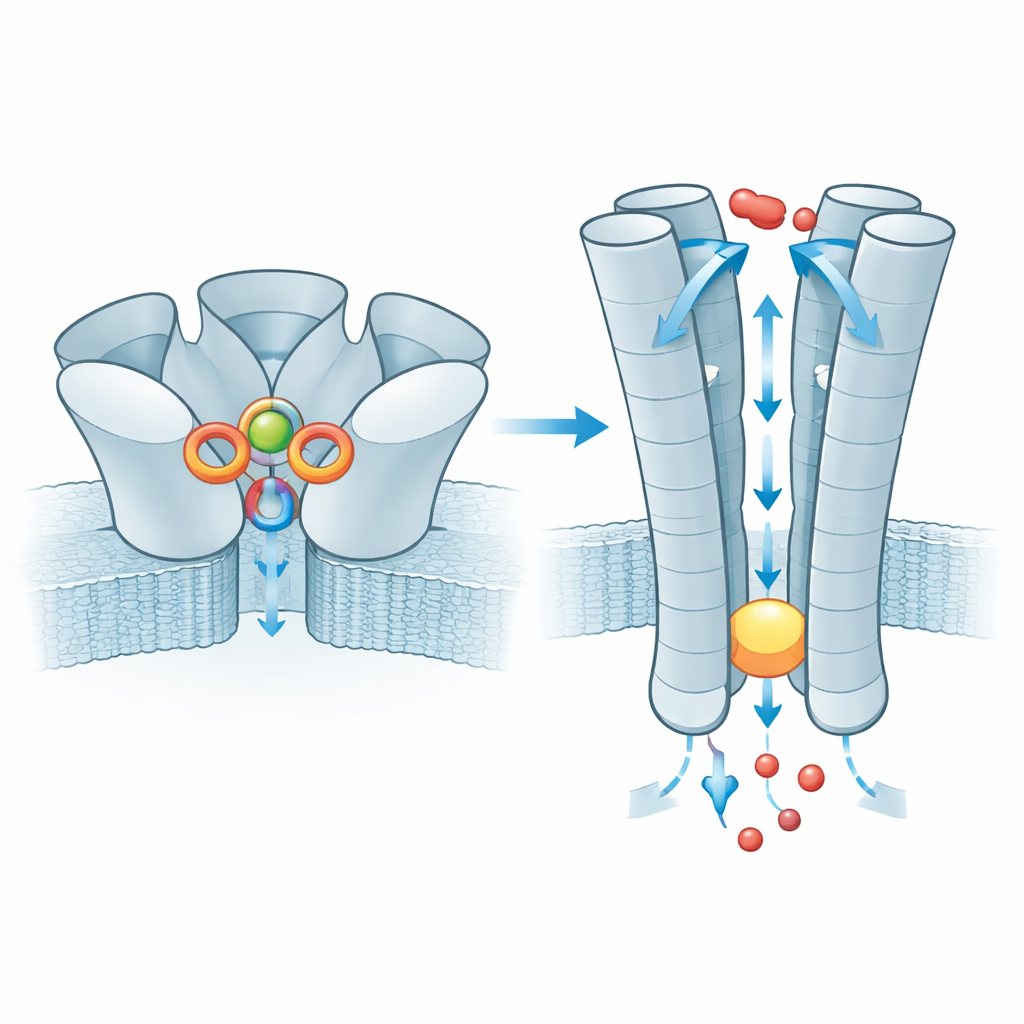
El camino para los iones y una variante genética común
Una vez que el zinc se ha unido, el efecto se transmite hacia la parte transmembrana de ZAC, donde cinco hélices interiores forman el poro. En el estado de reposo este tubo se estrecha en un anillo de residuos de leucina, creando un tapón hidrófobo que bloquea el movimiento iónico. Con el zinc unido, el tapón se ensancha lo justo para permitir que iones positivos pequeños como sodio y potasio pasen, mientras que el revestimiento cargado del poro ayuda a seleccionar estos iones. El equipo también examinó una variante humana muy común de ZAC en la que un único aminoácido (treonina) es reemplazado por alanina en una corta hebra por encima del tapón. Este pequeño cambio debilita una red de interacciones entre subunidades vecinas que normalmente ayuda a transmitir la unión del zinc hacia la puerta, y las medidas eléctricas muestran que los canales construidos con esta variante conducen corrientes mucho menores. Por tanto, la variante actúa como un conversor de señal menos eficiente, aunque su impacto en la fisiología humana sigue siendo desconocido.
Cómo dos fármacos silencian el canal
Más allá del zinc, el estudio también explora cómo dos antagonistas, TTFB y d‑tubocurarina (d‑TC), apagan ZAC. TTFB es una pequeña molécula diseñada a medida que resulta alojarse profundamente en la región de la membrana, deslizándose entre dos de las hélices formadoras del poro justo por encima de la puerta. Allí interactúa con un ajustado bolsillo hidrófobo y residuos polares cercanos, apuntalando efectivamente las hélices para que no puedan moverse hacia un estado totalmente abierto y conductor. d‑TC, un fármaco más antiguo usado como relajante muscular, actúa de forma más amplia. Una molécula de d‑TC se une en el mismo bolsillo externo que normalmente aloja al zinc, imitando la carga positiva del zinc pero bloqueando que el zinc real se una correctamente. Una segunda molécula de d‑TC se sitúa en la entrada del propio poro, taponando físicamente el túnel. En conjunto, estos enlaces atrapan a ZAC en una conformación desensibilizada y no conductora mientras la forma de la proteína permanece relativamente abierta.
Qué significan los hallazgos para el zinc y la salud
Este trabajo estructural muestra con detalle molecular claro que ZAC es un sensor genuino de zinc, usando una inusual cuna aromática para detectar el metal en el mismo tipo de sitio donde otros miembros de la familia unen neurotransmisores. También identifica redes de interacción específicas que ajustan la facilidad con la que el canal se abre y se cierra, y mapea dos sitios distintos de unión a fármacos que pueden o bien calzar la puerta cerrada o obstruir el poro. Para el público no especializado, el mensaje clave es que el zinc no es solo un nutriente estático sino una señal activa, y ZAC es uno de sus receptores dedicados. Mientras los científicos buscan los papeles de ZAC en el cuerpo humano y en trastornos neurológicos vinculados al desequilibrio de zinc, estos planos a nivel atómico proporcionan una hoja de ruta para diseñar moléculas más precisas que modulen este canal y, potencialmente, corrijan la señalización del zinc alterada.
Cita: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Palabras clave: señalización por zinc, canales iónicos activados por ligando, neurociencia, estructura por criomicroscopía electrónica, modulación del canal