Clear Sky Science · es
El receptor del complemento 5a 2 atenúa la enfermedad renal diabética al promover la formación de membrana asociada a mitocondrias y retículo endoplásmico mediada por la interacción PSS‑MFN2
Por qué importa esta investigación renal
La enfermedad renal diabética es una de las razones más comunes por las que las personas con diabetes terminan necesitando diálisis o un trasplante, y los tratamientos actuales mayormente ralentizan, en lugar de detener, el daño. Este estudio descubre un sistema de defensa natural inesperado dentro de las células renales que las ayuda a lidiar con la mezcla tóxica de alto azúcar y grasa en la diabetes. Al revelar cómo un receptor inmunitario poco conocido, C5aR2, protege las fábricas de energía y el manejo de lípidos de las células renales, el trabajo apunta a un tipo nuevo de fármaco que podría proteger los riñones sin bloquear el sistema inmunitario.
Un guardián sorprendente en el riñón diabético
Los investigadores se centraron en la enfermedad renal diabética, en la que pequeñas estructuras del riñón se cicatrizan y dejan de funcionar gradualmente tras la exposición prolongada a la hiperglucemia y al metabolismo alterado. Examinaron biopsias renales de pacientes y encontraron que un receptor llamado C5aR2 estaba muy aumentado en el tejido entre los filtros renales, especialmente en las células tubulares proximales que reabsorben nutrientes. Niveles más altos de C5aR2 se asociaron con una enfermedad más grave y una mayor probabilidad de progresar a insuficiencia renal, lo que sugiere que el receptor se activa más a medida que el daño se acumula. Curiosamente, trabajos previos habían enmarcado a C5aR2 principalmente como un receptor inmunitario “señuelo”; este artículo muestra que también tiene un papel importante en el metabolismo celular.
Cuando falta el defensor, el daño se acelera
Para comprobar si C5aR2 es aliado o adversario, el equipo usó ratones diabéticos que carecían del gen C5ar2. En comparación con ratones diabéticos que mantenían el receptor, estos animales knockout desarrollaron mayor pérdida de proteína en la orina, más cicatrización e inflamación en el tejido renal y más daño estructural visible al microscopio. Sus células tubulares estaban obstruidas con gotas de grasa, mostraban marcados signos de estrés en el retículo endoplásmico (la estación de plegado y empaquetado celular) y tenían mitocondrias hinchadas y con funcionamiento deficiente. Problemas similares aparecieron en células renales cultivadas cuando se silenció C5aR2, incluida una reducción del consumo de oxígeno, una medida directa del rendimiento mitocondrial. En conjunto, estos hallazgos indican que C5aR2 normalmente ayuda a las células tubulares a soportar el estrés metabólico de la diabetes.
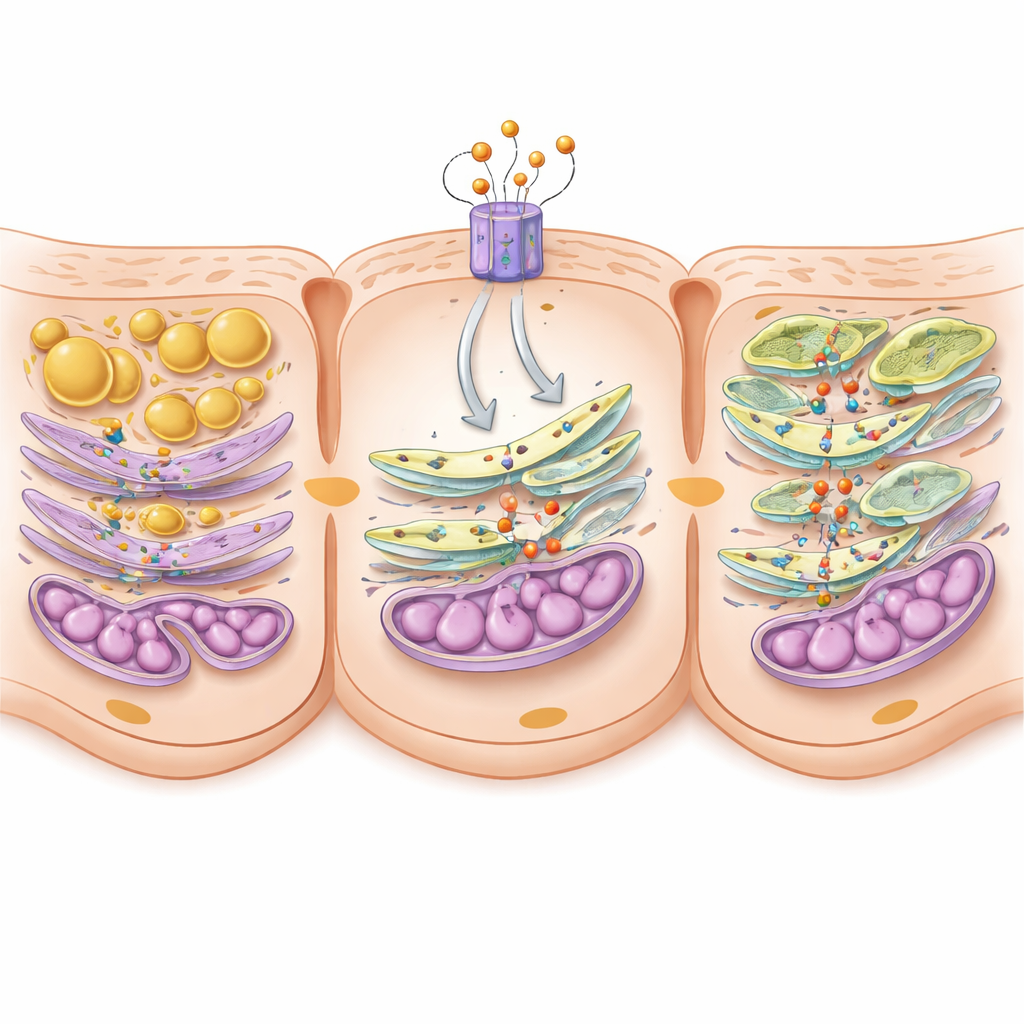
Cómo sitios de contacto diminutos y un ingrediente lipídico clave mantienen las células saludables
Al profundizar, los científicos perfilizaron lípidos en los riñones y encontraron que los ratones sin C5aR2 presentaban una pérdida marcada de fosfatidilserina, un bloque de construcción crucial de las membranas celulares, mientras que las grasas de almacenamiento neutras aumentaban. La fosfatidilserina se sintetiza principalmente en uniones especializadas donde el retículo endoplásmico y las mitocondrias se tocan, llamadas membranas asociadas a mitocondrias. En estas uniones, las enzimas denominadas PSS1 y PSS2 sintetizan fosfatidilserina, y una proteína ancladora llamada MFN2 ayuda a transferirla a las mitocondrias. En los ratones diabéticos, estas zonas de contacto ya estaban acortadas; eliminar C5aR2 las hizo encoger aún más, y la cantidad de PSS1, PSS2 y MFN2 en las uniones disminuyó. En células, la actividad de C5aR2 resultó en el aumento de un factor de transcripción, c‑FOS, que a su vez incrementó la producción de las enzimas PSS. El equipo mostró además que las proteínas PSS se unen físicamente a MFN2 para formar un puente funcional que sostiene tanto la formación de contactos como la transferencia lipídica.
Restaurar el eslabón perdido para rescatar células estresadas
Para demostrar que este puente molecular realmente importa, los autores aumentaron artificialmente los niveles de PSS2 solo en las células tubulares renales de ratones diabéticos. A pesar de la diabetes persistente, estos animales tuvieron menos proteína en la orina, menos cicatrización, menos gotas de grasa, mejor forma y función mitocondrial y zonas de contacto más largas entre mitocondrias y retículo endoplásmico. Los niveles de fosfatidilserina en estas uniones también se recuperaron. En experimentos celulares, el aumento de PSS2 restauró la producción de energía y redujo la acumulación de grasa incluso cuando C5aR2 estaba suprimido, confirmando que PSS2 ocupa un punto crítico en esta vía protectora.
Una nueva estrategia farmacológica que modula, en lugar de bloquear, el complemento
Puesto que bloquear por completo la señalización del complemento puede perjudicar la defensa del huésped, los investigadores exploraron una táctica más selectiva: activar C5aR2 con un pequeño péptido diseñado llamado P59. En ratones diabéticos db/db, P59 administrado por vía subcutánea durante 10 semanas redujo el peso corporal y los triglicéridos sanguíneos, disminuyó la pérdida de proteína en orina y mejoró notablemente el daño tubulointersticial. Los riñones de los animales tratados mostraron menos gotas lipídicas, menos estrés del retículo endoplásmico, mitocondrias más saludables y membranas asociadas a mitocondrias más robustas, enriquecidas con PSS1, PSS2, MFN2 y fosfatidilserina. El análisis de ARN unicelular reveló que P59 revivió específicamente la expresión de Pss2 en células del túbulo proximal lesionadas. En células renales en cultivo, los beneficios de P59 desaparecieron cuando se suprimieron C5aR2 o las enzimas PSS, lo que demuestra que sus efectos protectores se transmiten a través de este recién cartografiado eje C5aR2–c‑FOS–PSS–MFN2.
Qué significa esto para las personas con diabetes
En términos cotidianos, este estudio sugiere que los riñones bajo estrés diabético intentan activar C5aR2 para mantener en orden sus sistemas energéticos y el manejo de lípidos. Cuando este receptor falta o se ve desbordado, los diminutos sitios de contacto entre compartimentos celulares se deshacen, un ingrediente membranario clave escasea y la grasa y las señales de estrés se acumulan, impulsando la cicatrización. Al estimular suavemente C5aR2 con un fármaco dirigido, puede ser posible reconstruir estos puentes de contacto, restaurar un equilibrio lipídico más saludable y proteger la función renal sin suprimir de forma general el sistema inmunitario. Aunque queda mucho por hacer antes de que tales tratamientos lleguen a la clínica, los hallazgos abren una vía prometedora para ralentizar o prevenir la insuficiencia renal en personas con diabetes.
Cita: Zhao, Yy., Wang, Yh., Li, Zh. et al. Complement 5a receptor 2 attenuates diabetic kidney disease by promoting mitochondria-associated endoplasmic reticulum membrane formation mediated by PSS-MFN2 interaction. Cell Discov 12, 24 (2026). https://doi.org/10.1038/s41421-026-00873-w
Palabras clave: enfermedad renal diabética, membranas asociadas a mitocondrias, metabolismo de lípidos, receptor del complemento C5aR2, células tubulares proximales