Clear Sky Science · es
La palmitoilación de ASCT2 regulada por el eje JNK1-ZDHHC14 orquesta el metabolismo de la glutamina y la progresión del NSCLC
Avivando el fuego del cáncer de pulmón
Muchos cánceres de pulmón de crecimiento rápido son adictos a la glutamina, un aminoácido común que actúa como combustible y bloque de construcción clave. Este estudio revela cómo las células tumorales ajustan con precisión una importante “puerta” de entrada de glutamina en su superficie y cómo interrumpir este sistema de control podría frenar el crecimiento del cáncer. Entender esta válvula oculta de combustible ayuda a explicar por qué algunos tumores son tan difíciles de privar de nutrientes y apunta a nuevas combinaciones de fármacos que podrían cortar su suministro de energía de manera más efectiva.
Una puerta celular para la glutamina
La glutamina entra en las células principalmente a través de una proteína transportadora llamada ASCT2, que se sitúa en la membrana externa y traslada glutamina hacia el interior. El cáncer de pulmón no microcítico (NSCLC), la forma más común de cáncer de pulmón, a menudo depende en gran medida de la glutamina para sostener la rápida división y supervivencia. Los altos niveles de ASCT2 en los tumores se asocian con enfermedad agresiva y peores resultados en los pacientes. Sin embargo, ASCT2 se sintetiza, modifica y degrada constantemente, lo que plantea la pregunta: ¿qué decide cuánto de este guardián permanece en la superficie celular en cada momento?
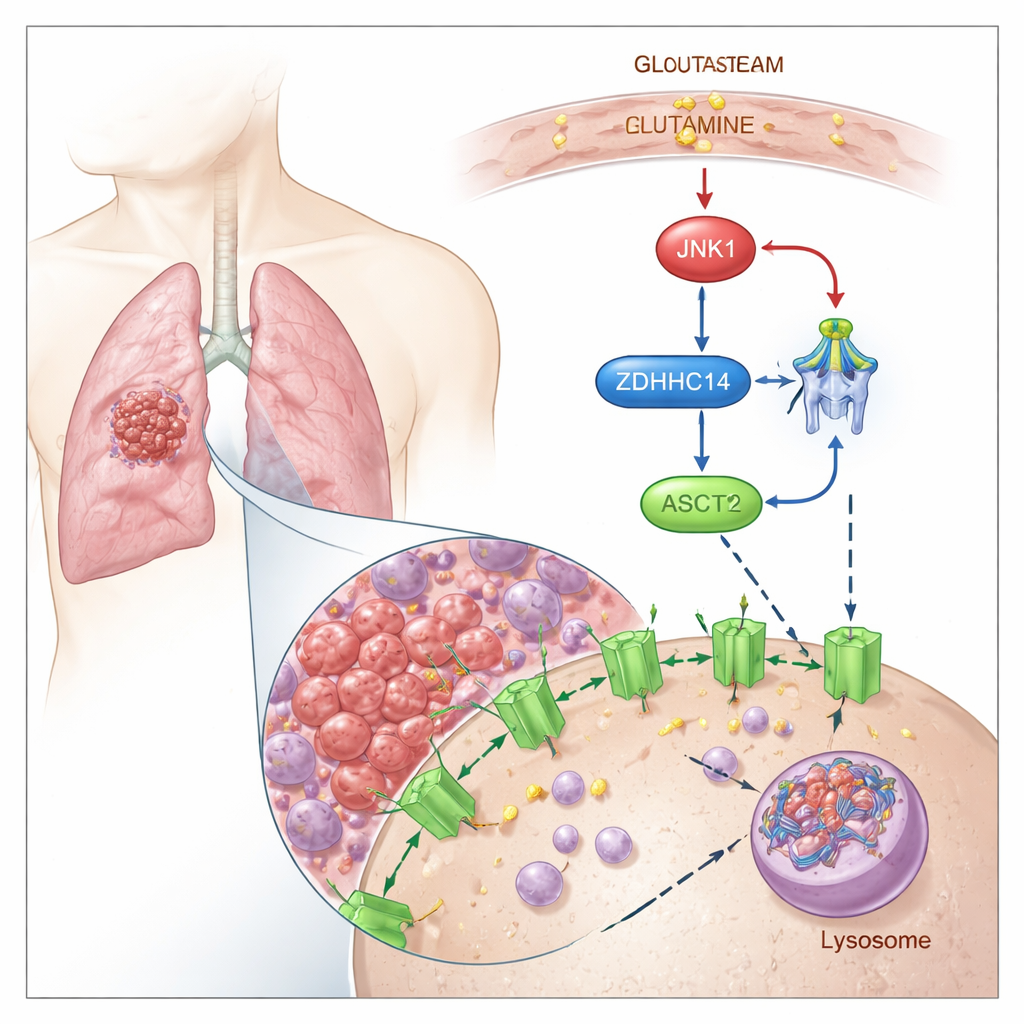
Etiquetando ASCT2 para su degradación
Los investigadores demuestran que ASCT2 está controlado por una “etiqueta” química llamada palmitoilación, en la que un ácido graso se une a aminoácidos cisteína específicos de la proteína. Encuentran que una enzima denominada ZDHHC14 añade esta etiqueta lipídica en dos sitios conservados de ASCT2 (Cys39 y Cys48). Una vez etiquetado, ASCT2 es redirigido desde la superficie celular hacia centros de reciclaje celular llamados lisosomas, donde se degrada. Bloquear la palmitoilación impide que ASCT2 sea etiquetado y degradado, lo que conduce a niveles más altos de la proteína ASCT2 y a un aumento de la captación de glutamina, sin alterar la actividad génica subyacente.
Una contraenzima que protege la puerta
En oposición a ZDHHC14 actúa otra enzima, ABHD17B, que elimina la etiqueta grasosa de ASCT2. Cuando ABHD17B está activa, ASCT2 está menos palmitoilada, es más estable y es más probable que sea reciclada de nuevo a la superficie celular en lugar de ser enviada al lisosoma. Este vaivén de etiquetado y des-etiquetado funciona como un dial finamente ajustado del flujo de glutamina: ZDHHC14 empuja a ASCT2 hacia la destrucción, mientras que ABHD17B la rescata y mantiene el transporte de glutamina. En células de cáncer de pulmón, desplazar este equilibrio hacia menos palmitoilación aumenta la captación de glutamina y favorece el crecimiento tumoral en cultivos y en ratones.
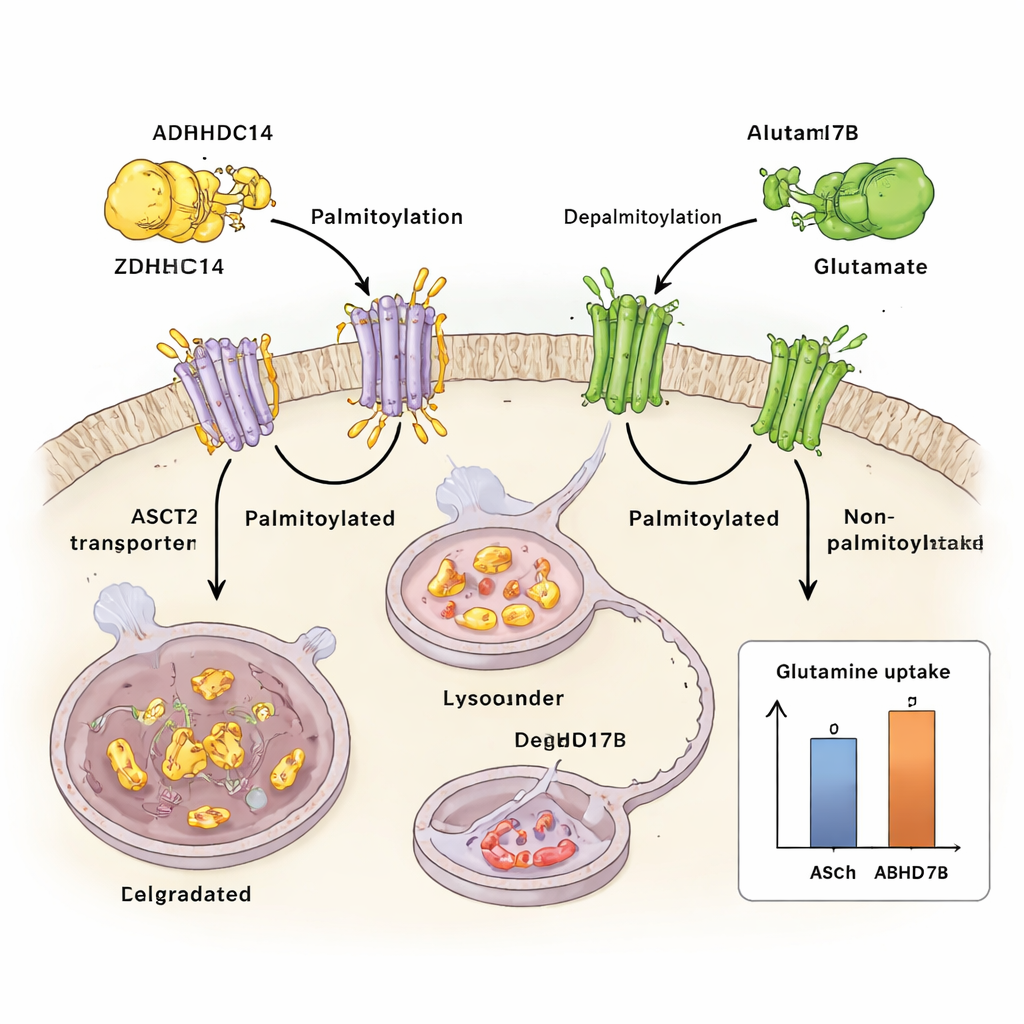
Cómo el estrés por nutrientes reconfigura el sistema
El equipo examinó luego qué ocurre cuando las células tumorales se quedan sin glutamina. Bajo privación de glutamina, una proteína de señalización sensible al estrés llamada JNK1 se activa. JNK1 se une físicamente a ZDHHC14 y añade un grupo fosfato en un sitio específico (Thr440), marcando a ZDHHC14 para su propia degradación lisosomal. A medida que los niveles de ZDHHC14 disminuyen, ASCT2 recibe menos etiquetas de palmitoilación, evita la degradación y se acumula en la superficie celular, precisamente cuando la célula más necesita capturar la glutamina escasa. Mutar este único sitio sensible a JNK1 estabiliza ZDHHC14, restaura el etiquetado de ASCT2 y reduce la captación de glutamina, lo que subraya cuán estrechamente está conectado el estrés por nutrientes a este circuito de control.
Trasladar el mecanismo a la terapia
Dado que ASCT2 es tan importante para el metabolismo tumoral, se están explorando fármacos que lo bloquean, como el compuesto experimental V9302, como tratamientos contra el cáncer. Este estudio revela que la señalización JNK1 puede contrarrestar la destrucción de ASCT2, protegiendo eficazmente la puerta de la glutamina. En modelos celulares y murinos de NSCLC, combinar un inhibidor de JNK con V9302 redujo con mayor intensidad la captación de glutamina, el crecimiento de las células tumorales y el tamaño del tumor que cada fármaco por separado. Muestras de pacientes y conjuntos de datos públicos muestran además que la baja expresión de ZDHHC14 y la alta de ASCT2 son comunes en NSCLC y se asocian con peor supervivencia, lo que sugiere que este patrón molecular podría ayudar a identificar a los pacientes con más probabilidades de beneficiarse de atacar esta vía.
Qué significa esto para los pacientes
En términos cotidianos, este trabajo muestra que ciertos cánceres de pulmón controlan su combustible preferido ajustando una válvula molecular en su superficie. Un trío de actores—JNK1, ZDHHC14 y ABHD17B—decide si la puerta de la glutamina ASCT2 se etiqueta para su destrucción o se mantiene abierta. Cuando la glutamina escasea, el sistema cambia para preservar ASCT2 y mantener el flujo de combustible, ayudando a los tumores a sobrevivir en condiciones adversas. Al bloquear conjuntamente ASCT2 y la vía JNK que lo protege, los investigadores lograron privar de nutrientes a las células cancerosas con mayor eficacia en modelos de laboratorio y animales. Aunque se necesitan más ensayos, este eje fosforilación–palmitoilación ofrece una nueva y prometedora vía para terapias destinadas a cortar las líneas de vida de nutrientes de los tumores de pulmón hambrientos de glutamina.
Cita: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Palabras clave: metabolismo de la glutamina, cáncer de pulmón no microcítico, transportador ASCT2, palmitoilación de proteínas, señalización JNK