Clear Sky Science · es
Inhibir HSP27 activa la interacción XBP1s/CerS1, que dispara la mitofagia impulsada por DRP1, protegiendo así frente a la muerte celular y promoviendo el ciclo lítico del KSHV en células de linfoma de derrame primario
Cuando el estrés celular se convierte en una espada de doble filo
Nuestras células sobreviven a los ataques cotidianos activando programas de emergencia que reparan el daño y las mantienen vivas. Sin embargo, las células cancerosas pueden secuestrar esos mismos programas para crecer y proteger virus latentes. Este artículo explora cómo bloquear una única proteína protectora frente al estrés en un linfoma raro no solo empuja a las células tumorales hacia la muerte, sino que además ofrece a un virus oculto en su interior una ventana para despertarse y multiplicarse. Comprender este delicado equilibrio podría ayudar a diseñar terapias que eliminen el cáncer sin dar al virus oportunidad de propagarse.
Un virus oculto en un linfoma agresivo
El linfoma de derrame primario es un cáncer muy agresivo de células B, un tipo de glóbulo blanco. La mayoría de estas células tumorales albergan un pasajero en estado latente: el herpesvirus asociado al sarcoma de Kaposi (KSHV). En su estado silencioso, o latente, el virus produce solo unas pocas proteínas y se oculta dentro del genoma del huésped. Ciertos estreses pueden empujarlo a una fase activa, lítica, en la que se replica y genera nuevas partículas virales, normalmente provocando la muerte de la célula huésped. Las propias células tumorales dependen de varios sistemas de respuesta al estrés, incluidas las denominadas proteínas de choque térmico y la respuesta a proteínas mal plegadas (unfolded protein response), que les ayudan a lidiar con proteínas mal plegadas, alteraciones del metabolismo de los lípidos y daños en sus mitocondrias productoras de energía. 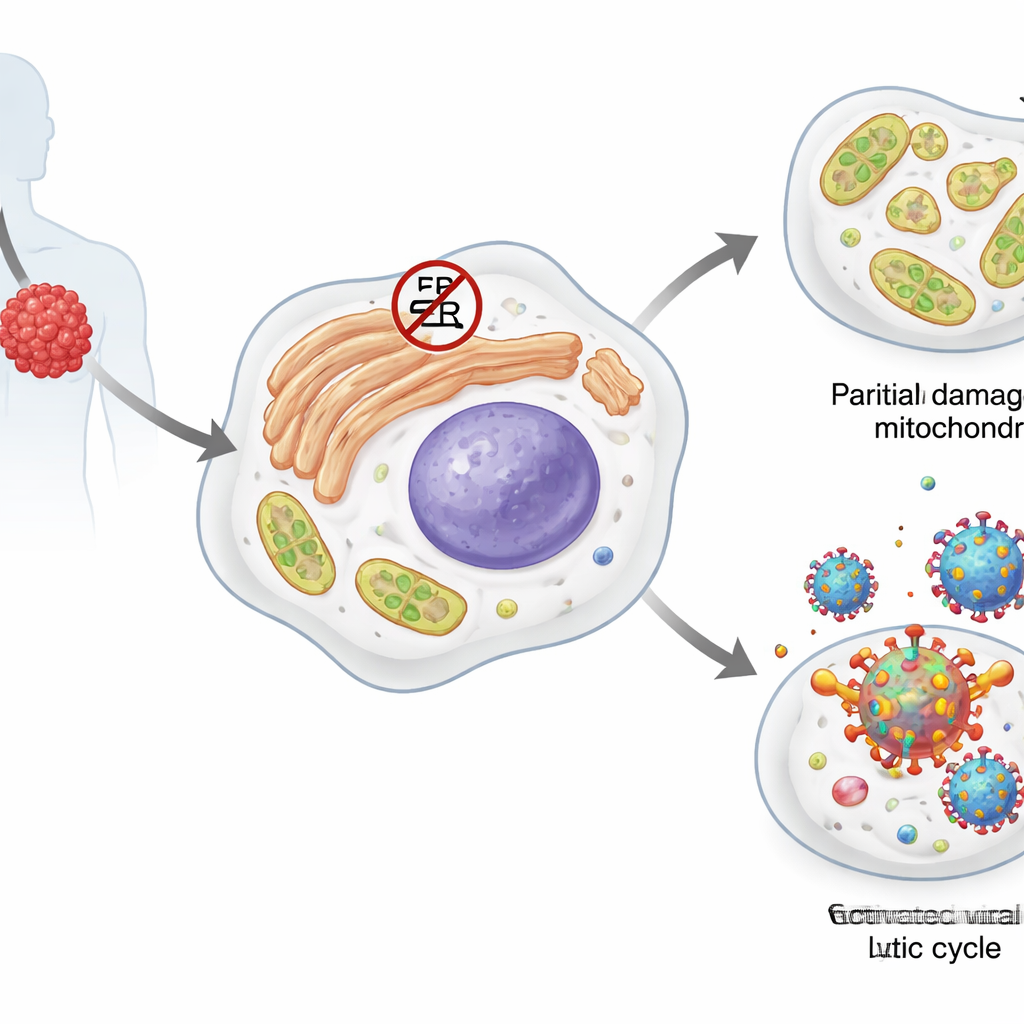
Bloquear a un guardaespaldas celular
Los investigadores se centraron en HSP27, una pequeña proteína de choque térmico conocida por proteger a las células frente al estrés. Usando un inhibidor químico llamado J2 o silenciando el gen con pequeños ARN, redujeron la actividad de HSP27 en células de linfoma cultivadas en el laboratorio. Esto hizo que las células fueran menos capaces de sobrevivir y desencadenó una intensa señal de estrés en una red de membranas interna llamada retículo endoplásmico. Aumentaron los marcadores de esta respuesta, incluidos factores protectores y pro‑muerte, y se activó un interruptor clave llamado XBP1s. Al mismo tiempo, las células mostraron más signos de muerte celular programada, lo que confirma que eliminar HSP27 las empuja hacia un punto de inflexión entre la supervivencia y la desaparición.
Un bucle de estrés que se comunica con los lípidos celulares
El estrés en el retículo endoplásmico está estrechamente entrelazado con el manejo de lípidos por parte de la célula. El equipo encontró que bloquear HSP27 aumentó los niveles de CerS1, una enzima que sintetiza una molécula lipídica específica llamada ceramida C18. Cuando inhibieron químicamente XBP1s, el aumento de CerS1 desapareció, lo que muestra que XBP1s contribuye a activar el gen CerS1 en estas condiciones. De forma llamativa, inhibir CerS1 redujo a su vez los niveles de XBP1s, revelando un bucle de retroalimentación positiva: cada factor sostiene al otro. Este apretón de manos molecular no solo remodela el metabolismo lipídico, sino que también refuerza la capacidad de la célula para adaptarse al estrés del retículo endoplásmico, aun cuando las señales de muerte se están acumulando.
Mitocondrias recicladas en lugar de destruidas
El estrés en una parte de la célula a menudo se extiende a las mitocondrias, las pequeñas centrales eléctricas que generan energía. Tras bloquear HSP27, las células de linfoma produjeron más especies reactivas de oxígeno, indicio de problemas mitocondriales, y aumentaron los niveles de DRP1, una proteína que fragmenta las mitocondrias en piezas más pequeñas. Los autores demostraron que el bucle XBP1s–CerS1 era responsable del aumento de DRP1. Esto, a su vez, desencadenó la mitofagia, un proceso de control de calidad en el que las mitocondrias dañadas se envuelven en membranas y se envían a los “centros de reciclaje” celulares llamados lisosomas. Mediante tintes fluorescentes y marcadores proteicos, confirmaron que las mitocondrias se eliminaban de forma selectiva. Cuando inhibieron DRP1 química o genéticamente, esta mitofagia se redujo y las células murieron con mayor facilidad, lo que significa que el reciclaje mitocondrial estaba ayudando a las células tumorales estresadas a resistir.
Dando al virus tiempo para escapar
La misma mitofagia que protegía a las células tumorales también benefició al KSHV. La activación de XBP1s, la acumulación de ceramida C18 y el aumento de la fragmentación mitocondrial se han relacionado con el despertar de este virus. Aquí, cuando se inhibió HSP27, más células expresaron proteínas virales tempranas y tardías, señales claras de replicación lítica. Bloquear DRP1, y por tanto la mitofagia, redujo esta reactivación viral. Los autores sugieren que al prolongar ligeramente la supervivencia celular bajo estrés, la mitofagia da al KSHV tiempo para completar su ciclo de replicación y abandonar la célula moribunda, potencialmente infectando nuevos objetivos y contribuyendo al desarrollo del cáncer.
Qué significa esto para tratamientos futuros
Para un público no especializado, el mensaje clave es que HSP27 actúa como un controlador central de tráfico sobre cómo las células de linfoma afrontan el estrés, cómo reciclan mitocondrias dañadas y cómo un virus asociado al cáncer decide cuándo despertarse. Apagar HSP27 desata una cadena de eventos que tanto socava la supervivencia celular como, paradójicamente, protege temporalmente a las células mediante la mitofagia mientras permite que KSHV se replique. Desde el punto de vista terapéutico, combinar la inhibición de HSP27 con fármacos que bloqueen la mitofagia impulsada por DRP1 podría empujar a las células tumorales a morir más rápido y limitar la oportunidad del virus de propagarse, ofreciendo una estrategia doble contra este linfoma letal.
Cita: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Palabras clave: linfoma de derrame primario, virus de Kaposi, respuesta al estrés celular, mitofagia, proteína de choque térmico HSP27