Clear Sky Science · es
Un modelo de ratón viable con RIPK3 cinasa-inactiva D143N revela su función de andamiaje en el impulso de trastornos inflamatorios inducidos por TNF
Por qué importa este estudio en ratones para la inflamación
Muchas enfermedades graves, desde infecciones mortales hasta brotes autoinmunes, no son causadas solo por gérmenes o genes, sino por la propia inflamación descontrolada del organismo. Una proteína llamada RIPK3 se ha considerado durante mucho tiempo como un ejecutor clave de una forma violenta de muerte celular que alimenta esa inflamación, lo que la convierte en un objetivo farmacológico atractivo. Pero RIPK3 también desempeña otros papeles dentro de la célula menos comprendidos. Este estudio describe un nuevo tipo de ratón de laboratorio que separa de forma limpia la actividad letal de RIPK3 de su papel de señalización como «andamiaje», revelando cómo cada función contribuye a la inflamación y apuntando a nuevas estrategias terapéuticas.
Dos maneras en que puede actuar una proteína de muerte
Las células pueden morir de forma ordenada o desordenada. En la muerte celular ordenada y «silenciosa», el organismo recicla las partes celulares sin alarma notable. En una forma más desordenada llamada necroptosis, las células estallan y vierten su contenido, lo que desencadena respuestas inmunitarias intensas. RIPK3 es central en la necroptosis: cuando se activa, pone en marcha a otra proteína que perfora la membrana celular. Sin embargo, trabajos previos sugerían que RIPK3 también puede ayudar a desencadenar la apoptosis clásica mediada por caspasas y puede potenciar la señalización inflamatoria incluso sin matar células. Desentrañar estos roles ha sido difícil porque las formas inactivas de RIPK3 disponibles hasta ahora o mataban embriones o reducían drásticamente los niveles de la proteína, lo que dificultaba estudiar su comportamiento normal como andamiaje.
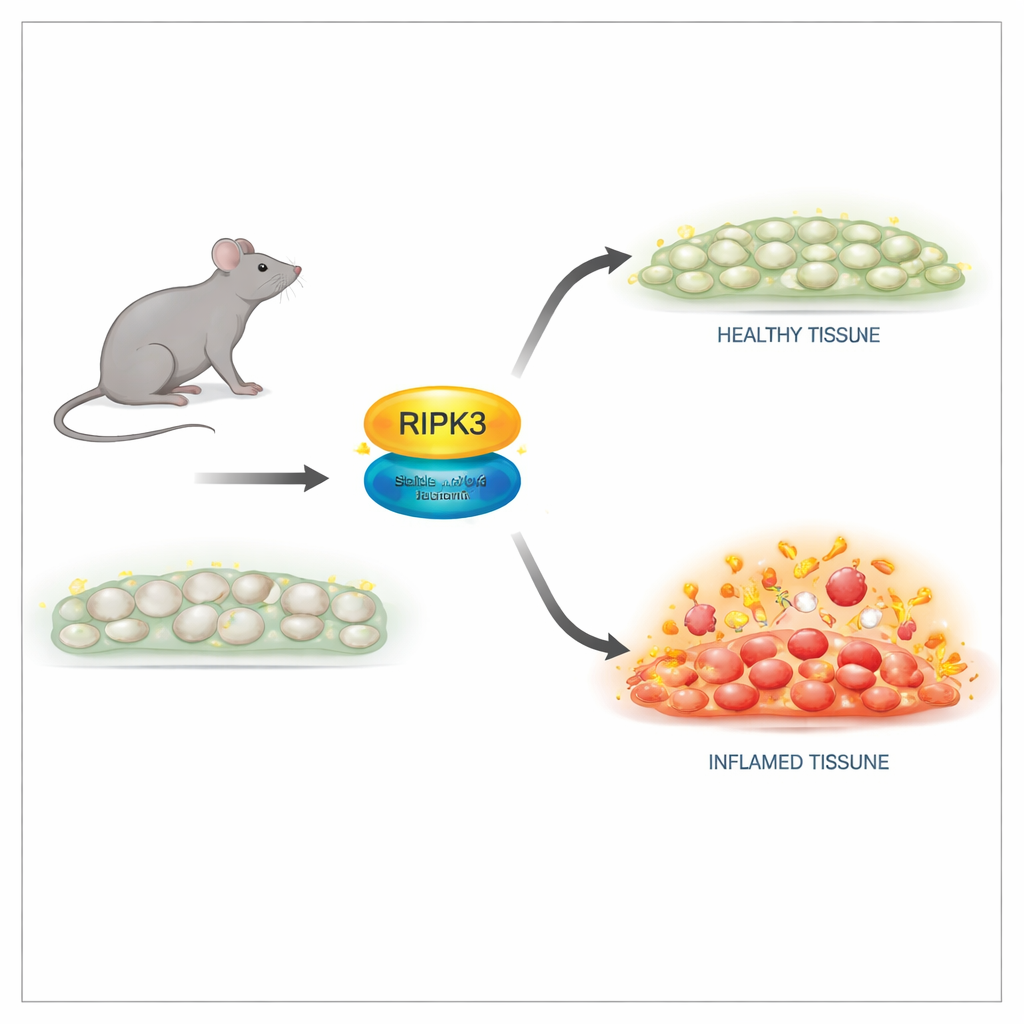
Una forma más segura de desactivar la función letal
Los investigadores diseñaron ratones que portan un cambio sutil en la proteína RIPK3 en una única posición, denominado D143N, que elimina su actividad enzimática preservando su estructura. En células de estos ratones, los niveles de RIPK3 y la arquitectura tisular parecían normales, y los animales nacieron y crecieron igual que sus camadas sanas. Importante: las células con la versión D143N fueron completamente resistentes a múltiples desencadenantes de necroptosis, incluidos los estímulos del factor de necrosis tumoral (TNF), receptores tipo toll y la infección viral. El RIPK3 mutante ya no podía activar a su socio aguas abajo ni formar el complejo destructivo necesario para la rotura de la membrana, y aun así no provocó apoptosis espontánea, evitando los efectos letales observados en mutantes anteriores de RIPK3.
Separando el desarrollo de la enfermedad
Uno de los roles más conocidos de RIPK3 se observa en embriones que carecen de otra proteína clave, la caspasa-8: sin caspasa-8, la necroptosis mediada por RIPK3 mata al embrión. En este estudio, introducir la versión D143N de RIPK3 rescató por completo a estos ratones que de otro modo no serían viables. Se desarrollaron normalmente y fueron fértiles, lo que demuestra que la actividad letal de RIPK3 no es imprescindible para el desarrollo normal cuando se preserva su estructura. Sin embargo, cuando ratones adultos fueron desafiados con dosis altas de TNF para inducir un síndrome inflamatorio tipo shock, el panorama cambió. Los animales que carecían por completo de RIPK3 estaban fuertemente protegidos contra la muerte, el daño tisular y las moléculas inflamatorias en sangre. Los ratones con la versión D143N, a pesar de no poder sufrir necroptosis, solo mostraron una protección parcial. Esto indicó que el papel no letal de andamiaje de RIPK3 seguía contribuyendo a impulsar la inflamación.
Señalización de andamiaje que aviva las llamas
Para comprender esta contribución no letal, el equipo examinó la actividad génica en el intestino de ratones tratados con TNF. En animales deficientes en RIPK3, muchos genes inflamatorios estaban fuertemente atenuados. En los ratones D143N, sin embargo, la supresión fue más débil, y los genes ligados a interferones y respuestas innatas siguieron más activos. A nivel de proteína, TNF activó con fuerza las vías de señalización JAK–STAT1 y ERK en ratones normales y D143N, pero esta activación estuvo casi ausente cuando RIPK3 se eliminó por completo. Esto mostró que, incluso sin su función letal, la presencia física de RIPK3 en complejos de señalización ayuda a transmitir las señales de TNF hacia un programa proinflamatorio a través de JAK–STAT1.
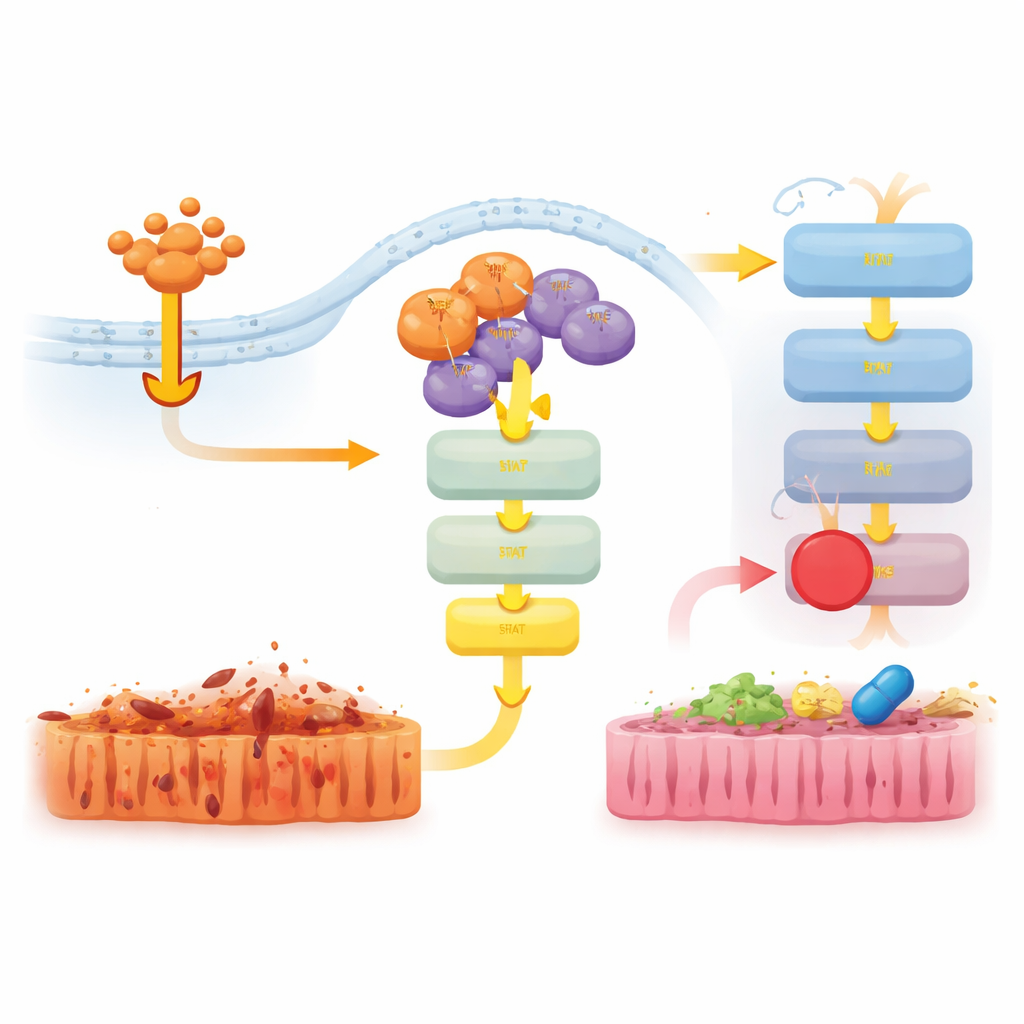
Atenuar señales dañinas con fármacos dirigidos
Los investigadores probaron luego si bloquear estas vías aguas abajo podría aliviar la enfermedad en ratones D143N sometidos a shock inducido por TNF. Tratar a los animales con un inhibidor de JAK1/2, pero no con un inhibidor de ERK, redujo la pérdida de temperatura corporal, disminuyó los niveles de la molécula inflamatoria IL-6 y atenúo el daño tisular y la muerte celular en el intestino. Un inhibidor distinto dirigido a otra proteína, RIPK1, también protegió con fuerza a los ratones y redujo la activación de JAK–STAT1 y ERK. En conjunto, estos resultados sugieren que la función de andamiaje de RIPK3 coopera con RIPK1 para activar JAK–STAT1 y promover la inflamación, y que interrumpir esta señalización puede reducir la lesión tisular incluso cuando la necroptosis ya está bloqueada.
Qué significa esto para tratamientos futuros
Durante años, RIPK3 se ha visto principalmente como un interruptor de una forma tóxica de muerte celular, y el desarrollo de fármacos se ha centrado en apagar su actividad enzimática. Este estudio muestra que eso puede no ser suficiente: RIPK3 sigue pudiendo actuar como una plataforma física que amplifica señales inflamatorias a través de JAK–STAT1, contribuyendo al shock y al daño tisular. El nuevo modelo de ratón D143N revela estos roles duales con una claridad inusual, estableciendo una herramienta potente para estudiar cuándo y cómo cada función importa en distintas enfermedades. Para los pacientes, el trabajo sugiere que combinar fármacos dirigidos a RIPK3 o RIPK1 con inhibidores de JAK–STAT1 podría calmar con más eficacia la inflamación dañina en condiciones impulsadas por TNF y citocinas relacionadas.
Cita: Du, Y., Li, J., Zhao, C. et al. A viable kinase-inactive RIPK3 D143N mouse model reveals its scaffold function in driving TNF-induced inflammatory disorder. Cell Death Discov. 12, 107 (2026). https://doi.org/10.1038/s41420-026-02962-x
Palabras clave: RIPK3, necroptosis, inflamación, shock por TNF, JAK-STAT1