Clear Sky Science · es
El eje AdipoR1–AMPK suprime el cáncer de mama en distintos subtipos moleculares mediante vías multimodales de muerte celular, incluida la ferroptosis y la apoptosis
Por qué las células grasas importan en el cáncer de mama
La mayoría pensamos en la grasa corporal como un depósito pasivo de energía, pero las células grasas son fábricas activas que liberan hormonas y moléculas señalizadoras al torrente sanguíneo. Este estudio explora cómo una de esas señales derivadas de la grasa, que actúa a través de una molécula llamada AdipoR1 en las células del cáncer de mama, puede frenar el crecimiento tumoral. El trabajo es relevante porque sugiere una nueva vía para tratar muchas formas de cáncer de mama aprovechando la comunicación entre el tejido adiposo y los tumores, potencialmente reforzando los efectos de los fármacos existentes.
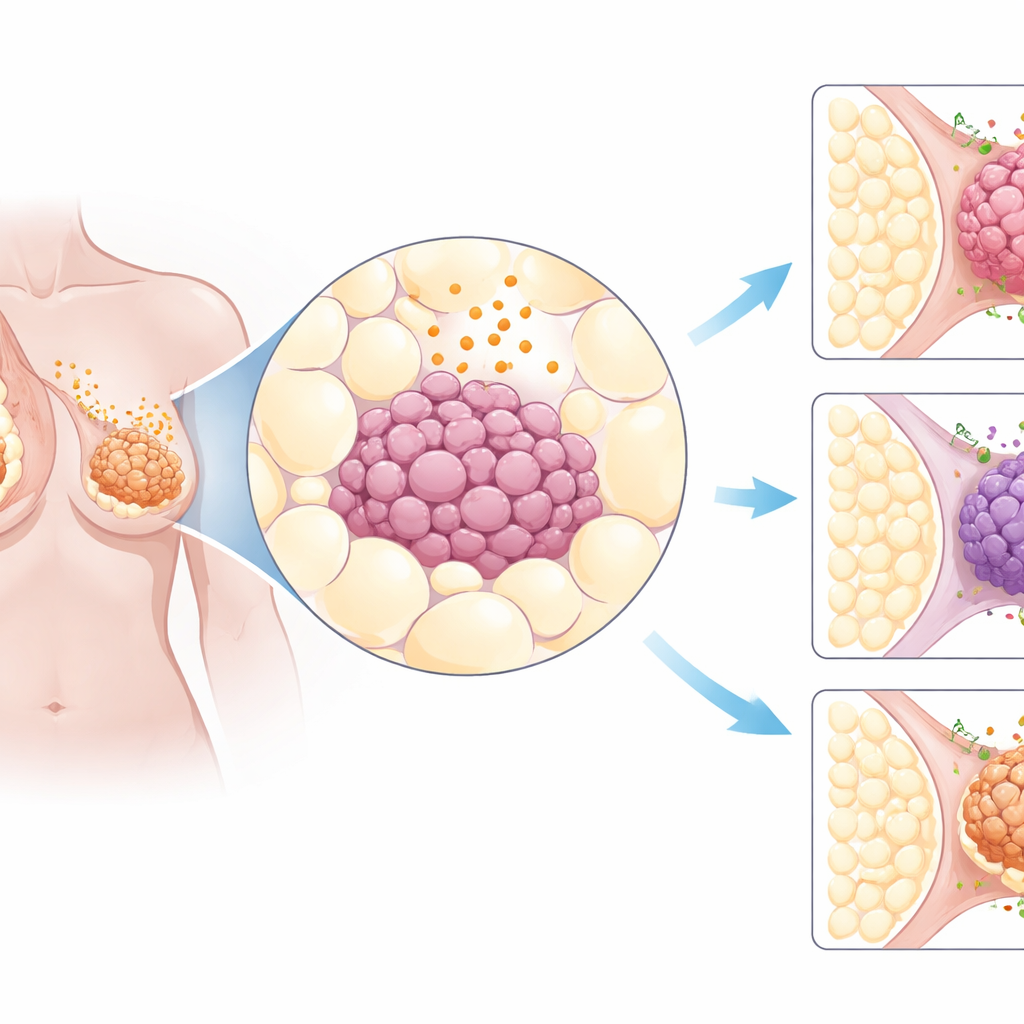
Observando a lo largo de muchos cánceres
Los investigadores comenzaron excavando grandes bases de datos públicas de cáncer que contienen información genética de miles de tumores de pacientes. Se centraron en unas tres docenas de genes implicados en las señales procedentes del tejido adiposo y en las estructuras celulares que reciben esas señales. Al comparar tumores de 31 órganos distintos con tejido sano, surgió un patrón claro: los cánceres de mama mostraban cambios especialmente notables en estas señales relacionadas con la grasa. En particular, el receptor AdipoR1 aparecía con frecuencia en niveles más altos de lo normal en tumores mamarios, tanto si eran impulsados por hormonas, HER2‑positivos o del tipo más agresivo triple negativo. Muestras de tejido de más de 600 cánceres de mama confirmaron que la proteína AdipoR1 estaba ampliamente presente en las células tumorales.
Probando un fármaco que imita la señal grasa en células cancerosas
Para ver qué hace AdipoR1 dentro de los tumores, el equipo recurrió a líneas celulares de cáncer de mama cultivadas en el laboratorio, que representan varios subtipos comunes. Trataron estas células con AdipoRon, una pequeña molécula que activa AdipoR1. AdipoRon activó rápidamente un interruptor conocido de detección energética en las células llamado AMPK, demostrando que la señal llegaba. A medida que aumentaba la dosis de AdipoRon, las células cancerosas se dividían más lentamente, se desplazaban menos en pruebas de cicatrización de heridas y muchas entraban en autodestrucción programada. Cuando los investigadores redujeron deliberadamente los niveles de AdipoR1 en las células, AdipoRon perdió gran parte de su efecto, mientras que aumentar AdipoR1 hizo que el fármaco fuera más eficaz, vinculando el efecto directamente con este receptor.
Múltiples maneras de empujar a las células cancerosas hacia la muerte
Al analizar la actividad génica tras el tratamiento, los científicos observaron que AdipoRon activaba respuestas de estrés dentro de las células del cáncer de mama. Activó genes asociados a la muerte celular programada clásica, así como genes implicados en una forma más recientemente reconocida de destrucción celular dependiente del hierro llamada ferroptosis. Marcadores clave de este proceso aumentaron tanto a nivel de ARN como de proteína, especialmente en células de cáncer de mama sensibles a hormonas, y lecturas químicas de lípidos celulares dañados apoyaron este hallazgo. Al mismo tiempo, AdipoRon redujo los niveles de proteínas que normalmente ayudan a las células cancerosas a sobrevivir, incluidos ayudantes de reparación del ADN (BRCA1 y BRCA2), el receptor de estrógenos que impulsa el crecimiento en muchos tumores y TROP2, una molécula de superficie vinculada a un comportamiento agresivo.
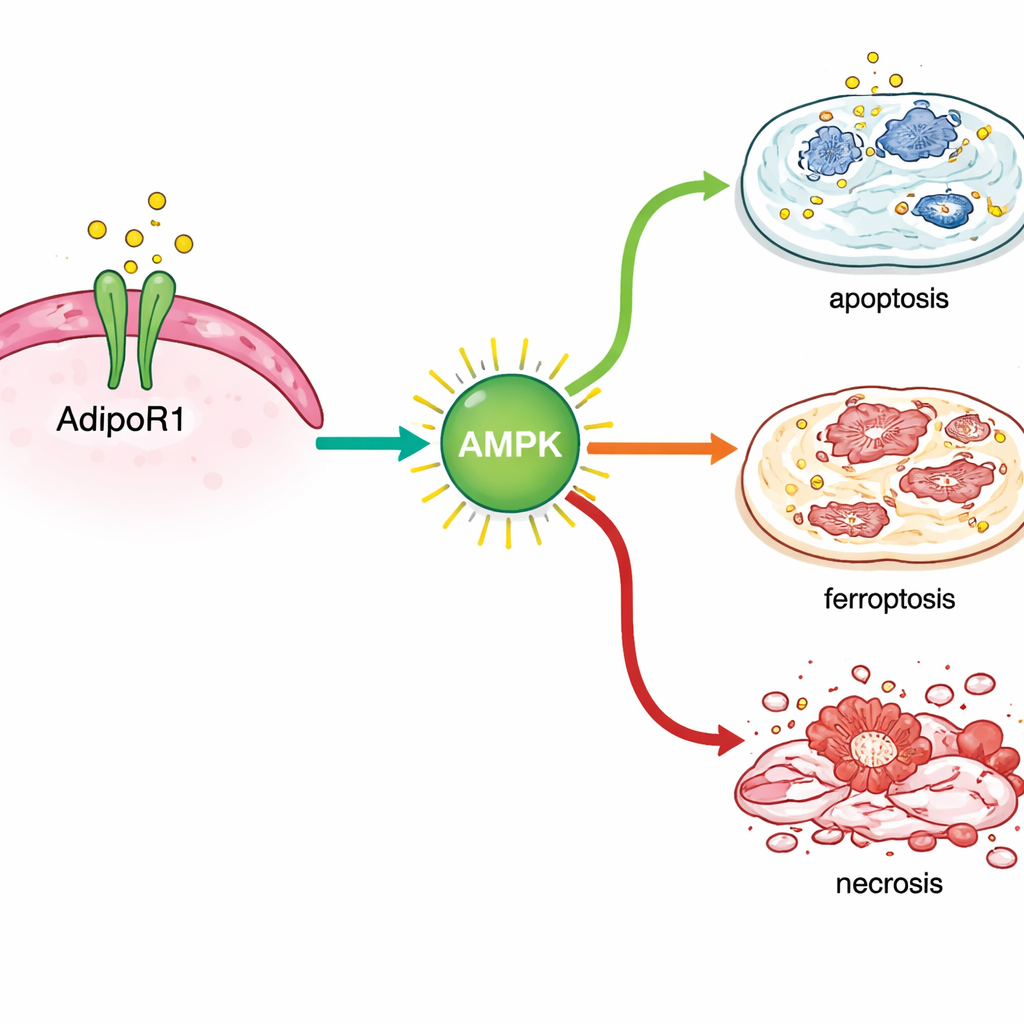
Trabajar con, no en contra de, los tratamientos actuales
El equipo se preguntó entonces si activar AdipoR1 podría complementar los fármacos estándar. En células de cáncer de mama sensibles a hormonas, AdipoRon combinado con tamoxifeno produjo una supresión del crecimiento mayor que cualquiera de los dos fármacos por separado. En líneas triple negativas, AdipoRon potenció los efectos de agentes quimioterápicos comunes como el paclitaxel y la doxorrubicina. Pasando a ratones con tumores mamarios sensibles a hormonas, los investigadores administraron AdipoRon por vía oral. Los tumores en los animales tratados crecieron más despacio y contenían zonas de necrosis más grandes al examinarse al microscopio. Importante: los ratones no mostraron efectos secundarios evidentes en comportamiento, peso o salud hepática durante el tratamiento.
Qué podría significar esto para los pacientes
En conjunto, los hallazgos sugieren que activar AdipoR1 en las células del cáncer de mama activa varias vías superpuestas hacia la muerte celular mientras debilita sistemas clave de supervivencia, y que este enfoque funciona a través de diferentes formas genéticas de la enfermedad. En lugar de reemplazar las terapias actuales, fármacos que apunten a AdipoR1 como AdipoRon podrían actuar como complementos que hacen a los tumores más vulnerables a la terapia hormonal, la quimioterapia o futuros agentes dirigidos. Antes de que esta estrategia llegue a la clínica, los investigadores deberán desarrollar activadores de AdipoR1 más potentes y selectivos, aclarar en qué pacientes los tumores expresan con mayor intensidad el receptor y evaluar la seguridad con cuidado. Aun así, este trabajo apunta a una idea intrigante: las señales de nuestro propio tejido graso podrían redirigirse para ayudar a combatir el cáncer de mama en lugar de alimentarlo.
Cita: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Palabras clave: cáncer de mama, adipocinas, AdipoR1, vías de muerte celular, metabolismo del cáncer