Clear Sky Science · es
Papel de las balsas lipídicas en la señalización oncogénica mediada por FGFR2c mediante la participación del canal TRPA1 en células de adenocarcinoma ductal pancreático
Por qué importan las pequeñas islas en las membranas celulares
El cáncer de páncreas es uno de los más letales, en parte porque sus células son extraordinariamente eficaces a la hora de desprenderse del tumor original e invadir tejidos cercanos. Este estudio examina unas pequeñas “islas” en la superficie de las células cancerosas, formadas por colesterol y lípidos, y plantea una pregunta sencilla con importantes implicaciones: ¿estas islas ayudan a activar una señal de crecimiento que hace al cáncer de páncreas más agresivo, y puede su alteración ralentizar ese proceso?
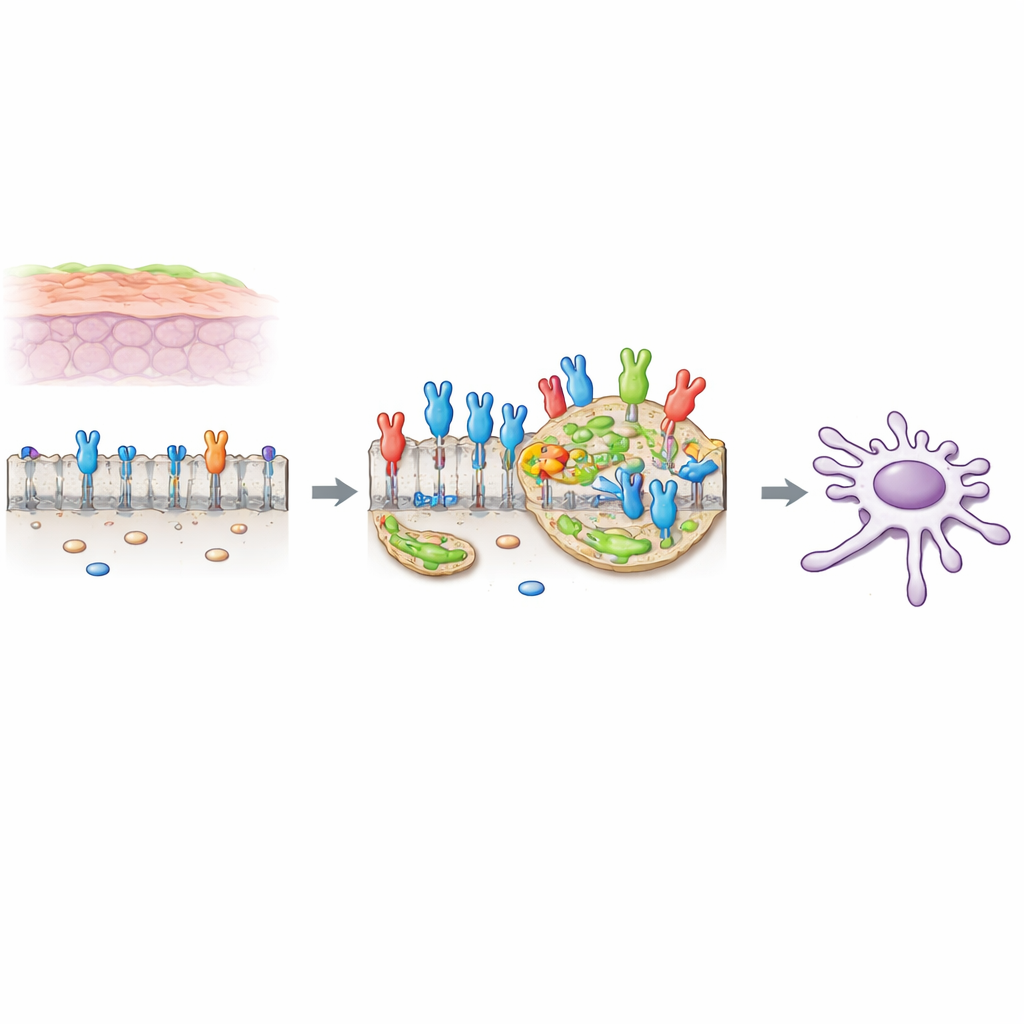
Un interruptor que favorece el cáncer en la superficie celular
Muchas células poseen interruptores en su superficie que responden a señales de crecimiento. Uno de estos interruptores, llamado FGFR2c, es una variante que normalmente se encuentra en células más flexibles y móviles, pero que aparece de forma anómala en gran cantidad en células de adenocarcinoma ductal pancreático (PDAC). Cuando este interruptor se activa por su molécula ligando en el entorno, induce cambios conocidos como transición epitelio–mesénquima (EMT), que hacen que las células se despeguen más y aumenten su capacidad de movimiento e invasión. Trabajos previos de los autores mostraron que, en células PDAC, FGFR2c activa una cascada de mensajeros intracelulares que incluye a la proteína PKCε y varias vías clásicas de crecimiento, potenciando la supervivencia, la migración y la invasión celular.
Islas ricas en colesterol como amplificadores de señal
La membrana externa de la célula no es uniforme. Contiene pequeños parches ricos en colesterol, llamados balsas lipídicas, que actúan como plataformas diminutas donde las moléculas de señalización pueden agruparse y comunicarse con mayor eficacia. Los investigadores encontraron que, cuando FGFR2c se activa por su señal externa, más receptores se desplazan hacia estas balsas lipídicas. Utilizando marcadores fluorescentes y fraccionamiento bioquímico, mostraron que FGFR2c activado se concentra en estos parches, mientras que su distribución fuera de las balsas cambia de un patrón liso a uno punteado, coherente con el agrupamiento del receptor en estas islas.
Deshacer las islas debilita rasgos cancerígenos
Para probar si estas islas lipídicas son esenciales para los efectos promotores del cáncer de FGFR2c, el equipo usó un compuesto (metil-β-ciclodextrina) que elimina selectivamente colesterol de la membrana y desestabiliza las balsas sin matar las células. En células PDAC con alto contenido de FGFR2c, la disrupción de las balsas redujo de forma marcada la activación de moléculas de señalización clave aguas abajo del receptor y atenuó el programa de EMT: los genes y proteínas asociados a un estado móvil e invasivo disminuyeron, mientras que las características epiteliales se restauraron parcialmente. El mismo tratamiento también redujo los niveles de proteínas vinculadas a la invasión como MCL-1, SRC y enzimas degradadoras de matriz, y disminuyó la capacidad de las células cancerosas para desplazarse y penetrar un gel que simula el tejido circundante. Las células con muy poco FGFR2c mostraron casi ninguna respuesta, lo que subraya lo central que es esta asociación receptor–balsa en estos tumores.
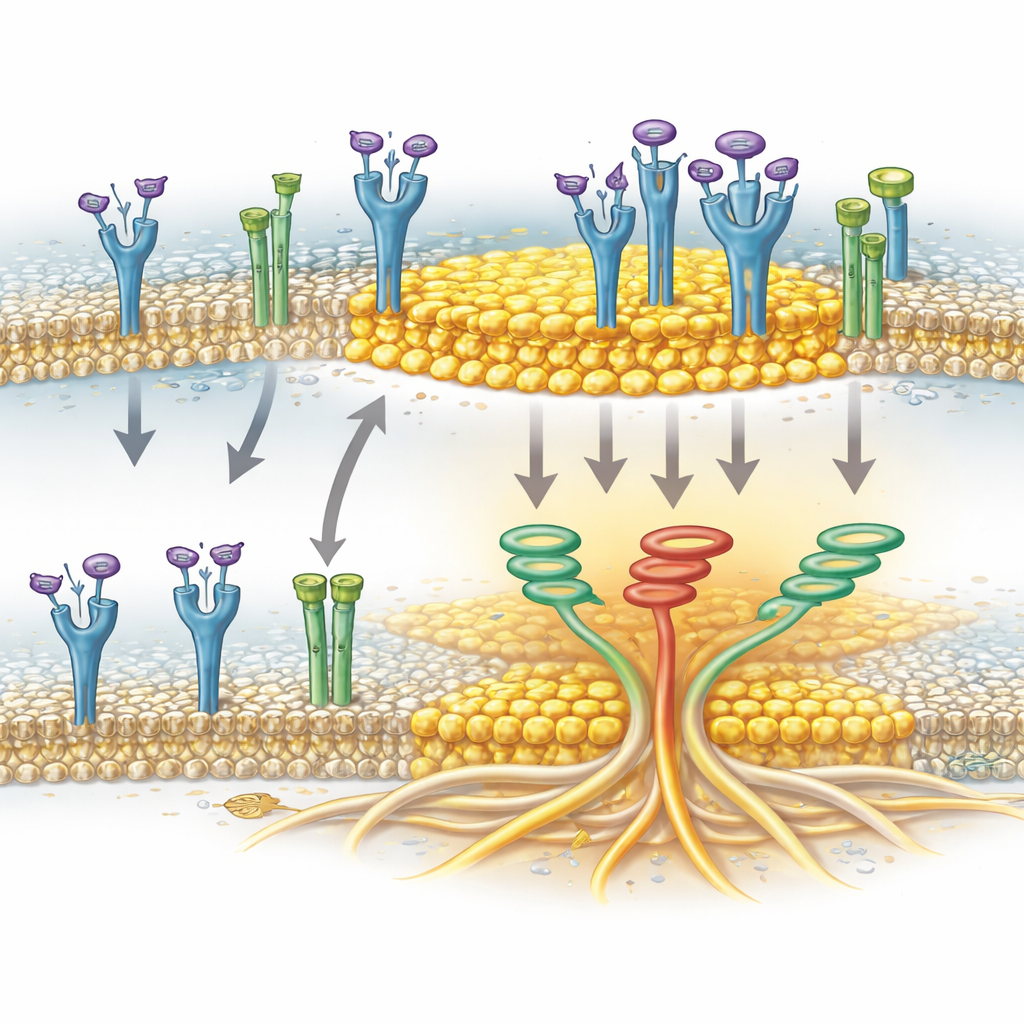
Un canal iónico como colaborador del agrupamiento
El estudio también identifica un colaborador sorprendente: TRPA1, una proteína de canal conocida principalmente por detectar irritantes y estrés oxidativo en las neuronas. En las células de cáncer de páncreas, TRPA1 está presente en la membrana y puede localizarse en balsas lipídicas. Los autores demostraron que TRPA1 se asocia físicamente con FGFR2c cuando el receptor se activa y que esta asociación coincide con el enriquecimiento de FGFR2c en las fracciones de balsa. Cuando se redujeron los niveles de TRPA1, FGFR2c activado dejó de acumularse eficientemente en las regiones de balsa, aunque las propias balsas permanecieron intactas. Esto indica que TRPA1 no es un mero pasajero pasivo, sino que contribuye activamente a escoltar o estabilizar a FGFR2c dentro de estas plataformas ricas en colesterol, donde el receptor puede desencadenar con mayor eficacia la red de señalización invasiva.
Qué significa esto para futuros tratamientos
En conjunto, el trabajo pinta un panorama en el que FGFR2c, TRPA1 y las balsas lipídicas forman una unidad cooperativa que refuerza el comportamiento invasivo de las células de cáncer de páncreas. FGFR2c aporta la señal de crecimiento, las balsas lipídicas ofrecen el escenario físico donde se ensamblan los complejos de señalización, y TRPA1 ayuda a llevar el receptor a ese escenario. Para un lector no especializado, la conclusión clave es que no solo las moléculas causantes del cáncer, sino también los pequeños paisajes membranosos que ocupan, pueden determinar lo peligroso que se vuelve un tumor. Al dirigirse a FGFR2c, TRPA1 o la estabilidad de estas islas ricas en colesterol—por separado o en combinación—las terapias futuras podrían debilitar la maquinaria invasiva de las células de cáncer de páncreas de una manera más precisa y específica para el tumor.
Cita: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Palabras clave: cáncer de páncreas, balsas lipídicas, FGFR2c, canal TRPA1, invasión celular