Clear Sky Science · es
Dirigiéndose a los mutantes cancerosos de p53 Y220C, Y220N y Y220S con el estabilizador de pequeña molécula rezatapopt
Por qué esto importa para los tratamientos futuros del cáncer
El cáncer suele desactivar a p53, una proteína a la que a veces se llama el “guardián” de la célula, mediante mutaciones que le impiden mantener a raya a las células peligrosas. Un cambio concreto en p53, conocido como Y220C, es frecuente en tumores sólidos y se ha convertido en un caso de prueba para fármacos que pretenden reparar el p53 dañado en lugar de matar células directamente. Este estudio plantea una cuestión práctica y orientada al paciente: ¿puede un fármaco experimental prometedor, rezatapopt, que ya está en ensayos clínicos para Y220C, ayudar también a personas cuyos tumores tienen mutaciones estrechamente relacionadas pero más raras en la misma posición de p53?
Un fármaco diseñado para parchear una grieta en p53
Muchas mutaciones de p53 hacen que la proteína se abra y pierda su forma precisa. En la mutación Y220C, el cambio crea una pequeña cavidad en la superficie de la proteína, un defecto que los químicos comprendieron que podría “taparse” con pequeñas moléculas a medida para estabilizar p53. Rezatapopt es una de esas moléculas, diseñada a partir de series químicas previas que se unen a esa cavidad y actúan como una abrazadera molecular. Los autores se centran en otras dos mutaciones en la misma posición de aminoácido, Y220S y Y220N, que también forman un bolsillo similar pero desestabilizan p53 aún más que Y220C. Si rezatapopt pudiera también parchear estas variantes, podría extender este enfoque de medicina de precisión a miles más de pacientes cada año. 
Midiendo cuánto rezatapopt sujeta y estabiliza el p53 mutante
Para probarlo, el equipo purificó el dominio central de unión al ADN de p53 con las mutaciones Y220C, Y220S o Y220N y expuso cada una a rezatapopt (y a compuestos químicamente cercanos). Usando ensayos basados en calor, mostraron que las tres proteínas mutantes se volvieron más estables cuando el fármaco se unía, con Y220C y Y220S recuperando eficazmente una robustez similar a la de tipo salvaje. En contraste, Y220N recuperó solo parte de la estabilidad perdida. Una segunda técnica que mide el calor liberado al unirse reveló por qué: rezatapopt se adhiere muy fuertemente a Y220C (del orden de unas decenas de nanomolares), algo menos fuerte a Y220S y más débil aún a Y220N, aunque todas están en rangos que los químicos medicinales consideran prometedores.
Viendo el parche molecular con detalle atómico
Estructuras cristalográficas de alta resolución proporcionaron una explicación visual. En las tres mutantes, rezatapopt se introduce en la hendidura creada por la mutación con una pose conservada: su andamiaje central llena la cavidad, un extremo alcanza profundamente el bolsillo con un racimo de átomos de flúor y el otro extremo interactúa con un lazo proteico cercano. El fármaco establece una red de contactos, incluido un átomo de flúor estratégicamente situado que interacciona con la cadena principal de la proteína. En Y220S, estas interacciones se mantienen con solo desplazamientos menores, permitiendo una fuerte estabilización. En Y220N, sin embargo, la unión del fármaco obliga a la cadena lateral de asparagina hacia el núcleo oleoso de la proteína de un modo energéticamente desfavorable, y se pierden algunos contactos con el “ancla” fluorada del fármaco. Este encaje forzado explica tanto la unión más débil como la recuperación incompleta de estabilidad. 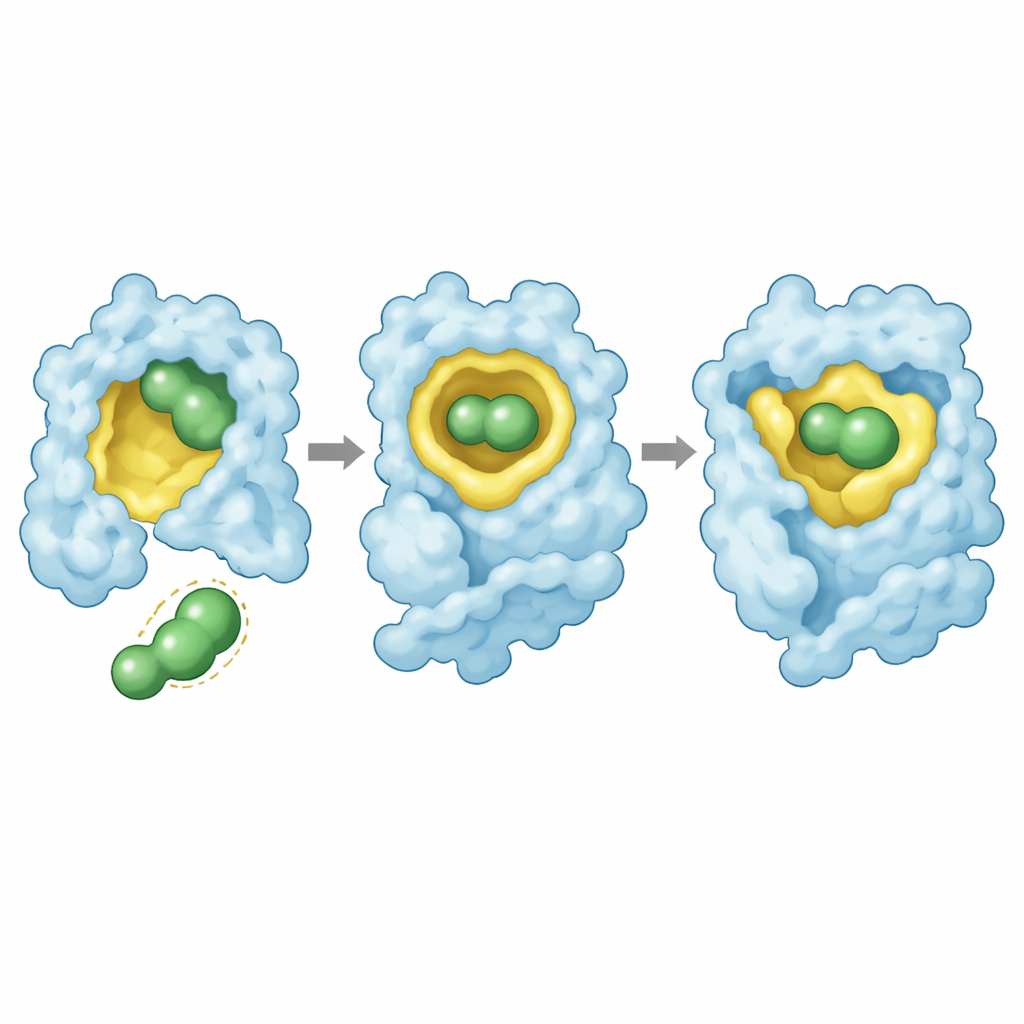
De la reparación de la proteína al comportamiento celular
La prueba crucial es si esa estabilización revive el papel protector de p53 dentro de células vivas. Los investigadores diseñaron células de cáncer de pulmón carentes de p53 natural para que expresaran las variantes Y220C, Y220S, Y220N o Y220H. Al tratarse con rezatapopt, las células con Y220C mostraron una potente activación de genes clásicos diana de p53 implicados en la detención del ciclo celular y el desencadenamiento de la muerte celular. Las células Y220S mostraron un patrón muy similar: recuperación de la forma plegada y activa de p53, fuerte activación génica, proliferación más lenta y aumento de la muerte celular, pero solo a concentraciones del fármaco más de diez veces superiores a las necesarias para Y220C. Las células Y220N, en comparación, no mostraron una activación clara de genes diana a dosis tolerables y permanecieron en gran medida en el estado mal plegado, aunque ligeros efectos tardíos sobre el crecimiento sugieren una rescate funcional solo parcial.
Qué significa esto para los pacientes y el diseño futuro de fármacos
Para las personas con tumores que portan la mutación Y220S, estos hallazgos son cautelosamente alentadores: rezatapopt puede, en principio, restaurar las funciones protectoras de p53, pero solo a dosis sustancialmente más altas, lo que podría ser difícil de lograr con seguridad en pacientes. Para Y220N, el fármaco actual parece insuficiente para reparar completamente p53 en condiciones realistas. Aun así, los planos estructurales de este trabajo explican por qué el diseño actual rinde menos y cómo podrían ajustarse moléculas futuras para implicar las tres cadenas laterales mutantes sin forzarlas a posiciones desfavorables. En otras palabras, crear un verdadero fármaco de reparación de p53 “pan-Y220” parece desafiante pero alcanzable, y ampliaría modestamente el número de pacientes que podrían beneficiarse de esta estrategia emergente de arreglar, en lugar de reemplazar, el supresor tumoral del propio organismo.
Cita: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Palabras clave: reactivación de p53, rezatapopt, mutación Y220C, medicina de precisión contra el cáncer, estabilización de proteínas