Clear Sky Science · es
La desubiquitinación por OTUD4 estabiliza EGFR y activa la vía PI3K/AKT para promover la invasividad del cáncer de mama triple negativo
Por qué esta investigación importa para el cáncer de mama
El cáncer de mama triple negativo es una de las formas más difíciles de tratar porque carece de los marcadores hormonales y de crecimiento que apuntan muchas terapias. Este estudio descubre una molécula «protectora» oculta que ayuda a las células tumorales a mantener activado un potente interruptor de crecimiento. Al comprender este sistema de apoyo no evidente, los científicos podrían encontrar nuevas formas de cortar las señales que impulsan el crecimiento y la diseminación del tumor.
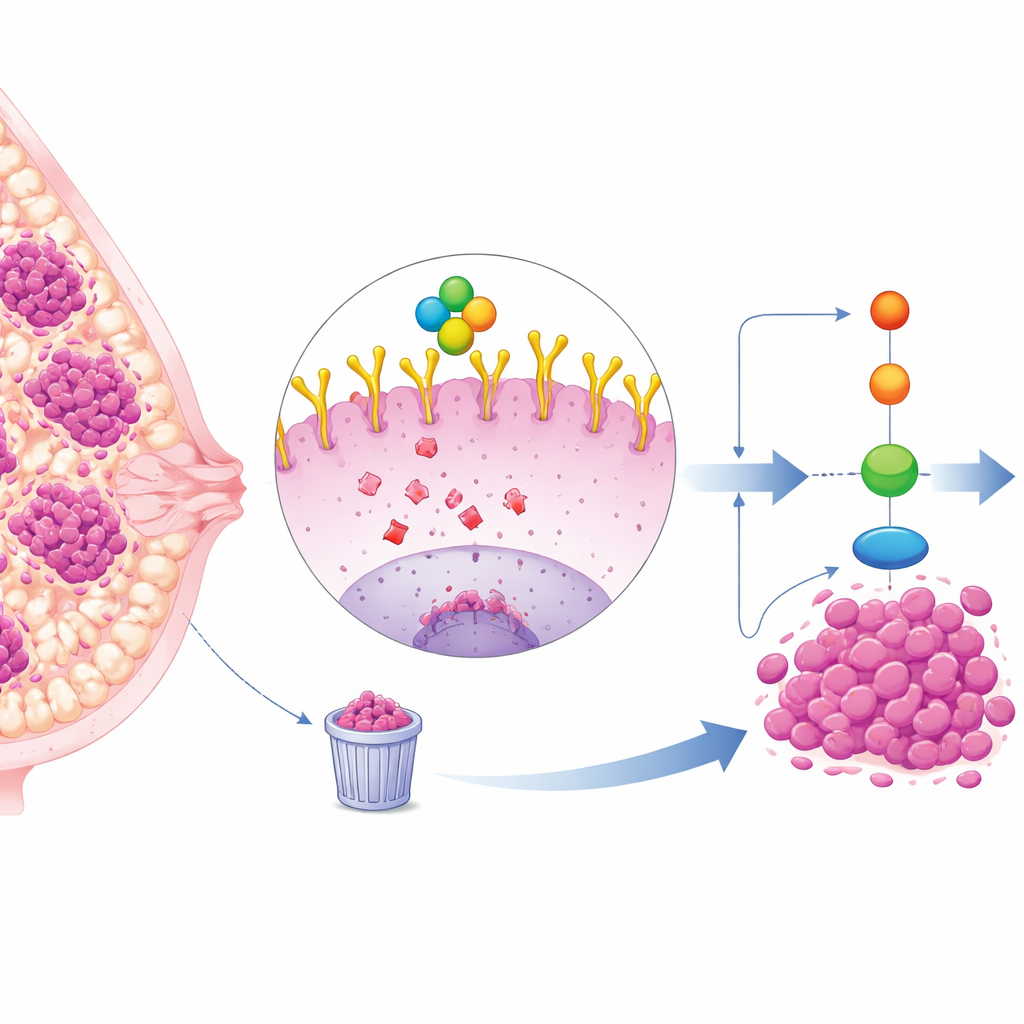
Un subtipo de cáncer de mama difícil de tratar
El cáncer de mama triple negativo (CMTN) representa aproximadamente una cuarta parte de los casos de cáncer de mama y tiende a crecer y diseminarse más rápido que otros subtipos. Dado que las células de CMTN no expresan receptores de estrógeno, progesterona ni HER2, las terapias dirigidas estándar son menos eficaces, quedando la quimioterapia y la cirugía como las principales opciones. No obstante, muchos tumores de CMTN muestran niveles altos de una proteína de superficie celular llamada EGFR, que actúa como una antena para recibir señales de crecimiento y supervivencia. Los niveles elevados de EGFR se asocian con malos pronósticos, pero los fármacos que bloquean directamente EGFR han dado resultados decepcionantes en la clínica, lo que sugiere que existen capas más profundas de regulación.
Encontrar un ayudante oculto del crecimiento tumoral
Los investigadores se centraron en OTUD4, una enzima que elimina pequeñas etiquetas proteicas llamadas ubiquitinas de otras proteínas. Estas etiquetas suelen actuar como señales de desecho, marcando proteínas para su degradación; al eliminarlas se puede estabilizar y proteger la proteína etiquetada. Mediante grandes bases de datos oncológicas y muestras de tejido de pacientes, el equipo mostró que OTUD4 está presente en niveles más altos en tumores y líneas celulares de CMTN que en tejido mamario normal. Los pacientes cuyos tumores tenían más OTUD4 tendían a presentar una peor supervivencia, lo que sugiere que OTUD4 se comporta como un oncogén, un gen que favorece la progresión del cáncer.
Cómo OTUD4 hace que las células cancerosas sean más agresivas
Para probar qué hace realmente OTUD4 en células de CMTN, los científicos redujeron sus niveles en dos líneas celulares de CMTN ampliamente estudiadas. Cuando OTUD4 se silenciaba, las células tumorales proliferaban más lentamente, formaban menos colonias y migraban menos en ensayos de cicatrización de heridas y Transwell, signos de menor agresividad. Cuando se incrementó OTUD4, ocurrió lo contrario: las células proliferaron más rápido y se movieron con mayor facilidad, reforzando la idea de que OTUD4 impulsa el comportamiento maligno. En ratones, los tumores formados a partir de células carentes de OTUD4 crecieron más despacio y mostraron marcadores reducidos de división celular y señales de crecimiento, confirmando estos efectos en organismos vivos.
Un escudo molecular que protege EGFR
Indagando en el mecanismo, el equipo utilizó cribados de interacción proteica y ensayos bioquímicos para identificar a EGFR como un socio de unión directo de OTUD4. Encontraron que OTUD4 se acopla a una región concreta de EGFR y elimina cadenas de ubiquitina unidas en K48, el tipo de etiqueta que normalmente marca a las proteínas para su destrucción por la maquinaria de reciclaje celular. Cuando se redujo OTUD4, EGFR se degradó más rápido, pero la actividad génica de EGFR permaneció igual, lo que demuestra que OTUD4 actúa después de la síntesis de EGFR, no a nivel del ADN o ARN. Bloquear el sistema de eliminación de proteínas restauró los niveles de EGFR, subrayando que el paso clave es la protección frente a la degradación. Con más EGFR estable en la superficie celular, una vía de señalización intracelular mayor, la vía PI3K/AKT/mTOR, permanece activada, impulsando el crecimiento y la supervivencia celular.
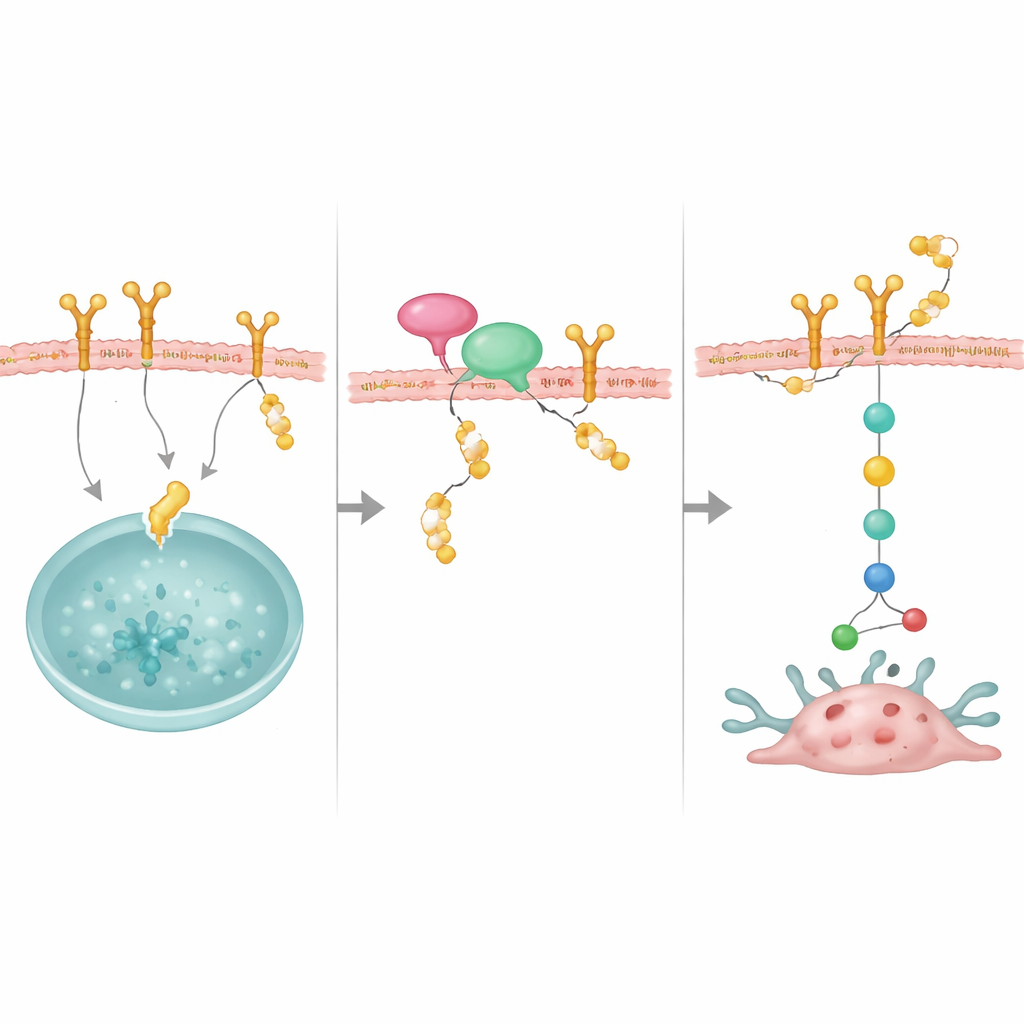
Un adaptador que acerca al protector a su objetivo
El estudio también descubrió un socio importante, NRP1, una proteína de membrana vinculada previamente con cánceres de mama agresivos. NRP1 se une tanto a OTUD4 como a EGFR y ayuda a situar a OTUD4 para rescatar EGFR de la destrucción. Cuando se redujo NRP1, EGFR fue menos estable y sus señales de crecimiento se debilitaron, aunque los niveles de OTUD4 no cambiaron. La sobreexpresión de OTUD4 pudo compensar en parte la pérdida de NRP1, lo que sugiere que NRP1 actúa como una plataforma de acoplamiento que recluta a OTUD4 hacia EGFR. Juntas, estas moléculas forman un complejo estabilizador que mantiene abundante a EGFR en la superficie celular.
Qué significa esto para tratamientos futuros
Al revelar cómo OTUD4 y NRP1 actúan en conjunto para proteger a EGFR de la degradación, este estudio identifica un nuevo punto de control de una señal de crecimiento clave en el cáncer de mama triple negativo. En lugar de intentar bloquear la actividad de EGFR en su sitio activo, las terapias futuras podrían dirigirse a interrumpir las acciones protectoras de OTUD4 o su reclutamiento por NRP1, reduciendo los niveles de EGFR y atenuando la vía PI3K/AKT que alimenta el crecimiento tumoral. Aunque se necesita más trabajo para encontrar inhibidores de OTUD4 seguros y eficaces y para entender posibles vías de escape que utilicen las células cancerosas, los hallazgos abren vías prometedoras para tratamientos más precisos contra este desafiante subtipo de cáncer de mama.
Cita: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Palabras clave: cáncer de mama triple negativo, señalización EGFR, OTUD4, vía PI3K AKT, degradación de proteínas