Clear Sky Science · es
La acil-CoA deshidrogenasa de cadena corta inicia la desmetilación y filtración del ADN mitocondrial para impulsar la inmunidad antitumoral en el cáncer colorrectal
Por qué nuestras propias células a veces ocultan el cáncer al sistema inmunitario
El cáncer colorrectal es uno de los tumores más letales del mundo, en parte porque las defensas inmunitarias del organismo con frecuencia no lo reconocen ni lo atacan. Este estudio descubre un vínculo inesperado entre cómo las células cancerosas queman grasas, cómo sus pequeñas centrales energéticas (mitocondrias) gestionan su ADN y si el sistema inmunitario se activa frente al tumor. Rastreando esta cadena de acontecimientos, los investigadores también ponen de relieve un compuesto natural antiguo, la hipericina, como una posible manera de reactivar el ataque inmune en el cáncer colorrectal.
Un “guardían” mitocondrial ausente en los tumores de colon
El equipo comenzó buscando en grandes conjuntos de datos humanos y de ratón genes metabólicos que cambian de forma constante en el cáncer colorrectal. Una enzima destacó: la acil-CoA deshidrogenasa de cadena corta, o ACADS, que normalmente ayuda a las mitocondrias a degradar ácidos grasos cortos. Tanto en muestras de pacientes como en varios modelos de ratón, los niveles de ACADS eran notablemente más bajos en el tejido tumoral que en el colon sano circundante. Cuando los científicos disminuyeron ACADS en células de cáncer de colon de ratón, los tumores crecieron más rápido y de forma más agresiva; aumentar ACADS ralentizó el crecimiento tumoral. Ratones diseñados para carecer de ACADS específicamente en el revestimiento intestinal desarrollaron más y mayores tumores en un modelo químico de cáncer asociado a colitis, lo que respalda la idea de que ACADS actúa como un supresor tumoral en el intestino.
Cómo los tumores apagan las señales de alarma inmunitarias
Estos efectos sobre el crecimiento no podían explicarse solo por la rapidez con la que las células cancerosas se multiplicaban en cultivo, que cambió poco. En cambio, la pérdida de ACADS solo impulsó el crecimiento tumoral en animales con sistemas inmunitarios intactos, lo que apunta a cambios en el microentorno tumoral. Los análisis unicelulares de cánceres colorrectales humanos mostraron que los tumores con baja ACADS estaban rodeados de más células tumorales y de células inmunes supresoras —como células supresoras derivadas de la médula, ciertos macrófagos y células T reguladoras— y de menos células T efectoras y células asesinas naturales. Este patrón sugiere un “vecindario inmunosupresor” que protege al cáncer frente al ataque. 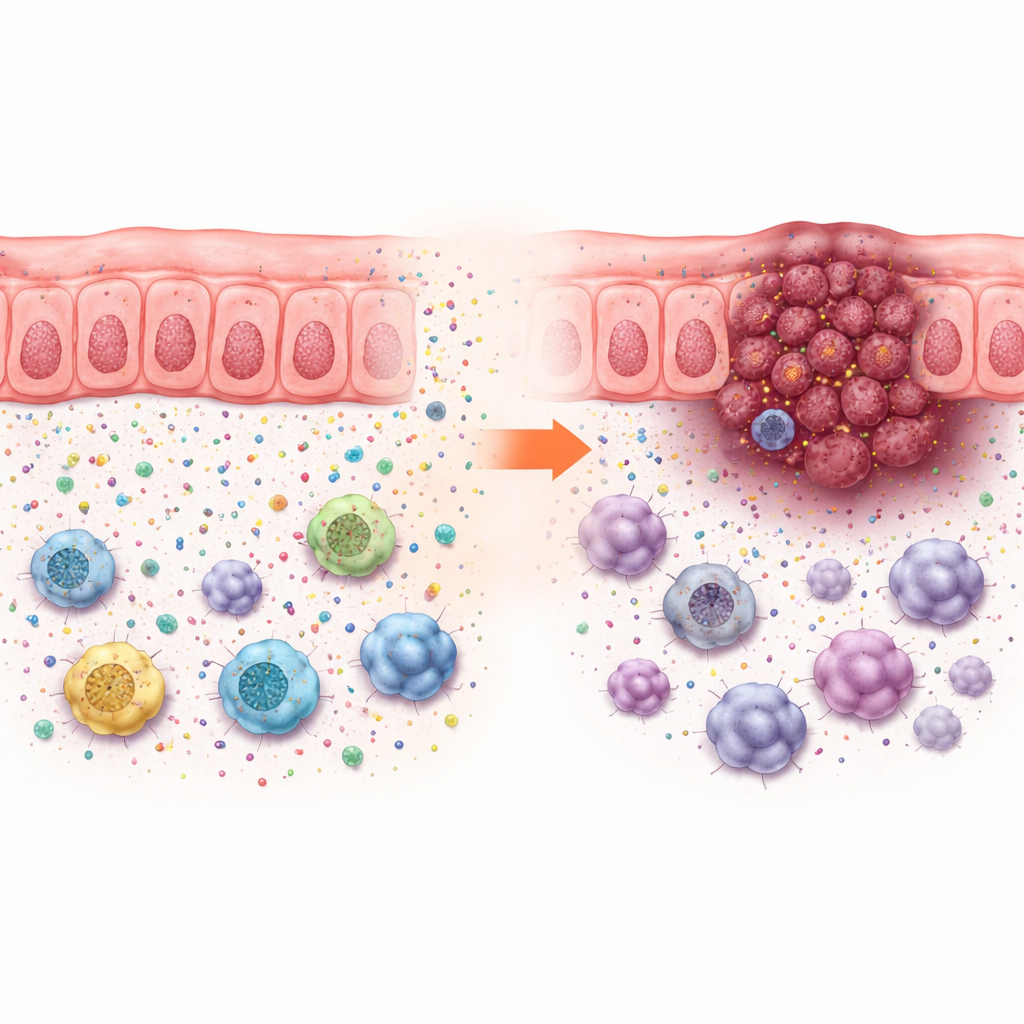
La filtración de ADN mitocondrial como el disparador oculto
¿Qué conecta una enzima de quema de grasas con un sensor inmunitario de ADN? La respuesta está en el ADN mitocondrial (ADNmt). Bajo estrés, fragmentos de ADNmt pueden filtrarse desde las mitocondrias hacia el fluido circundante de la célula, donde cGAS los detecta como una señal de peligro. Los investigadores demostraron que las células cancerosas deficientes en ACADS tenían menos ADNmt en este compartimento, aun cuando el ADNmt total no cambiaba. Bloquear la filtración de ADNmt en células con alto ACADS silenció cGAS–STING, confirmando que estos fragmentos escapados son la alarma crítica. Sorprendentemente, factores clásicos de estrés mitocondrial como especies reactivas de oxígeno, picos de calcio y cambios mayores en la morfología mitocondrial no pudieron explicar completamente la diferencia. En su lugar, el estudio apunta a las “puertas” en la membrana mitocondrial y, más importante, a las marcas químicas sobre el propio ADNmt. 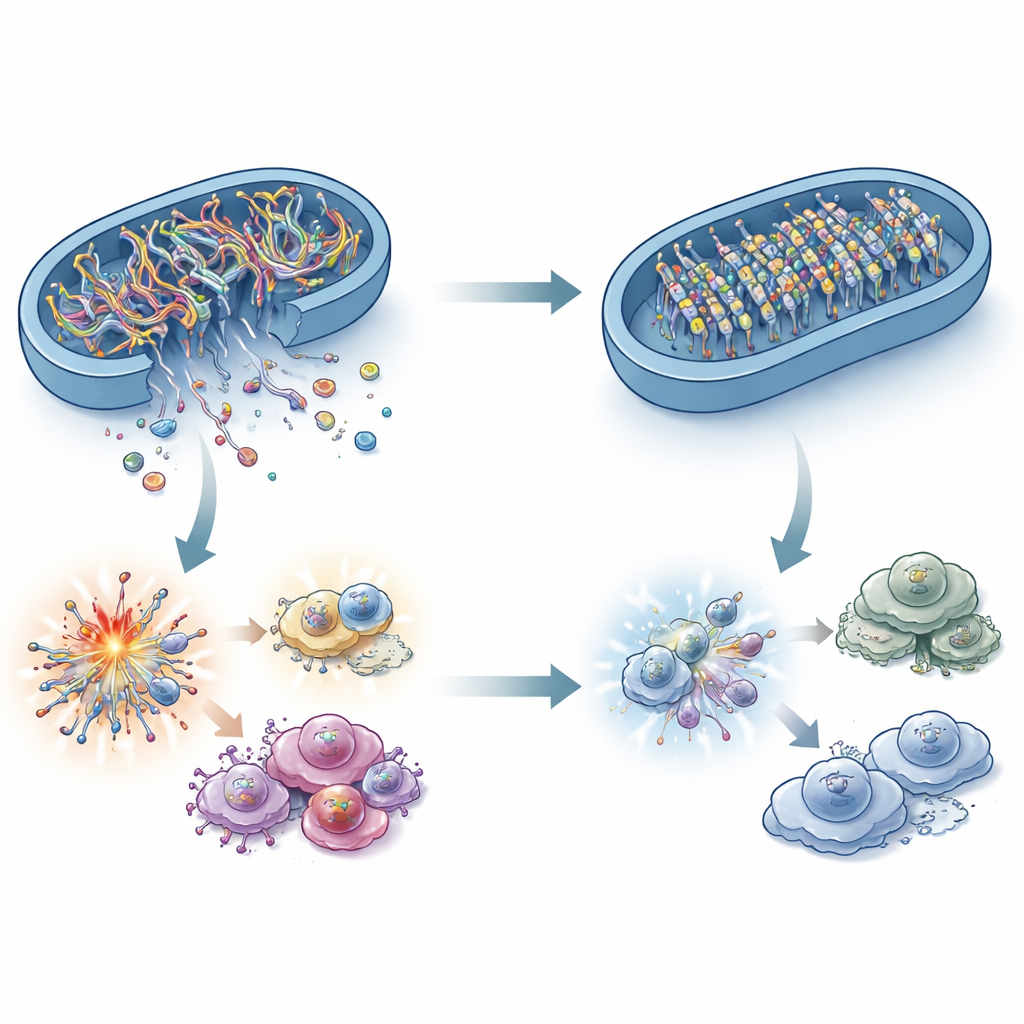
Un compañero metilador del ADN que cierra la alarma
A través de pantallas de interacción proteica, se encontró que ACADS se asocia con una forma de la enzima metiladora del ADN DNMT1 que se localiza en las mitocondrias. Cuando ACADS se perdió, esta DNMT1 mitocondrial se acumuló, colocando grupos metilo adicionales sobre el ADNmt. Estas marcas hacen que el ADNmt sea más estable y menos propenso a romperse y filtrarse. Sobrecargar las células con DNMT1 mitocondrial redujo la fuga de ADNmt, amortiguó la señalización cGAS–STING y aceleró el crecimiento tumoral, mientras que bloquear DNMT1 con el fármaco decitabina restauró la filtración de ADNmt y ralentizó tumores deficientes en ACADS. Las muestras de pacientes reflejaron estos hallazgos: baja ACADS se alineó con alta DNMT1 mitocondrial, señalización STING más débil, menos células T efectoras, más células inmunes supresoras y peores predicciones de respuesta a la inmunoterapia con inhibidores de puntos de control.
Reavivar las defensas inmunitarias con un compuesto antiguo
Para ver si esta vía podía explotarse terapéuticamente, los investigadores usaron cribado por computadora para buscar moléculas que se unan a ACADS. Identificaron la hipericina, un pigmento natural probado anteriormente como tratamiento activado por luz para ciertos linfomas cutáneos. En células de cáncer colorrectal, la hipericina aumentó los niveles de ACADS, redujo la DNMT1 mitocondrial, incrementó la filtración de ADNmt y reactivó la señalización cGAS–STING—cambios que dependieron de la presencia de ACADS. En modelos tumorales de ratón y en cultivos a corto plazo de tumores colorrectales humanos, el tratamiento con hipericina redujo el tamaño de los tumores o desplazó las células inmunes hacia un estado más activo, rico en células T. Aunque hacen falta más trabajos antes del uso clínico, estos resultados sugieren que “reactivar” farmacológicamente ACADS podría ayudar a convertir un tumor frío e inmunosupresor en otro que responda mejor a la inmunoterapia.
Qué significa esto para los pacientes y los tratamientos futuros
En términos sencillos, este trabajo muestra que algunos cánceres colorrectales crecen en parte porque silencian una enzima mitocondrial que normalmente facilita que pequeños fragmentos de ADN se filtren al interior de la célula, donde actúan como bengalas para atraer al sistema inmunitario. Al permitir que un socio metilador del ADN bloquee ese ADN mitocondrial en su lugar, los tumores deficientes en ACADS mantienen esas bengalas ocultas y evitan la detección inmune. Restaurar la actividad de ACADS, por ejemplo con fármacos tipo hipericina, podría reabrir este sistema de alarma mitocondrial, fortalecer la inmunidad antitumoral y mejorar las respuestas a las inmunoterapias existentes. ACADS, la DNMT1 mitocondrial y la actividad de la vía STING pueden por tanto servir como biomarcadores y dianas útiles en la búsqueda de tratamientos más efectivos para el cáncer colorrectal.
Cita: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Palabras clave: cáncer colorrectal, inmunidad tumoral, ADN mitocondrial, metabolismo de lípidos, vía cGAS-STING