Clear Sky Science · es
Atacar a fused in sarcoma (FUS): una nueva estrategia antisentido para tratar la fibrosis pulmonar idiopática
Por qué importan los pulmones cicatrizados
La fibrosis pulmonar idiopática (FPI) es una enfermedad pulmonar implacable en la que los delicados sacos de aire se transforman lentamente en tejido cicatricial rígido, lo que hace que cada respiración sea más difícil. Los fármacos actuales pueden ralentizar esta cicatrización, pero no pueden detenerla ni revertirla. Este estudio explora un nuevo objetivo llamado FUS, una proteína que ayuda a las células a manejar sus mensajes genéticos, y prueba si apagarla con una hebra diseñada de material similar al ADN podría calmar el proceso de cicatrización y ayudar a que los pulmones dañados se reparen.
Un controlador del tráfico celular que falla
FUS es una proteína que normalmente reside en el núcleo celular, donde ayuda a gestionar cómo se procesa y utiliza el ARN —la copia operativa de nuestros genes—. En enfermedades cerebrales como la ELA, FUS puede comportarse mal, abandonar el núcleo, agregarse en las regiones externas de la célula y perturbar la función celular normal. Los autores se preguntaron si un comportamiento similar podría impulsar la cicatrización en la FPI. Estudiaron fibroblastos pulmonares —las células del tejido conectivo que depositan material de cicatriz— de pacientes con FPI y de donantes sanos. En las células de FPI, los niveles de FUS eran mayores en general y, crucialmente, se encontraba mucho más FUS en el citoplasma que en las células sanas. Mediante microscopía electrónica de alta resolución, confirmaron que esta proteína era anormalmente abundante fuera del núcleo, lo que sugiere que su control habitual sobre el ARN podría estar distorsionado en pulmones fibróticos. 
Cómo FUS alimenta a las células cicatriciales
Para ver qué hace realmente esta proteína descontrolada, los investigadores aumentaron FUS en fibroblastos sanos y lo redujeron en fibroblastos de FPI. El exceso de FUS impulsó a las células sanas a dividirse más deprisa, mientras que reducir FUS en las células de FPI ralentizó su crecimiento y su movimiento, dos comportamientos centrales en la formación de cicatrices. El equipo empleó luego una técnica que “congela” las asociaciones proteína‑ARN y lee qué ARNs están ligados a FUS. En los fibroblastos de FPI, se encontró a FUS unido a muchos mensajeros genéticos que promueven la fibrosis, incluidos los que codifican colágeno, factores de crecimiento como TGF‑β y señales inflamatorias. En otras palabras, FUS actuaba como un nodo que conecta toda una red de mensajes pro‑cicatrización.
Silenciar la señal con un fármaco de precisión
El estudio probó un oligonucleótido antisentido llamado ION363 —una hebra corta químicamente modificada diseñada para unirse al ARN de FUS y provocar su destrucción. Cuando los fibroblastos de FPI se trataron con ION363, los niveles de FUS disminuyeron, las células redujeron su proliferación y migración, y los genes clave constructores de cicatriz se silenciaron. Importante: este efecto no dependió de matar las células ni de forzarlas a envejecer; en cambio, pareció reajustar su comportamiento. Cuando el mismo tratamiento se aplicó a cortes finos de tejido pulmonar de FPI mantenidos vivos en el laboratorio, amplios grupos de genes vinculados con la matriz extracelular, la inflamación y el revestimiento epitelial anómalo se atenuaron, mientras que los genes asociados con la producción saludable de surfactante y la función alveolar se reforzaron. El tratamiento también redujo la tinción de colágeno y aumentó marcadores de células de superficie pulmonar funcionales, lo que sugiere un cambio de la cicatrización hacia la reparación.
Ayudar a que los sacos de aire dañados vuelvan a crecer
Dado que las pequeñas células que recubren los alvéolos, conocidas como células alveolares tipo II, son cruciales para la reparación pulmonar, los investigadores construyeron “alveolosferas” tridimensionales a partir de células de pacientes para imitar unidades pulmonares en miniatura. En cultivos de pacientes con FPI, estas estructuras normalmente sobreviven con dificultad. Con el tratamiento con ION363, se formaron más alveolosferas, crecieron más y mostraron mayor actividad lisosomal —un sello de renovación activa. Tinciones detalladas revelaron más células que mostraban marcadores de células maduras intervinientes en el intercambio gaseoso, lo que indica que silenciar FUS no solo calmó a los fibroblastos, sino que también alentó al epitelio lesionado a reconstruir una superficie más saludable. 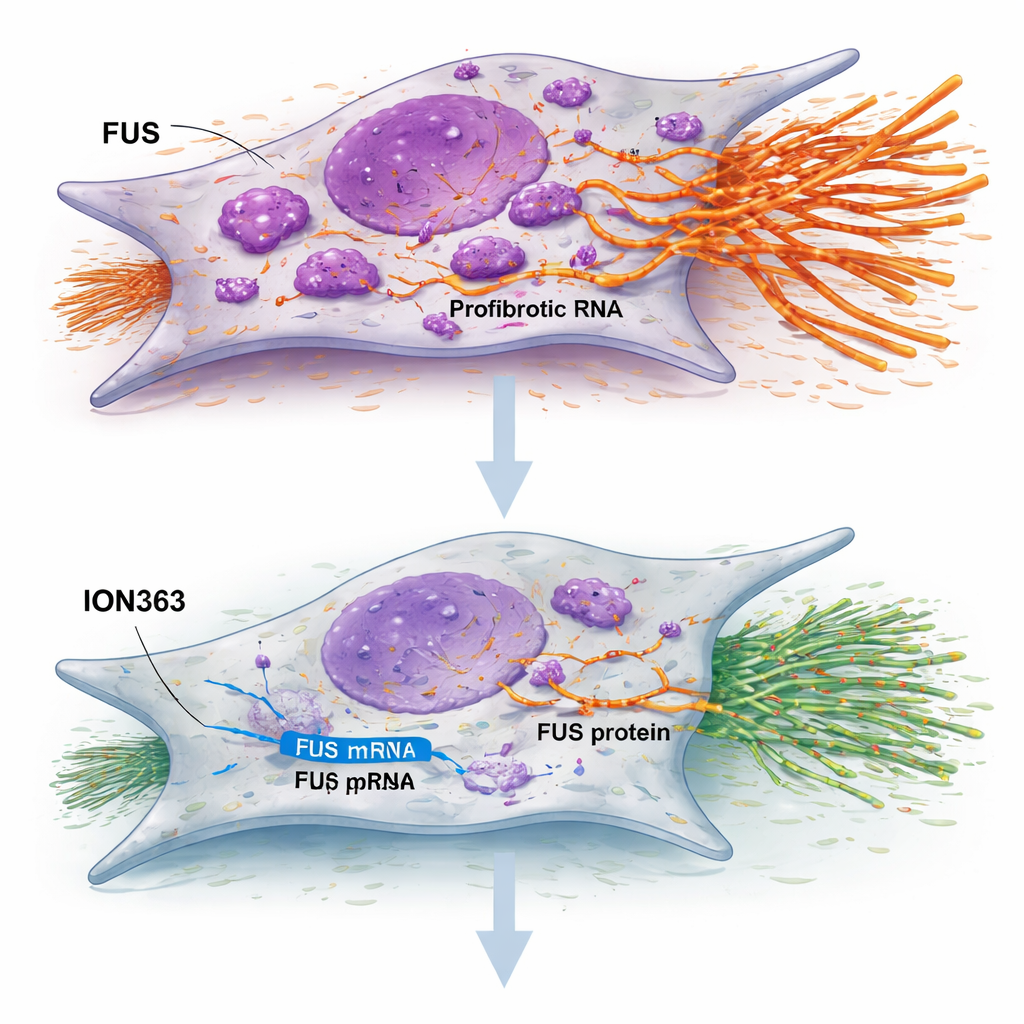
Qué podría significar esto para los pacientes
En conjunto, el trabajo presenta a FUS como un interruptor maestro en la FPI que vincula fibroblastos formadores de cicatriz hiperactivos con la incapacidad de reparar los delicados sacos de aire. Al reducir FUS con un fármaco antisentido dirigido, los investigadores pudieron disminuir los programas génicos profibróticos, aliviar la acumulación de colágeno y promover la regeneración en modelos pulmonares derivados de pacientes. Aunque este enfoque aún está en fase de laboratorio y requerirá pruebas cuidadosas en modelos animales y ensayos clínicos, sugiere que la FPI podría tratarse algún día no solo ralentizando la cicatrización, sino reequilibrando directamente los programas celulares que controlan la lesión y la reparación pulmonar.
Cita: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Palabras clave: fibrosis pulmonar idiopática, oligonucleótido antisentido, proteína FUS, fibrosis pulmonar, reparación alveolar