Clear Sky Science · es
El E7 del virus del papiloma humano 16 potencia la capacidad de las células madre al regular el eje APC2/SPIN4/β-catenina en el cáncer de cuello uterino
Por qué esta investigación importa
El cáncer de cuello uterino sigue siendo una causa importante de mortalidad entre las mujeres en todo el mundo, sobre todo donde el cribado y la vacunación son limitados. Los científicos saben que ciertos tipos del virus del papiloma humano (VPH), en particular el VPH16, son impulsores clave de esta enfermedad, pero todavía se están desentrañando los pasos concretos por los que el virus mantiene a los tumores agresivos y con tendencia a recurrir. Este estudio profundiza en cómo una proteína viral, llamada E7, ayuda a mantener una población pequeña pero poderosa de «células madre cancerosas» que pueden alimentar el crecimiento tumoral, la diseminación y la resistencia al tratamiento, ofreciendo pistas para terapias nuevas y más precisas.
De virus común a cáncer peligroso
La mayoría de las infecciones por VPH se resuelven por sí solas, pero la infección persistente por tipos de alto riesgo puede transformar las células sanas del cuello uterino en cáncer. La proteína viral E7 es central en este proceso: inactiva salvaguardas clave que normalmente mantienen el control de la división celular. Trabajos previos de este grupo de investigación mostraron que el E7 del VPH16 potencia propiedades similares a las de las células madre en células de cáncer cervical, haciéndolas más difíciles de erradicar. En el estudio actual, el equipo se propuso cartografiar las redes génicas controladas por E7 para entender exactamente cómo mantiene vivas y prósperas a estas células peligrosas.
Rastreando el impacto de E7 dentro de las células tumorales
Para seguir la influencia de E7, los investigadores utilizaron líneas celulares de cáncer cervical cultivadas en el laboratorio y redujeron los niveles de E7 con ARN interferente pequeño, una herramienta que silencia temporalmente genes específicos. Después midieron qué genes cambiaban su actividad en todo el genoma. Combinado con esto, realizaron una batería de pruebas funcionales: la velocidad de crecimiento celular, la capacidad de migración e invasión a través de membranas artificiales y la facilidad para formar cúmulos esféricos en cultivo—un rasgo distintivo de las células madre cancerosas. También examinaron tumores crecidos en ratones y analizaron grandes conjuntos de datos públicos de cáncer para ver cómo sus hallazgos coincidían con los patrones en muestras de pacientes.
Un papel sorprendente para una vía conocida
Los experimentos de mapeo génico apuntaron con fuerza a la vía Wnt/β-catenina, un regulador bien conocido de las células madre normales y de numerosos cánceres. Cuando se silenciaba E7, los niveles de β-catenina disminuían, lo que sugiere que esta vía quedaba desactivada. Al mismo tiempo, el equipo observó cambios importantes en un gen llamado APC2. En muchos otros cánceres, las proteínas relacionadas con APC actúan como frenos sobre la señalización Wnt, ayudando a controlar el crecimiento celular. Aquí, sin embargo, las células de cáncer cervical parecían usar APC2 de manera inesperada: cuando APC2 se reducía, las células cancerosas crecían más lentamente, tenían menor capacidad de moverse e invadir y perdían rasgos de tipo madre. En ratones, los tumores con silenciamiento prolongado de APC2 eran mucho más pequeños, y aun así los animales se mantenían sanos, lo que sugiere una posible ventana terapéutica segura.
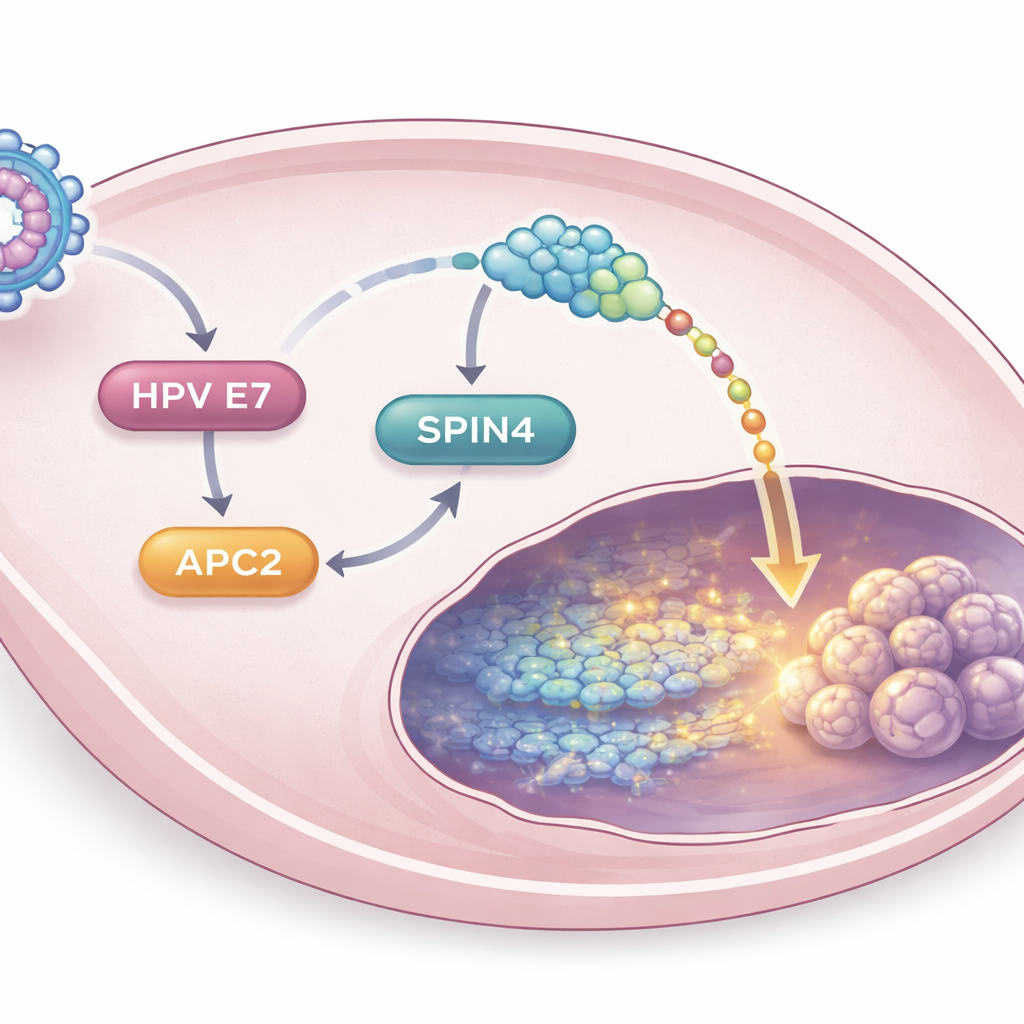
Descubriendo una nueva cadena promotora del cáncer
Al profundizar, los científicos demostraron que el E7 del VPH16 aumenta los niveles de APC2 de forma indirecta a través de otra proteína llamada E2F1, que ayuda a activar conjuntos de genes relacionados con el crecimiento. Una vez elevado, APC2 a su vez potencia la actividad de una proteína menos conocida llamada SPIN4. El análisis de datos de tumores humanos reveló que SPIN4 es más abundante en cánceres cervicales que en tejido normal, y que sus niveles elevados se asocian con una supervivencia peor. En el laboratorio, apagar SPIN4 atenuó la capacidad de APC2 para impulsar el crecimiento celular, la invasión, la actividad Wnt/β-catenina y el comportamiento tipo célula madre cancerosa. En experimentos en ratones, los tumores sin SPIN4 eran más pequeños y mostraban marcadores reducidos asociados a la pluripotencia. En conjunto, estos hallazgos delinean una cadena escalonada—VPH16 E7 a APC2 a SPIN4 a Wnt/β-catenina—que colectivamente mantiene a las células del cáncer cervical agresivas y con rasgos de célula madre.
Mirando hacia tratamientos más inteligentes
Para quienes no son especialistas, el mensaje clave es que este estudio identifica un diagrama de cableado interno hasta ahora no reconocido en los cánceres cervicales impulsados por VPH. En lugar de actuar como un simple interruptor, la proteína viral E7 secuestra una serie específica de proteínas del huésped—APC2 y SPIN4—para mantener un reservorio peligroso de células madre tumorales vivo mediante la vía Wnt/β-catenina. Este eje no solo ayuda a explicar por qué algunos tumores son tan persistentes, sino que también destaca varios objetivos nuevos a los que podrían dirigirse fármacos o terapias combinadas, especialmente en pacientes cuyos cánceres resisten el tratamiento estándar. Al centrarse en la circuitería moldeada por el virus que sostiene a las células «semilla» del tumor, las terapias futuras podrían ser más efectivas para prevenir la reaparición y mejorar los resultados a largo plazo.
Cita: Shen, T., Ma, Y., Wu, T. et al. Human papillomavirus16 E7 enhances cell stemness by regulating the APC2/SPIN4/β-catenin axis in cervical cancer. Oncogenesis 15, 10 (2026). https://doi.org/10.1038/s41389-026-00602-8
Palabras clave: cáncer de cuello uterino, virus del papiloma humano, células madre cancerosas, vía Wnt beta-catenina, señalización oncogénica