Clear Sky Science · es
Truncamiento parcial del dominio C-terminal de PTCH1 en el cáncer promueve la tumorogénesis mediante la activación no canónica de un bucle GLI-PI3K
Por qué un pequeño cambio proteico importa en el cáncer de colon
El cáncer de colon suele surgir por una acumulación lenta de errores genéticos. Este estudio se centra en una alteración sorprendentemente pequeña en una proteína de la superficie celular llamada PTCH1 y muestra cómo recortar parte de su cola puede ayudar a las células de cáncer de colon a crecer más rápido, diseminarse con mayor facilidad y, potencialmente, resistir algunos fármacos existentes. Comprender este interruptor oculto de crecimiento podría abrir la puerta a tratamientos nuevos y más precisos para un subconjunto de pacientes.
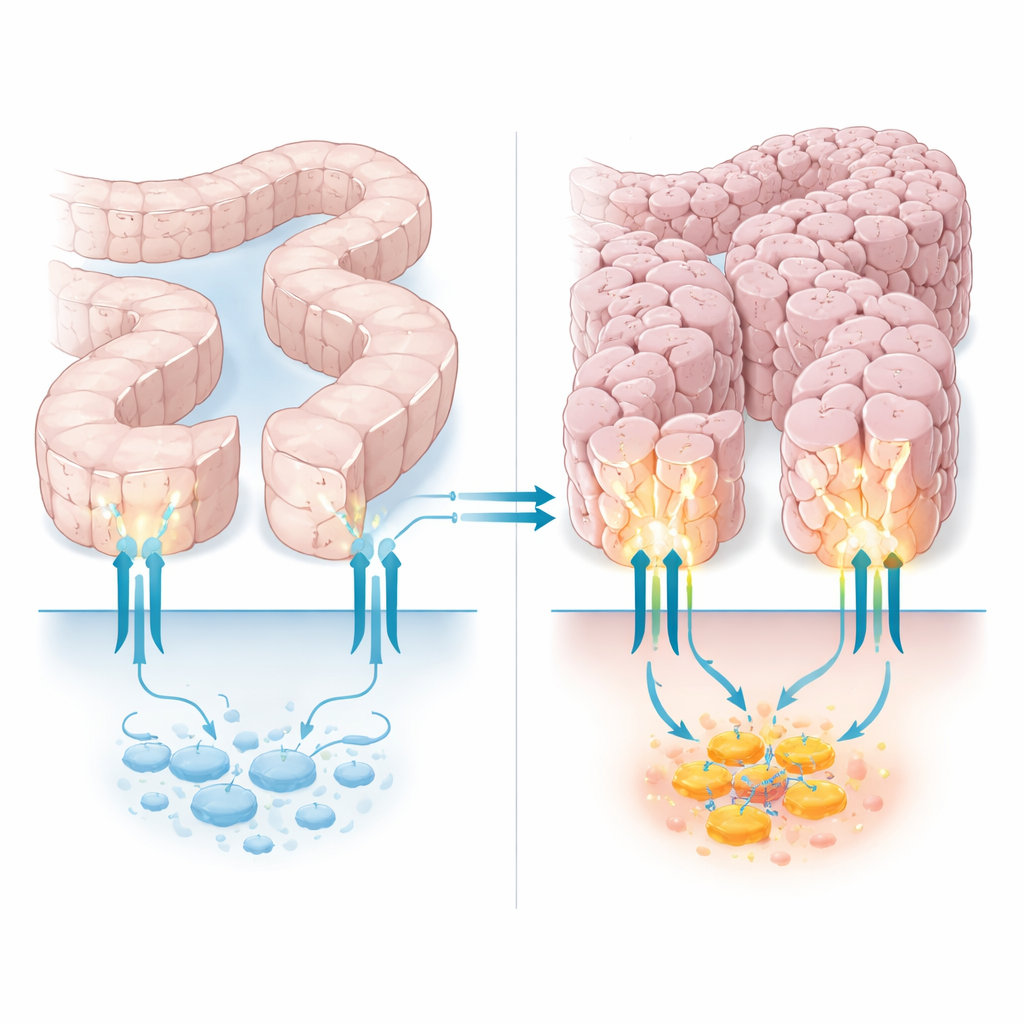
El guardián de la célula con un trabajo secundario escondido
PTCH1 es más conocido como el guardián de la vía Hedgehog, una vía de comunicación que usan las células durante el desarrollo y la reparación tisular. En su papel clásico, PTCH1 mantiene bajo control a una proteína compañera, Smoothened, y de ese modo regula a una familia de controladores del ADN llamados GLI. Pero PTCH1 también tiene una cola larga y flexible que cuelga dentro de la célula, actuando como una tira de acoplamiento para otras proteínas que influyen en la muerte celular, el reciclaje de componentes celulares y más. Trabajos anteriores mostraron que algunos cánceres de colon, estómago y útero llevan mutaciones que cortan parte de esta cola interna. Esas mutaciones no parecían romper el interruptor Hedgehog clásico, pero sí mejoraban la capacidad de las células cancerosas para sobrevivir al estrés, lo que sugiere que este segmento de la cola contribuye silenciosamente al papel supresor de tumores de PTCH1.
Ingeniería de células cancerosas para probar el impacto
Para ver qué hacen realmente estas mutaciones que acortan la cola, los investigadores usaron edición genética CRISPR/Cas9 para recrearlas en una línea celular de cáncer de colon. Compararon dos clones editados, cada uno con una truncación distinta en la cola de PTCH1, con células idénticas que conservaban PTCH1 normal. Las células mutantes se dividieron más rápido, formaron muchas más colonias y prosperaron incluso cuando tuvieron que crecer sin adhesión—un comportamiento vinculado a la capacidad de diseminarse en el organismo. Al implantarlas en ratones, las células con la cola truncada produjeron tumores mucho más grandes en pocas semanas, con más células en fase de división. Es importante que las células editadas aún producían PTCH1 y mantenían su función protectora principal, lo que demuestra que la agresividad adicional proviene de perder las funciones internas especializadas de la cola y no de eliminar PTCH1 por completo.
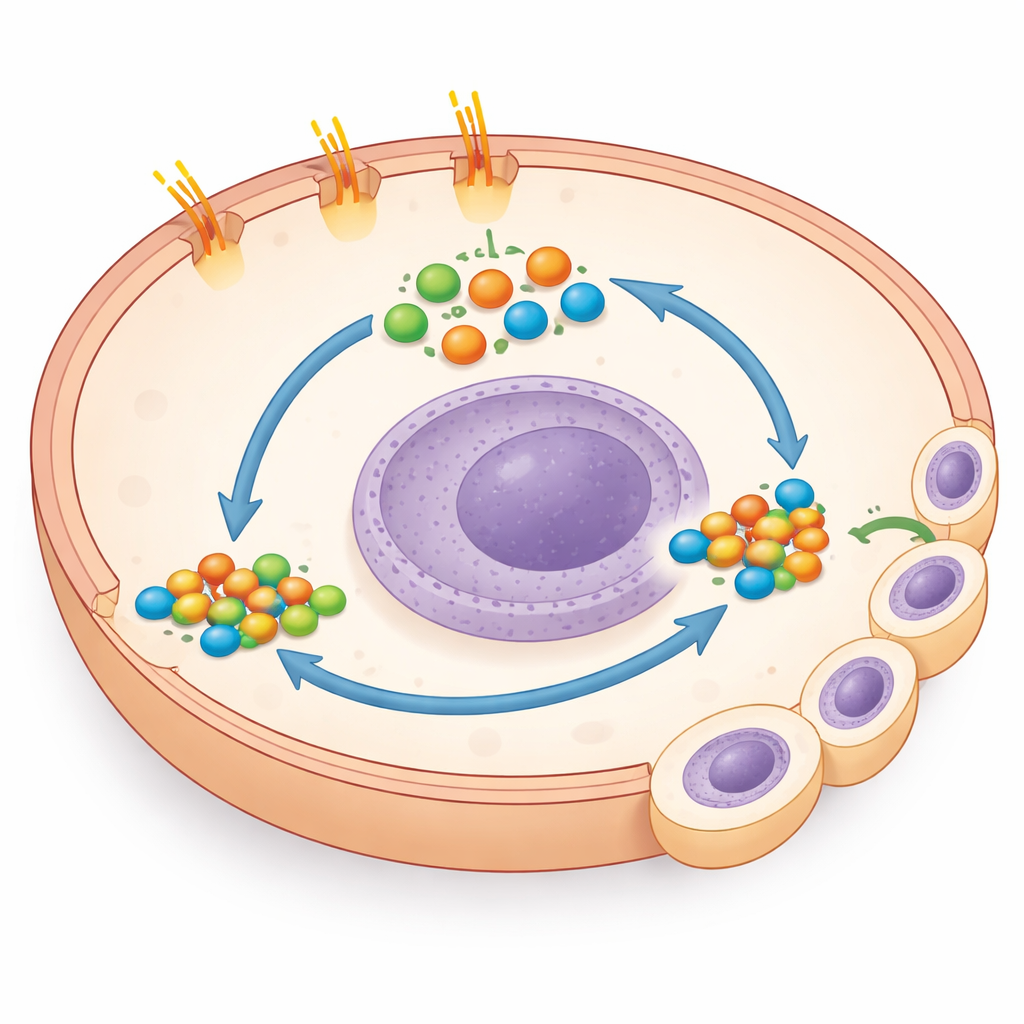
Un atajo sorprendente hacia un potente interruptor de crecimiento
Al profundizar en la biología subyacente, el equipo hizo un hallazgo inesperado: las células con la cola truncada mostraron niveles muy aumentados de GLI1 y GLI2, conductores clave de programas génicos que promueven el crecimiento y la supervivencia. Normalmente, la actividad de GLI aumenta cuando Smoothened queda liberado, pero bloquear Smoothened no tuvo efecto aquí. En cambio, bloquear directamente GLI con una pequeña molécula, o reducir GLI1 con herramientas genéticas, redujo drásticamente el crecimiento de las células mutantes en cultivo y en otras líneas celulares de cáncer de colon que de forma natural portan mutaciones en la cola de PTCH1. Esto mostró que la pérdida de la cola activa a GLI mediante una vía “no canónica” que elude el interruptor Hedgehog habitual, y que las células cancerosas pasan a depender en gran medida de este atajo para su comportamiento agresivo.
Se encienden múltiples circuitos de crecimiento, pero uno domina
Al secuenciar el ARN de las células, los investigadores encontraron miles de genes cuya actividad cambia cuando se trunca la cola de PTCH1. Muchos pertenecían a circuitos conocidos en el cáncer, incluidos los controlados por el receptor del factor de crecimiento epidérmico (EGFR), Ras y sistemas de señalización que regulan el metabolismo celular y propiedades similares a las de células madre. Las células mutantes mostraron mayor actividad de EGFR y de sus ligandos y una mayor señalización en dos rutas descendentes principales: las vías MAPK y PI3K/Akt. Sin embargo, cuando los científicos bloquearon EGFR o su rama MAPK, las células mutantes solo se ralentizaron parcialmente. En contraste, dosis bajas de inhibidores de PI3K limitaron firmemente su crecimiento y formación de colonias y redujeron los niveles de GLI1, subrayando a PI3K/Akt como un socio crítico en este nuevo mecanismo de activación de GLI.
Un bucle auto-reforzante que alimenta el crecimiento tumoral
Experimentos adicionales revelaron un ciclo de retroalimentación: truncar la cola de PTCH1 aumenta la actividad de GLI; GLI, a su vez, ayuda a mantener alta la señalización PI3K/Akt; y PI3K/Akt contribuye a estabilizar y activar GLI. Interrumpir ya sea GLI o PI3K rompía este bucle y despojaba a las células mutantes de su ventaja de crecimiento, mientras que simplemente aumentar PI3K/Akt no podía superar el bloqueo directo de GLI. Las células también mostraron una actividad reducida de PKA, una enzima que normalmente marca a las proteínas GLI para su inactivación, lo que probablemente inclina aún más la balanza hacia los programas impulsados por GLI.
Qué puede significar esto para futuros tratamientos
Para los pacientes, el mensaje clave es que algunos cánceres de colon llevan mutaciones en la cola de PTCH1 que conectan silenciosamente un bucle de realimentación positivo GLI–PI3K, ayudando a los tumores a crecer y a evadir fármacos que apuntan al interruptor Hedgehog más familiar o a la vía EGFR–MAPK. Estos tumores pueden, en cambio, ser especialmente vulnerables a tratamientos que inhiban GLI directamente o que actúen sobre PI3K/Akt. El trabajo sugiere que secuenciar PTCH1 en tumores de colon—especialmente en aquellos del lado derecho del colon, donde tales mutaciones son más frecuentes—podría ayudar a identificar a los pacientes que podrían beneficiarse de estrategias dirigidas a PI3K o GLI, convirtiendo un recorte proteico sutil en una pista terapéutica útil.
Cita: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Palabras clave: cáncer de colon, señalización Hedgehog, mutaciones de PTCH1, factores de transcripción GLI, vía PI3K Akt