Clear Sky Science · de
Multimodale Sensortechnologien für die HPAI-Biosurveillance in Geflügelproduktionssystemen
Warum Vogelgrippe auf Bauernhöfen uns alle betrifft
Hochpathogene aviäre Influenza, oft HPAI oder Vogelgrippe genannt, ist nicht mehr nur ein Problem für Hühner auf entfernten Farmen. Jüngste Wellen des H5N1-Stamms haben in den Vereinigten Staaten mehr als 168 Millionen Vögel ausgelöscht, die Eierpreise stark ansteigen lassen und sind sogar auf Milchkühe und Menschen übergesprungen. Dieser Übersichtsartikel erklärt, wie neue „smarte“ Sensortechnologien – das Lauschen auf Tiergeräusche, das Probenahmen von Stallluft und schnelle genetische Tests vor Ort – Ausbrüche früher erkennen, die Nahrungsmittelversorgung schützen und das Risiko verringern könnten, dass ein gefährliches Grippevirus sich so anpasst, dass es leicht unter Menschen übertragbar wird.
Die wachsende Bedrohung auf Farmen und beim Menschen
In den vergangenen Jahren hat sich ein neuer Zweig des H5N1-Virus (Klade 2.3.4.4b) weit in der US-Geflügelpopulation und neuerdings auch in Milchviehbeständen ausgebreitet. Jeder Ausbruch zwingt Landwirtinnen und Landwirte, ganze Bestände zu vernichten, verursacht Verluste von über 1,4 Milliarden Dollar und führt zu plötzlichen Einbrüchen bei Eier- und Fleischlieferungen. Zugleich wurden in den USA mehr als 70 Menschinfektionen registriert, meist bei geringverdienenden Beschäftigten, die infizierte Tiere handhaben und oft nur eingeschränkten Zugang zu Gesundheitsversorgung haben. Karten und Überwachungsdaten zeigen, dass Wellen von H5N1 bei Vögeln häufig mit den üblichen winterlichen Spitzen der saisonalen Grippe beim Menschen zusammenfallen, wodurch an der Grenze zwischen Tier und Mensch ein gemeinsames Risikoumfeld entsteht. Diese Überschneidung macht es besonders wichtig, zu verfolgen, was in Ställen und auf Weiden sowie in Kliniken geschieht.
Wie dieses Virus funktioniert und warum es sich so leicht ausbreitet
Aviäre Influenzaviren sind kleine, umhüllte Partikel, die ihr genetisches Material in acht separaten RNA-Segmenten tragen. Zwei Oberflächenproteine, Hämagglutinin (H) und Neuraminidase (N), führen zu vertrauten Bezeichnungen wie H5N1 oder H3N2 und bestimmen, welche Wirte das Virus infizieren kann und wie schwer die Erkrankung ausfällt. Niedrigpathogene Stämme bleiben meist im Darm und den Atemwegen von Vögeln und verursachen oft wenige sichtbare Anzeichen. Im Gegensatz dazu besitzen hochpathogene Stämme wie das heutige H5N1 eine spezielle „Spaltstelle“ am H-Protein, die dem Virus erlaubt, sich im gesamten Körper zu vermehren, was zu einem plötzlichen Tod bei bis zu 90–100 % der betroffenen Vögel führen kann. Das segmentierte Genom erleichtert es außerdem, dass Influenzaviren verschiedener Wirte Stücke austauschen und sich weiterentwickeln, weshalb Kreuzinfektionen in Rindern, Katzen oder Wildtieren so besorgniserregend sind: Jeder neue Wirt ist eine Gelegenheit für das Virus, sich zu verändern.
Grenzen der heutigen Biosicherheit und Tests
Geflügelbetriebe halten bereits strenge Biosicherheitsregeln ein, darunter kontrollierten Zugang, Desinfektion und visuelle Gesundheitskontrollen. Dennoch sind große HPAI-Ausbrüche selbst auf Farmen aufgetreten, die diese Standards erfüllen. Ein Grund ist die Geschwindigkeit: Traditionelle Überwachung beruht darauf, kranke Vögel zu bemerken, Abstriche zu nehmen und diese an ein entferntes Labor zur PCR-Testung zu schicken – ein Verfahren, das zwei bis drei Tage dauern kann. Da H5N1 einen Bestand in etwa 48 Stunden töten kann, lässt diese Verzögerung ein Zeitfenster, in dem das Virus durch Ställe fegen und zwischen Betrieben verbreitet werden kann. Ausreichend viele Vögel aus riesigen Beständen zu beproben ist außerdem schwierig, und routinemäßige Protokolle testen selten Staub, Wasser oder Oberflächen, auf denen das Virus unbemerkt verweilen kann. Daher entgehen frühe Infektionen, milde Fälle und niedrige Kontaminationsniveaus oft den Abwehrmaßnahmen.
Hören, Riechen und Sehen: Neue Wege, Ausbrüche zu erkennen
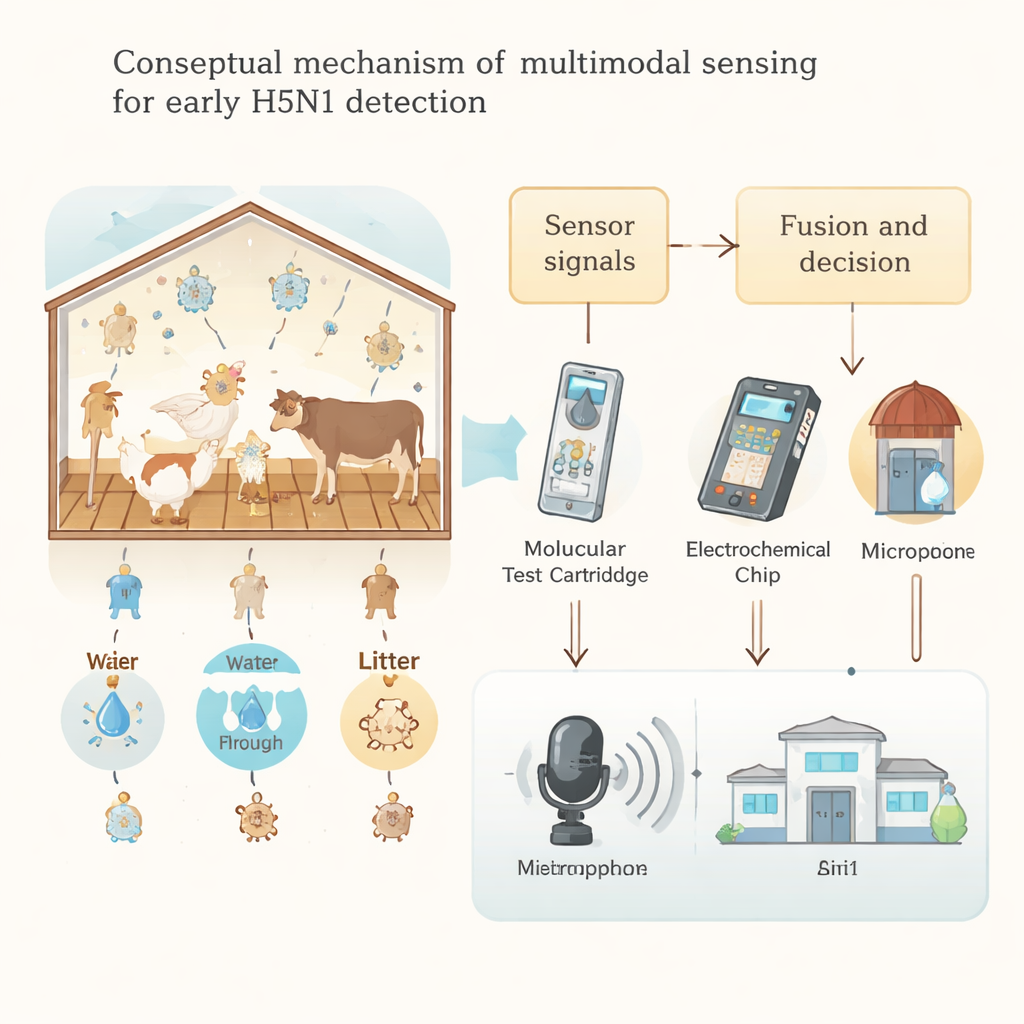
Die Autoren argumentieren, dass Farmen multimodale Sensorik benötigen – mehrere, sich ergänzende Wege, um nach Problemen zu suchen. Auf der zielgerichteten Seite stehen Werkzeuge, die direkt nach dem Virus oder seinen Bestandteilen suchen: tragbare Methoden, die virale RNA bei konstanter Temperatur verstärken, programmierbare CRISPR-basierte Tests, die Ergebnisse in unter einer Stunde liefern, sowie kompakte elektrochemische und optische Biosensoren, die virale Proteine in Luft, Wasser oder Abstrichen nachweisen können. Auf der nicht-zielgerichteten Seite gibt es Methoden, die allgemeine Krankheitszeichen erkennen, ohne sich für das verantwortliche Mikroorganismus zu interessieren, wie Thermalkameras zur Fiebersuche, Lasergeräte, die chemische Fingerabdrücke aus Stallstaub lesen, und Mikrofonsysteme, die die Klangmuster gesunder und kranker Bestände erlernen. Beispielsweise können Deep-Learning-Modelle subtile Veränderungen in Hühnerstimmen ein bis zwei Tage vor offensichtlicher Krankheit erkennen, während fortgeschrittene Lichtstreuungsverfahren virusbezogene Moleküle in Aerosolen, vermischt mit gewöhnlichem Stallstaub, unterscheiden können.
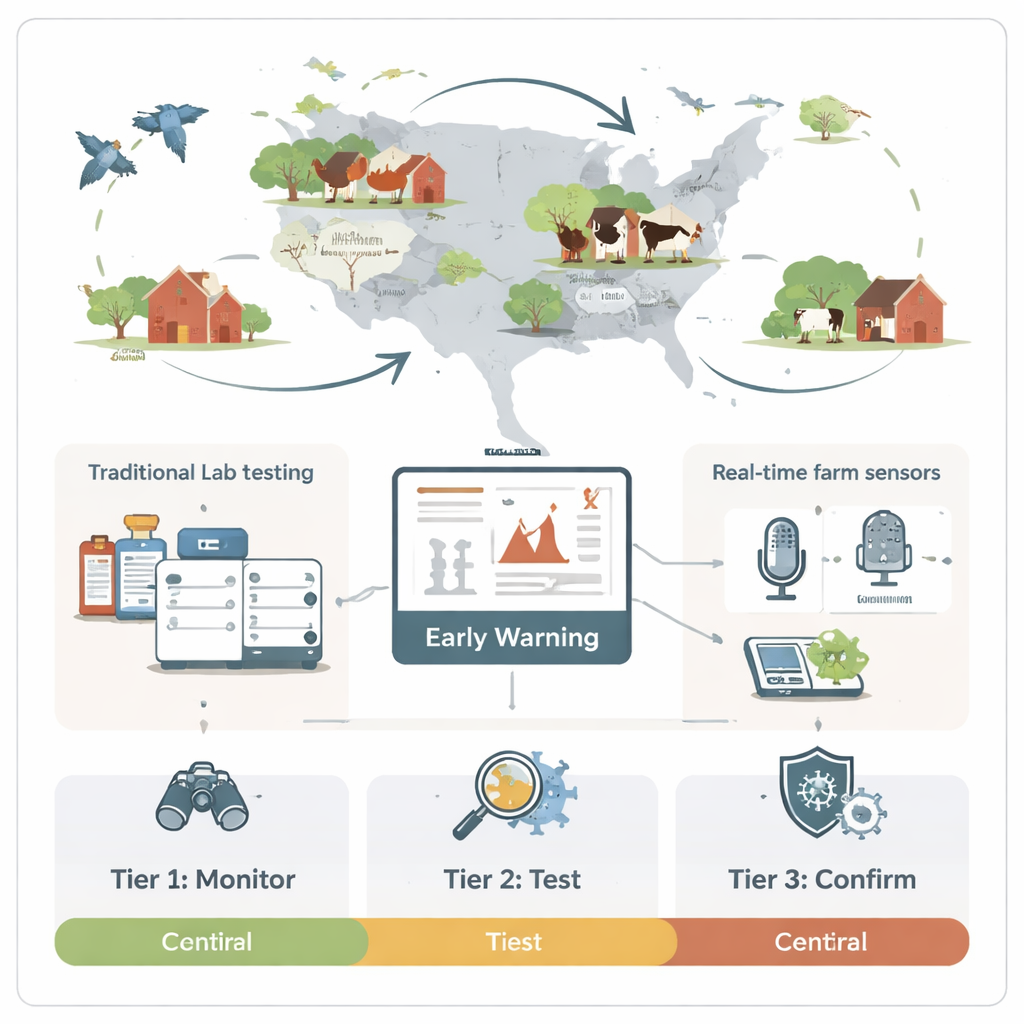
Aufbau eines gestuften Frühwarnsystems
Statt alle Werkzeuge überall einzusetzen, schlägt die Übersichtsarbeit ein dreistufiges System vor. In Stufe 1 laufen kostengünstige Sensoren kontinuierlich im Hintergrund, lauschen nach ungewöhnlichem Husten, überwachen luftgetragene Partikel oder scannen Staub nach verdächtigen chemischen Signaturen. Überschreiten diese breit angelegten Alarme eine Schwelle, schaltet Stufe 2 ein: schnelle molekulare Vor-Ort-Tests und Biosensoren prüfen gezielte Proben wie Luftkonzentrate oder Abstriche, typischerweise innerhalb von 30–60 Minuten. Erst wenn diese schnelleren Screenings echte Gefahr anzeigen, beginnt Stufe 3 mit bestätigenden Labortests wie umfassenden PCR-Panels oder Virusisolierungen, die einen Tag oder länger dauern. Dieser schrittweise Ansatz balanciert Geschwindigkeit und Zuverlässigkeit, reduziert Panik durch Fehlalarme und gewinnt dennoch im Vergleich zum Warten auf tote Vögel oder sichtbar erkrankte Arbeiter wertvolle Zeit.
Was das für Lebensmittelsicherheit und Gesundheit bedeutet
Kurz gesagt kommt der Artikel zu dem Schluss, dass der Kampf gegen moderne Vogelgrippe erfordert, dass Farmen sich mehr wie intelligente Fabriken und weniger wie isolierte Schuppen verhalten. Indem man Ohren (akustische Überwachung), Nasen (chemische und molekulare Sensoren) und Gehirne (Datenfusionsalgorithmen) über Tier-, Umwelt- und Gesundheitssektoren hinweg kombiniert, kann die Landwirtschaft vom Reagieren auf Katastrophen zum Vorhersehen übergehen. Früherer Nachweis bedeutet weniger großflächige Keulung, stabilere Preise für Eier, Fleisch und Milch und geringere Chancen, dass H5N1 die richtigen Mutationen aufnimmt, um eine menschliche Pandemie zu starten. Es gibt weiterhin Hürden – Technologiekosten, der Bedarf an Schulung der Arbeitskräfte und die Herausforderung, laute Daten aus sehr unterschiedlichen Sensoren zu kombinieren – doch multimodale Sensorik bietet einen realistischen Weg zu sichereren Farmen und einer stärkeren One-Health-Überwachung für alle.
Zitation: Ali, M.A., Ataei Kachouei, M., Jacobs, L. et al. Multimodal sensing technologies for HPAI biosurveillance in poultry production systems. npj Biosensing 3, 11 (2026). https://doi.org/10.1038/s44328-025-00075-6
Schlüsselwörter: Vogelgrippe, Biosensoren, Hofüberwachung, CRISPR-Diagnostik, akustische Überwachung