Clear Sky Science · de
Percutane Nephrostomie‑Führung durch ein auf Faltungsnetzen basierendes Optical‑Coherence‑Tomography‑Endoskop
Warum sicherer Nierenzugang wichtig ist
Die Nierenstein‑Erkrankung wird häufiger, und viele Patientinnen und Patienten benötigen einen kleinen Schlauch, der direkt in die Niere gelegt wird, um Urin abzuleiten oder Steine zu entfernen. Dieses Verfahren, perkutane Nephrostomie genannt, erfolgt durch das Einführen einer Nadel vom Rücken der Patientin bzw. des Patienten in das Hohlrauminnere der Niere. Obwohl die Punktion winzig ist, kann ein falscher Weg empfindliche Nierenstrukturen einreißen oder Blutgefäße beschädigen, was zu Blutungen und anderen Komplikationen führt. Diese Studie stellt eine neue hochauflösende Bildsonde vor, gekoppelt mit künstlicher Intelligenz, die in der Nadelspritze sitzt, um Ärzten zu helfen, genau zu sehen, wohin sie stechen, und Schäden zu vermeiden.
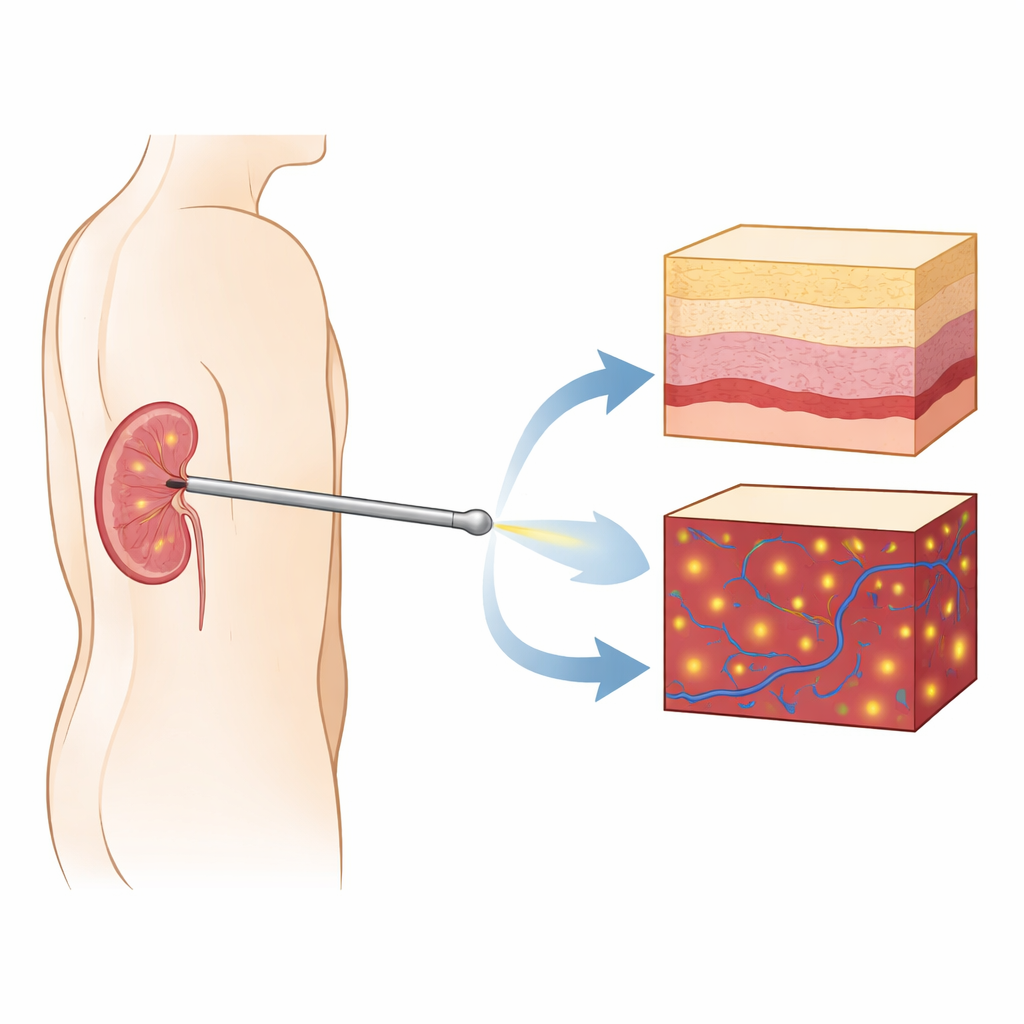
Eine winzige Kamera in der Nadel
Die Forscher bauten eine frontblickende Bildsonde auf Basis der optischen Kohärenztomographie (OCT), einer lichtbasierten Methode, die Querschnitts‑„Schnitte“ von Gewebe in Mikrometerauflösung erfassen kann — etwa zehnmal feiner als herkömmlicher medizinischer Ultraschall. Sie integrierten eine dünne Gradientenindexlinse in eine standardmäßige Nephrostomie‑Nadel, sodass die Sonde während des Einführens direkt vor sich in die Niere blicken kann. Anders als normale Endoskope, die vorwiegend Oberflächenansichten liefern, erzeugt dieses System tiefenaufgelöste Bilder und zeigt, wie sich die Gewebestruktur unter der Spitze verändert. Dieselbe Sonde kann zudem im Doppler‑Modus betrieben werden, der bewegte rote Blutkörperchen hervorhebt und so Blutgefäße vor der Nadel sichtbar macht, bevor sie durchstochen werden.
Erkennung von Nierenschichten in Echtzeit
Um zu prüfen, ob das System verschiedene Nierengewebe unterscheiden kann, führten die Forschenden Experimente an 31 gespendeten menschlichen Nieren unter nahezu normalen Bedingungen durch. In realen Eingriffen sollte die Nadel durch die äußere Rinde (Cortex) und das innere Mark (Medulla) führen, dann in eine kelchförmige Region, den Calyx, und schließlich in das zentrale Harnsammlungsbecken (Pelvis) eintreten. Ein Abweichen vom Kurs birgt das Risiko, durch fettgefüllte Zwischenräume zu laufen und dünne Wände zu verletzen. Die Forscher brachten die Sonde systematisch an fünf Gewebearten an — Cortex, Medulla, Calyx, Sinus‑Fett und Pelvis — und erfassten Millionen von OCT‑Bildern, die ihre charakteristischen Muster zeigten. Beispielsweise wirkten Cortex und Medulla glatt, unterschieden sich jedoch in der Tiefe; der Calyx zeigte streifenartige Übergänge; Sinus‑Fett erzeugte helle, gesprenkelte Netzwerke; und das Pelvis erschien als leerer Raum unter der Sonde.
Ein intelligentes System anlernen, Gefahren zu erkennen
Da menschliche Expertinnen und Experten Zeit und Schulung bräuchten, um diese neuen Bilder während einer Operation zu interpretieren, wandte sich das Team dem Deep Learning zu. Sie trainierten mehrere Faltungsnetzwerke (Convolutional Neural Networks), um jedes OCT‑Frame einer der fünf Gewebearten zuzuordnen, und wählten schließlich eine Architektur namens Inception als besten Performer. In internen Tests identifizierte dieses Modell Gewebe mit einer Genauigkeit von etwa 99,6 % korrekt und behielt auch bei zusätzlichen, ihm zuvor unbekannten Nieren eine hohe Leistung bei. In einer separaten Aufgabe nutzten sie ein anderes Netzwerkdesign, nnU‑Net, um Blutgefäße in Doppler‑OCT‑Bildern zu segmentieren. Dieses Modell lernte, strömendes Blut vom Hintergrundgewebe zu unterscheiden, mit sehr hoher Übereinstimmung gegenüber von Experten manuell gezeichneten Labels — selbst für Gefäße kleiner als 0,2 Millimeter, die mit Standardwerkzeugen schwer zu sehen sind.
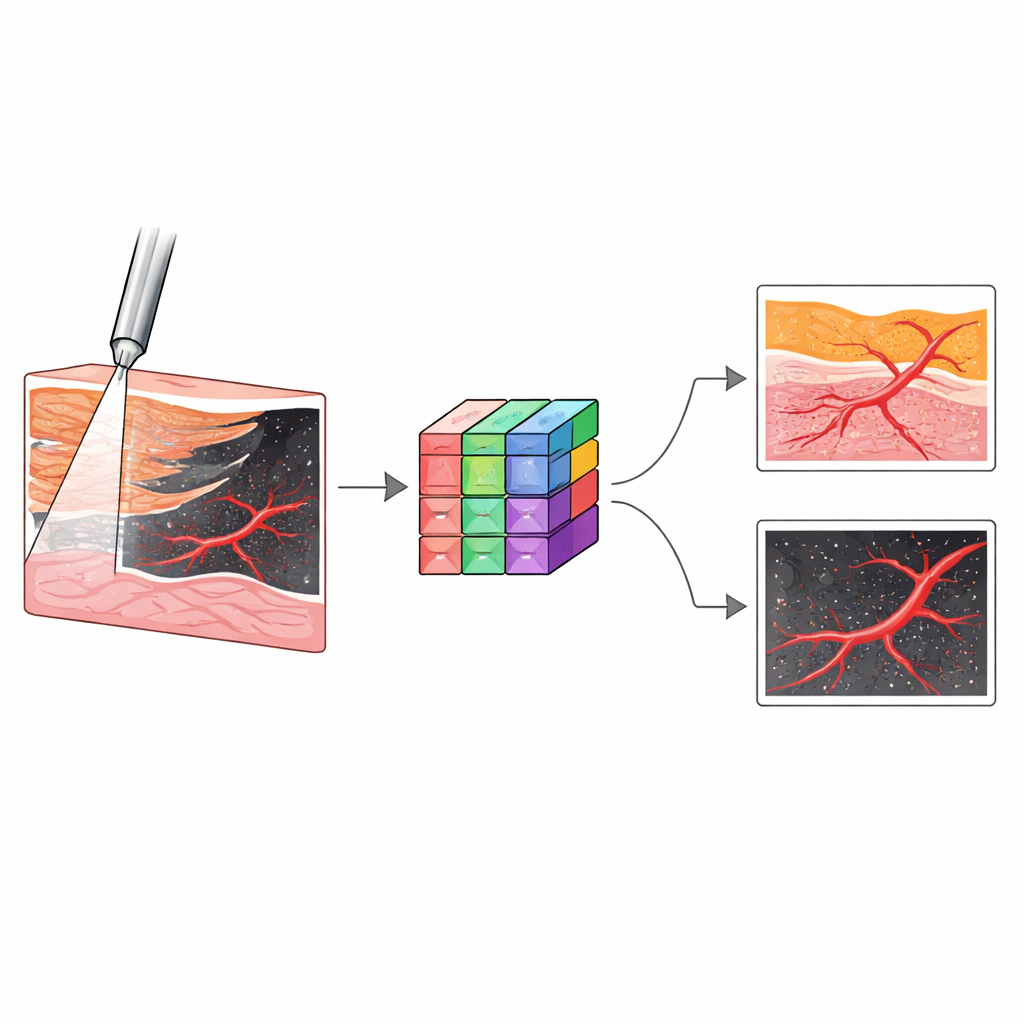
Wie es sich mit heutigen Werkzeugen vergleicht
Derzeit verlassen sich Ärztinnen und Ärzte in der Regel auf Ultraschall oder strahlenbasierte Durchleuchtung (Fluoroskopie), um Nephrostomie‑Nadeln zu führen. Diese Techniken zeigen die Gesamtposition der Niere und den allgemeinen Verlauf der Nadel, aber ihre vergleichsweise grobe Auflösung macht es schwer zu erkennen, welches Gewebe sich genau an der Spitze befindet oder wie nah ein Blutgefäß liegt. In Kontrollversuchen taten sich erfahrene Radiologen mit strukturellem und Doppler‑Ultraschall schwer, das präzise Gewebe an der Nadelspritze zu identifizieren, und konnten winzige Gefäße nicht zuverlässig darstellen. Im Gegensatz dazu bot das OCT‑System eine detaillierte lokale Ansicht plus eine automatisierte Analyse, die auf modernen Grafikprozessoren in einem Bruchteil einer Sekunde läuft — schnell genug, um während des Fortschreitens der Nadel Feedback zu geben.
Was das für Patientinnen und Patienten bedeuten könnte
Die Studie legt nahe, dass die Kombination einer nadelmontierten OCT‑Sonde mit Deep Learning Nierenzugangsverfahren sicherer und effizienter machen könnte. Künftig könnte eine Ärztin oder ein Arzt die übliche Nadel mit eingebauter Sonde einführen, feinstrukturierte Bilder in Echtzeit sehen und sich auf die Software verlassen, die signalisiert, wann die Spitze in die richtige Höhle eingetreten ist oder sich einem Blutgefäß nähert. Weniger Punktionen würden geringere Gewebeschädigung, ein geringeres Blutungsrisiko und potenziell kürzere Eingriffe und Krankenhausaufenthalte bedeuten. Obwohl die Arbeit an gespendeten Nieren und nicht an lebenden Patientinnen und Patienten durchgeführt wurde, schafft sie die Grundlage für klinische Systeme, die auch andere nadelbasierte Interventionen unterstützen könnten — von Biopsien und Nervenblockaden bis hin zu gezielter Medikamentenabgabe.
Zitation: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
Schlüsselwörter: Nierenstein‑Operation, Nadelsteuerung, optische Kohärenztomographie, medizinische Bildgebung KI, Erkennung von Blutgefäßen