Clear Sky Science · de
Einzelzell-Einblicke in die Heterogenität der Trophoblasten und adaptive Dysfunktion bei selektiver fetaler Wachstumsrestriktion
Wenn ein Zwilling zurückbleibt
Für Eltern, die Zwillinge erwarten, kann es sehr beunruhigend sein, wenn ein Baby nicht so gut wächst wie das andere, obwohl sie sich dieselbe Gebärmutter und Plazenta teilen. Dieser Zustand, selektive fetale Wachstumsrestriktion genannt, gefährdet nicht nur die Gesundheit des kleineren Zwillings vor der Geburt, sondern kann auch die langfristige Entwicklung beeinflussen. Diese Studie nutzt moderne Einzelzellanalyse, um in die gemeinsame Plazenta solcher Zwillingsschwangerschaften zu blicken und zeigt, wie kleine Veränderungen in spezifischen Plazentazellen und Immunantworten das Gleichgewicht zwischen gesundem Wachstum und gefährlichem Mangel kippen können.
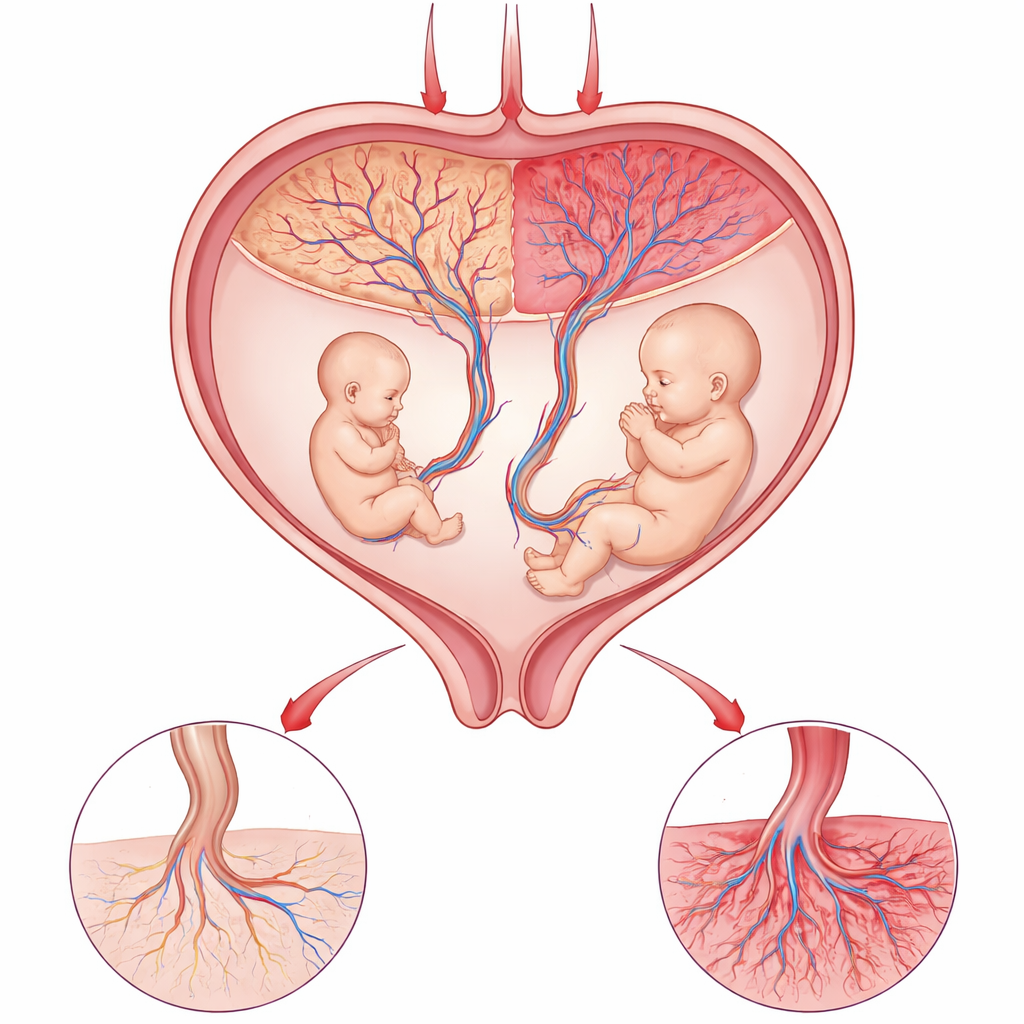
Das empfindliche Gleichgewicht der Plazenta
Die Plazenta ist die Lebensader zwischen Mutter und Kind: Sie liefert Sauerstoff und Nährstoffe und entfernt Abfallstoffe. Bei bestimmten eineiigen Zwillingsschwangerschaften teilen sich beide Babys eine Plazenta, besetzen darin aber unterschiedliche Bereiche. Wenn ein Zwilling deutlich kleiner wird als der andere, ist klar, dass lokal in diesem gemeinsamen Organ etwas schiefgelaufen ist. Da die Zwillinge dieselbe Mutter und fast dieselben Gene haben, bilden sie ein starkes natürliches Experiment: Große Wachstumsunterschiede stammen eher aus der Funktion der jeweiligen Plazentabereiche als aus Unterschieden zwischen den Babys selbst.
Reinschauen in einzelne Plazentazellen
Die Forschenden sammelten Plazentaproben aus drei Schwangerschaften, in denen ein Zwilling deutlich kleiner war als der andere. Mit Einzelzell-RNA-Sequenzierung — einer Methode, die die Aktivität von Tausenden Genen in einzelnen Zellen liest — profilierten sie mehr als 175.000 Zellen aus den verschiedenen Plazentaregionen. Dadurch konnten sie Zellen in unterschiedliche Typen einordnen, darunter Stütz- und Gefäßzellen sowie mehrere Arten von Immunzellen. Ihr Fokus lag auf einer Schlüsselgruppe, den villösen Zytotrophoblasten: einer Zellschicht, die die winzigen fingerförmigen Projektionen auskleidet, an denen mütterliches Blut und fetale Zirkulation aufeinandertreffen, und die die Oberfläche der Plazenta ständig erneuert und repariert.
Zwei zentrale Zellzustände: Struktur versus Überlebensmodus
Innerhalb dieser villösen Zytotrophoblasten entdeckte das Team zwei Hauptzustände mit sehr unterschiedlichen Rollen. Eine Gruppe, gekennzeichnet durch ein Molekül namens TP63, fungierte wie strukturelle Pfleger: Sie unterstützte die Barriere zwischen Mutter und Kind, erhielt Zell‑zu‑Zell-Verbindungen und half, das Gewebe organisiert zu halten. Die andere Gruppe, markiert durch ein Enzym namens LDHA, war auf intensive Energieproduktion und Stressbewältigung ausgerichtet und zeigte verstärkte Wege zu Mitochondrien, oxidativem Stress und Proteinhomöostase. In den Plazentabereichen der kleineren Zwillinge waren die schützenden TP63-Zellen vermindert, während die stressgeprägten LDHA-Zellen vermehrt und aktiver proliferierten. Computergestützte „Trajektorie“-Analysen deuteten darauf hin, dass Zellen entlang eines Pfades von gesunden Strukturfunktionen in einen Überlebensmodus gedrängt wurden, wobei weniger Zellen den vollständig verschmolzenen Zustand erreichten, der normalerweise eine glatte, effiziente Austauschoberfläche erhält.
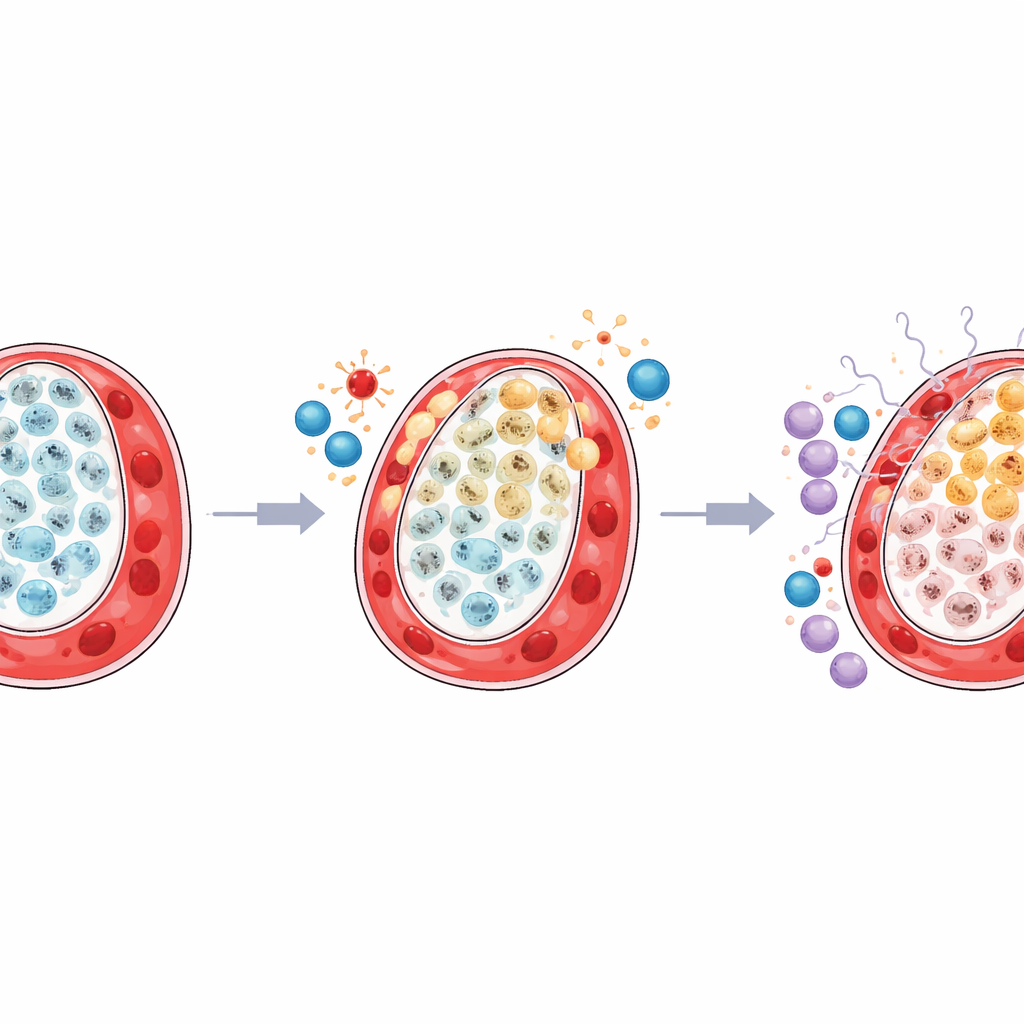
Entzündetes Umfeld um gestresste Zellen
Die Studie zeigte außerdem, dass das umliegende Immunumfeld in den Plazentabereichen des kleineren Zwillings auf schädliche Weise umgestaltet war. Eine hilfreiche Art von residenten Makrophagen, die Hofbauer-Zellen genannt werden und normalerweise Gewebegesundheit und Metabolismus unterstützen, war reduziert. Gleichzeitig wurden bestimmte natürliche Killerzellen, die auf antivirale und entzündliche Reaktionen vorbereitet sind, häufiger und aktiver. Eine detaillierte Kartierung der Signalübertragung zwischen Zellen zeigte, dass die gestressten LDHA-artigen Trophoblasten stärker mit Immunzellen über Signalwege kommunizierten, die von Interferon und verwandten Alarmmolekülen getrieben werden. Gleichzeitig schwächte sich die Kommunikation zwischen den strukturellen TP63-Zellen und unterstützenden Stromal‑ und Gefäßzellen, was darauf hindeutet, dass sowohl physische Unterstützung als auch ruhige Immunregulation verloren gingen.
Dreifacher Zusammenbruch, der das fetale Wachstum einschränkt
In der Summe zeichnet die Arbeit ein klares, nachvollziehbares Bild dessen, was in der Plazenta schiefgeht, wenn ein Zwilling zurückbleibt. Strukturelle Unterstützungzellen, die die Austauschoberfläche dicht und geordnet halten, erschöpfen sich; energiehungrige Stresszellen übernehmen; und das Immunsystem schwenkt in einen entzündlicheren Zustand. Diese drei Faktoren — Strukturverlust, metabolische Überlastung und chronische Entzündung — verstärken einander und untergraben allmählich die Fähigkeit der Plazenta, dem kleineren Baby ausreichend Sauerstoff und Nährstoffe zu liefern. Indem die Studie die spezifischen Zelltypen und Signalwege identifiziert, liefert sie eine Landkarte für künftige Tests und Therapien, die darauf abzielen, Plazentaprobleme früher zu erkennen und diese Zellen vielleicht wieder in ein gesünderes Gleichgewicht zu lenken.
Zitation: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Schlüsselwörter: Plazenta, Zwillingsschwangerschaft, fetale Wachstumsrestriktion, Einzelzell-RNA-Sequenzierung, Trophoblastzellen