Clear Sky Science · de
Quantifizierung von Mikrokernen in Ganzschnitt-Hämatologiebildern mittels KI als übertragbarer pharmakodynamischer Biomarker für Inhibitoren der DNA-Schadensantwort
Warum winzige Punkte im Blut große Geschichten erzählen können
Ärztinnen, Ärzte und Wissenschaftlerinnen sind stets auf der Suche nach einfachen Methoden, um zu prüfen, ob ein Krebsmedikament im Körper die gewünschte Wirkung entfaltet. Diese Studie zeigt, dass winzige Partikel in roten Blutkörperchen, sogenannte Mikrokerne, als natürliche Marker für DNA-Schäden durch bestimmte Krebstherapien dienen können. Durch die Kombination von großflächiger Ganzschnitt-Bildgebung mit künstlicher Intelligenz (KI) verwandelten die Forschenden wenige Blutstropfen in einen umfangreichen, automatisierten Messwert dafür, wie stark DNA‑angreifende Wirkstoffe wirken.
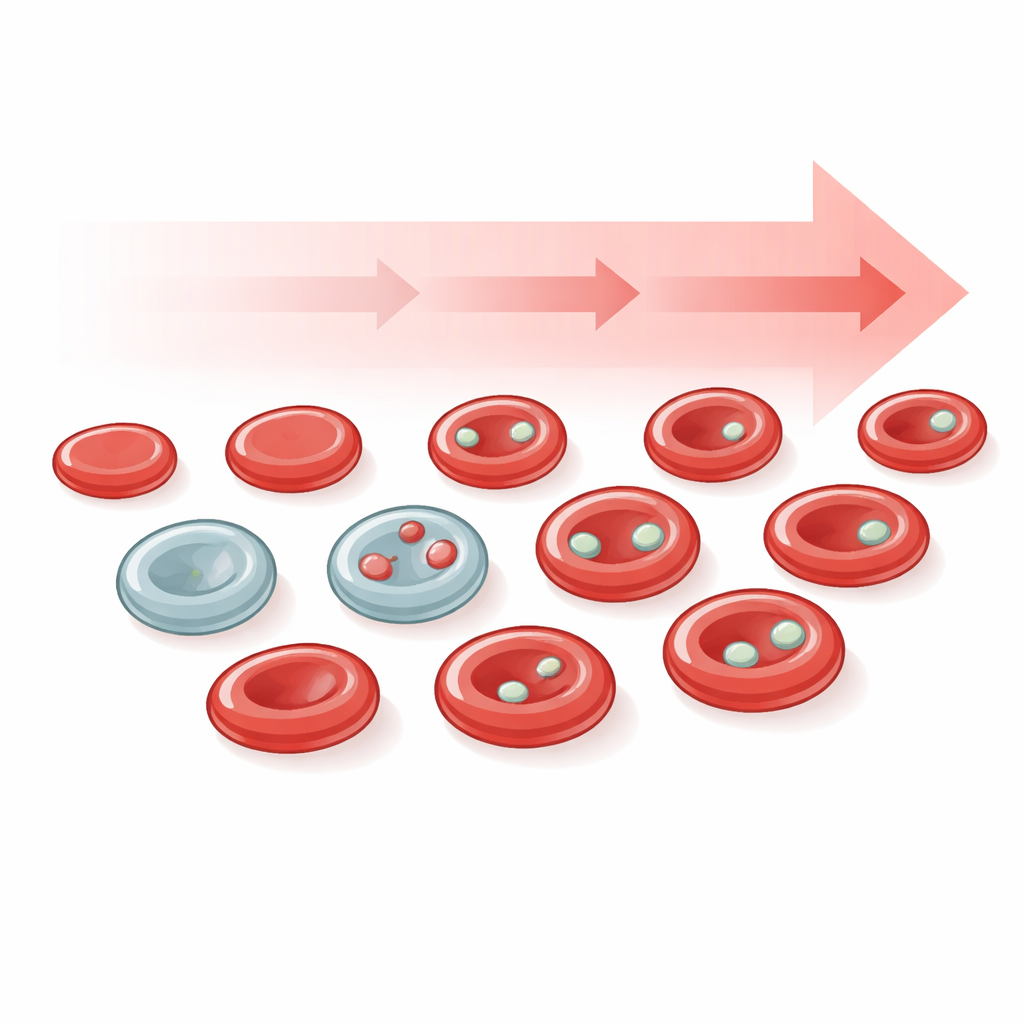
Kleine Inseln von DNA in roten Blutkörperchen
Mikrokerne sind kleine Bläschen aus DNA, die getrennt vom Hauptkern einer Zelle sitzen. Sie entstehen, wenn Chromosomen brechen oder bei der Zellteilung falsch verteilt werden — Vorgänge, die bei Krebs und nach Einwirkung DNA‑schädigender Agenzien häufig auftreten. In den meisten Geweben ist das Erkennen echter Mikrokerne im Mikroskop schwierig, da dünne Gewebeschnitte leicht täuschen können. Rote Blutkörperchen bieten hier einen Vorteil: Beim Reifen stoßen sie normalerweise ihren Hauptkern ab, doch vorher gebildete Mikrokerne können als winzige, klar abgegrenzte Punkte zurückbleiben. Diese lange bekannten Strukturen, historisch als Howell–Jolly‑Körper bezeichnet, sind somit praktische, echte Mikrokerne, die im Blutkreislauf zirkulieren und anzeigen können, wie viel DNA‑Schaden kürzlich aufgetreten ist.
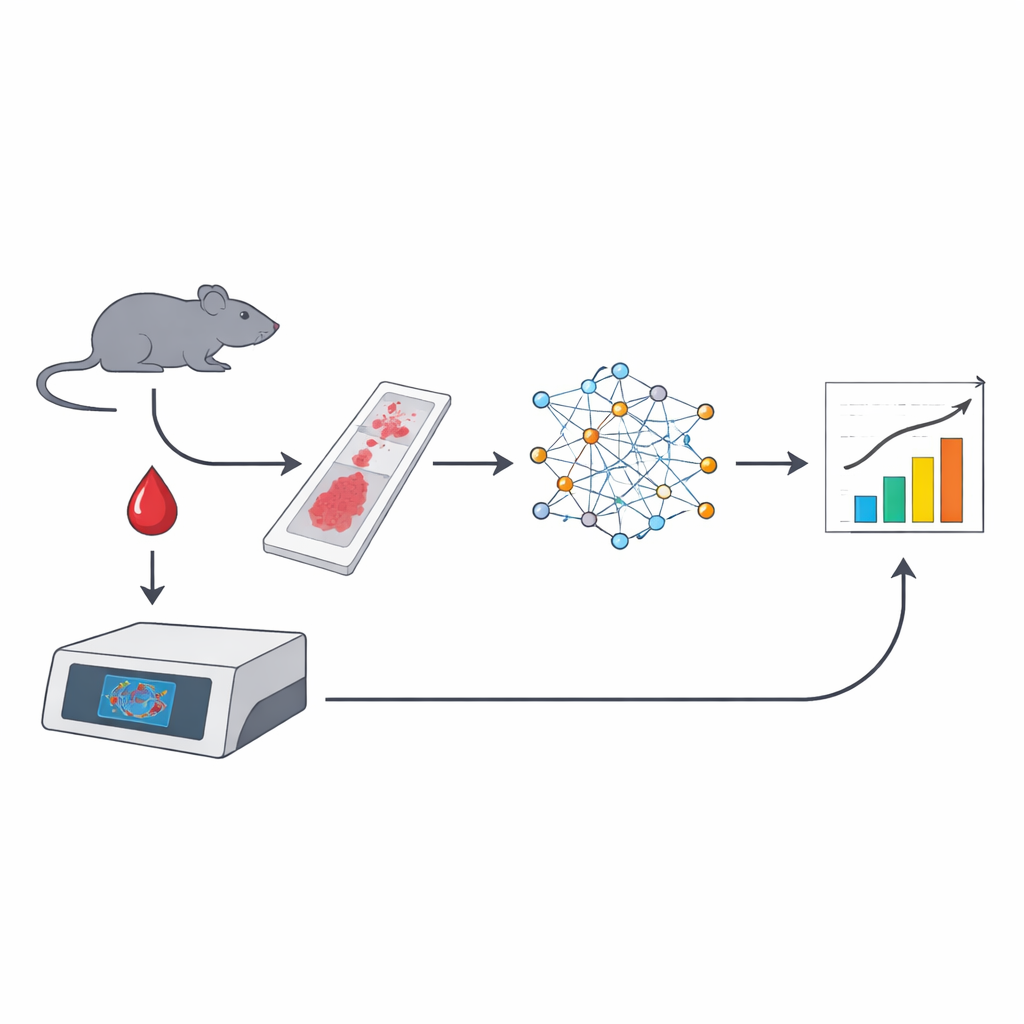
Blutausstriche mit KI in Daten verwandeln
Das Team entwickelte eine automatisierte Pipeline, die bei standardmäßigen Blutausstrichen von Mäusen ansetzt, gefärbt entweder mit einem fluoreszierenden DNA‑Farbstoff oder mit gebräuchlichen May–Grünwald‑Giemsa‑Färbungen aus Kliniklaboren. Ganze Objektträger wurden in hoher Auflösung gescannt, und überwachte Deep‑Learning‑Modelle wurden darauf trainiert, rote Blutkörperchen zu erkennen, Mikrokerne herauszufiltern und unreife Retikulozyten von reifen Erythrozyten anhand subtiler Unterschiede in Größe und Farbe zu unterscheiden. Aus einem einzigen Bild konnte das System mehr als 100.000 Zellen analysieren, diejenigen mit Mikrokernen markieren und sogar Zellen zählen, die mehr als einen Mikrokern enthielten — etwas, das mit konventioneller Durchflusszytometrie nicht leicht möglich ist.
Winzige Änderungen im Blut mit Wirkstärke von Medikamenten verknüpfen
Die Forschenden prüften anschließend, ob die Häufigkeit mikrokernpositiver roter Blutkörperchen mit der Exposition gegenüber DNA‑schädigender Chemotherapie und gegenüber Wirkstoffen, die die DNA‑Schadensantwort blockieren (wie PARP‑Inhibitoren), korreliert. Bei Mäusen, die mit Cisplatin oder Paclitaxel behandelt wurden, erfassten die KI‑basierten Zählungen die erwarteten Anstiege mikrokernhaltiger Zellen. In tumorbetragenen Mäusen, die mit den PARP‑Inhibitoren Olaparib oder Saruparib behandelt wurden, führten höhere Dosen zu stärkeren Zunahmen an Mikrokern‑tragenden Zellen und zu ausgeprägterer Tumorschrumpfung. Über mehrere Wochen täglicher Gabe ermöglichten kleine, serielle Blutproben (jeweils nur etwa 5 Mikroliter) dem Team, zu verfolgen, wie sich Mikrokerne langsam anhäufen und nach Absetzen der Behandlung wieder verringern. Beim Vergleich der objektträgerbasierten Methode mit standardmäßiger Durchflusszytometrie stimmten die beiden Ansätze eng überein, was zeigt, dass der neue Workflow sowohl genau als auch robust ist.
Auf junge Blutzellen zoomen für deutlichere Signale
Da junge rote Blutkörperchen (Retikulozyten) besonders häufig frische Mikrokerne enthalten, trainierten die Forschenden ihre Algorithmen, die Erythrozytenpopulation auf Routinenfärbungen in unreife und reife Zellen zu unterteilen. Diese Verfeinerung zeigte, dass Mikrokerne in Retikulozyten deutlich stärker angereichert und dynamischer sind als in älteren Zellen und somit ein sensibleres und schneller veränderliches Signal der Medikamentenwirkung liefern. Die Ganzschnittbilder ermöglichten außerdem die Überwachung der Probengüte selbst — etwa die Erkennung von roten Zellen, die durch schlechte Lagerung deformiert waren — sodass mangelhafte Objektträger vor der Analyse markiert werden konnten, ein wichtiger Schritt für den späteren klinischen Einsatz.
Was das für die künftige Krebsbehandlung bedeuten könnte
Die Studie zeigt, dass eine winzige Blutprobe, eine Standardfärbung und eine KI‑gestützte Bildverarbeitung zusammen eine skalierbare, minimalinvasive Messgröße dafür liefern können, wie stark DNA‑angreifende Medikamente im Körper wirken. Obwohl die Arbeit an Mäusen durchgeführt wurde und rote Blutkörperchen lediglich stellvertretend dafür stehen, was in Tumoren geschieht, deutet die starke Verbindung zwischen Mikrokernsignalen und Tumorantwort darauf hin, dass dieser Ansatz zu einem praktischen Werkzeug in der Wirkstoffentwicklung und schließlich in klinischen Studien werden könnte. Einfach ausgedrückt: Das Zählen dieser mikroskopischen DNA‑„Pünktchen“ im Blut kann Forschenden und Klinikerinnen helfen, Dosen zu justieren, neue Medikamente zu vergleichen und Behandlungseffekte im Zeitverlauf zu verfolgen — ohne wiederholte, invasive Biopsien.
Zitation: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Schlüsselwörter: Mikrokerne, rote Blutkörperchen, PARP-Inhibitoren, digitale Pathologie, DNA-Schadensantwort