Clear Sky Science · de
Entwicklung und Charakterisierung eines induzierbaren Tensin1-defizienten transgenen Mausmodells
Warum das An- und Ausschalten von Genen bei Mäusen wichtig ist
Unsere Körper sind auf unzählige Proteine angewiesen, die Zellen helfen, an ihrer Umgebung zu haften, physikalische Kräfte wahrzunehmen und auf Verletzungen zu reagieren. Eines dieser Proteine, Tensin1 genannt, wurde mit Nierenerkrankungen, Lungenproblemen und Krebs in Verbindung gebracht, doch Wissenschaftlern fehlte bislang eine präzise Methode, seine Funktion in adulten Geweben zu untersuchen, ohne die Entwicklung zu stören. Diese Arbeit beschreibt eine neue Art von Labormaus, bei der Tensin1 auf Befehl ausgeschaltet werden kann, sodass Forscher beobachten können, wie erwachsene Organe und Immunzellen reagieren, wenn dieses zentrale Strukturprotein fehlt.
Ein steuerbarer Schalter für ein klebendes Zellprotein
Tensin1 sitzt an den Stellen, an denen Zellen am umgebenden Stützgeflecht anhaften und innere Fasern der Zelle mit Molekülen außerhalb verbinden. Um seine Rolle sicherer zu untersuchen, konstruierten die Forschenden Mäuse so, dass ein entscheidender Abschnitt des Tensin1-Gens von speziellen DNA‑Sequenzen flankiert ist, die herausgeschnitten werden können, wenn ein anderes Protein, das durch das Medikament Tamoxifen aktiviert wird, vorhanden ist. Durch Einkreuzen dieser Komponenten schufen sie Mäuse, bei denen ein kurzer Tamoxifen‑Behandlungszeitraum im Erwachsenenalter Tensin1 sauber entfernt, während andere eng verwandte Proteine unangetastet bleiben. Tests am Lungengewebe zeigten etwa einen 95-prozentigen Rückgang der Tensin1‑Genaktivität und einen dramatischen Verlust des Tensin1‑Proteins nach der Behandlung, was bestätigt, dass der genetische Schalter wie beabsichtigt funktioniert.
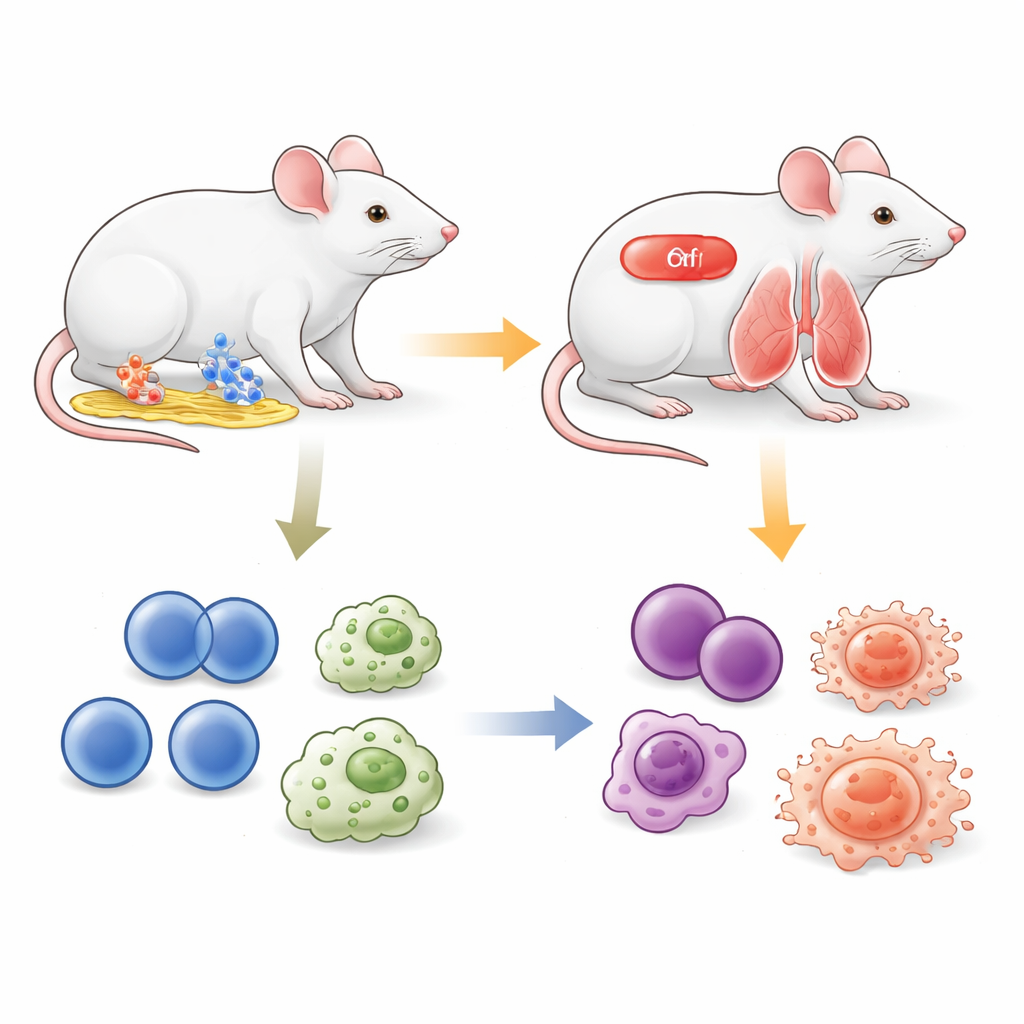
Gesundes Aussehen verbirgt subtile innere Veränderungen
Man hätte erwarten können, dass das Entfernen eines Strukturproteins, das mit schweren Nierenerkrankungen verbunden ist, die Tiere schnell krank macht. Überraschenderweise blieben diese induzierbaren Tensin1‑defizienten Mäuse äußerlich gesund. Vor der Tamoxifenbehandlung vermehrten sie sich normal und hatten Wurfgrößen ähnlich denen gängiger Labormäusestämme. Nachdem Tensin1 im Erwachsenenalter ausgeschaltet wurde, behielten die Tiere im Vergleich zu behandelten Kontrollen ein normales Körpergewicht. Detaillierte Untersuchungen wichtiger Organe wie Herz, Leber, Milz, Lunge und Nieren über den Zeitraum eines Jahres zeigten nur milde, verstreute Veränderungen, die sowohl bei normalen als auch bei Tensin1‑defizienten Mäusen zu finden waren. Viele dieser Befunde, einschließlich lokaler Entzündungen im Bauchraum und einer Verdickung der Gebärmutterschleimhaut, waren konsistent mit bekannten Nebenwirkungen von Tamoxifen selbst und nicht mit dem Verlust von Tensin1. Bluttests zeigten ebenfalls keine eindeutigen Unterschiede in Zellzahlen oder in Laborparametern von Leber und Niere, die dem Gen-Knockout zuzuschreiben wären.
Ein unerwartetes Signal aus Lungen-Immunezellen
Obwohl die Mäuse äußerlich unauffällig waren, vermuteten die Forschenden, dass auf molekularer Ebene, besonders in der Lunge, subtilere Verschiebungen stattfinden könnten, da Tensin1 dort bekanntlich Einfluss auf narbenbildende Zellen hat. Sie maßen die Genaktivität in der gesamten Lunge und fanden 171 Gene, die nach dem Verlust von Tensin1 hoch- oder herunterreguliert waren. Die Pathway‑Analyse ergab, dass viele dieser Gene nicht der strukturellen Unterstützung der Lunge zuzuordnen waren, sondern dem Immunsystem. Gruppen von Genen, die an Infektionsantworten, der Entwicklung von Immunzellen und der Kommunikation zwischen Immunzellen beteiligt sind, waren stark betroffen. Ein großer Cluster hauptsächlich erniedrigter Gene war mit myeloiden Zellen assoziiert — Immunzellen wie Monozyten und Makrophagen, die Gewebe patrouillieren und Trümmer oder Mikroben aufnehmen. Im Gegensatz dazu trug ein kleinerer Cluster erhöhter Gene das Signaturmuster von B‑Zellen, den Antikörper produzierenden Immunzellen.
Wie Tensin1 das Verhalten von Immunzellen prägt
Um tiefer zu verstehen, was diese Signaturen bedeuten, wandte sich das Team einer menschlichen Zelllinie zu, die Monozyten und Makrophagen nachahmt. Als sie Tensin1 in diesen Zellen mit kurzen RNA‑Molekülen stilllegten, wurden die Zellen kleiner und breiteten sich weniger auf mit Fibronectin beschichteten Oberflächen aus — einem wichtigen Stützprotein. Live‑Aufnahmen zeigten, dass Tensin1‑defiziente Zellen kürzere Wege zurücklegten, was auf beeinträchtigte Migration hindeutet. In einem Phagozytose‑Test, bei dem Zellen aufgefordert werden, fluoreszierende Partikel zu verschlingen, nahmen Zellen ohne Tensin1 weniger Partikel auf als Kontrollzellen. Zusammengenommen deuten diese Ergebnisse darauf hin, dass Tensin1 myeloiden Zellen hilft, ihre Form zu bewahren, sich effektiv über Gewebeoberflächen zu bewegen und ihre Aufräumfunktion auszuführen. Bei den lebenden Mäusen zeigte die kurz nach dem Tensin1‑Knockout gewaschene Flüssigkeit aus den Atemwegen eine Tendenz zu mehr Lymphozyten, was mit den B‑Zell‑bezogenen Genveränderungen im Lungengewebe übereinstimmt.
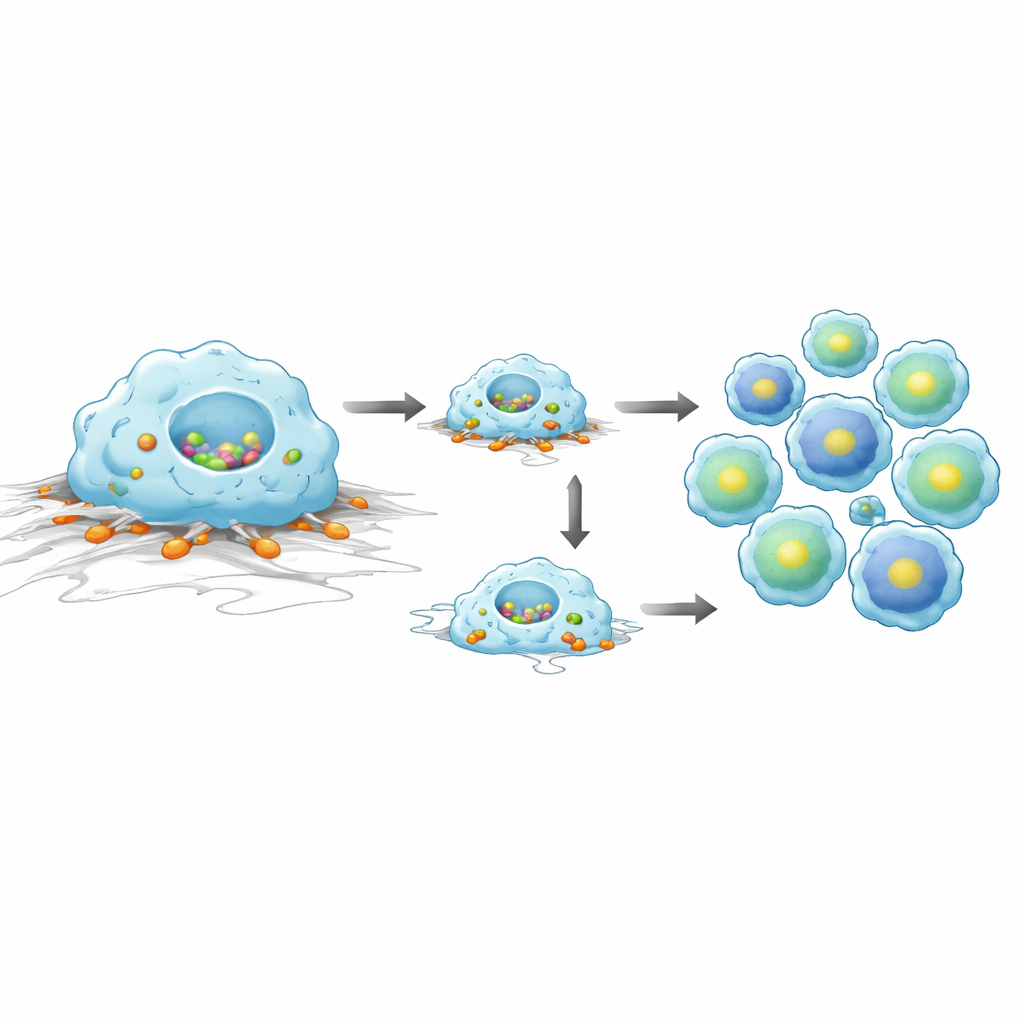
Was das für künftige Krankheitsforschung bedeutet
Einfach gesagt zeigt diese Studie, dass das Entfernen von Tensin1 bei erwachsenen Mäusen die lebenswichtigen Organe nicht dramatisch schädigt, wohl aber still die Immunaktivität in der Lunge umstellt — es schwächt die Signatur der patrouillierenden Zellen, die Trümmer entfernen, und verstärkt die der antikörperbezogenen Zellen. Das neue Mausmodell funktioniert wie ein Dimmschalter, mit dem Tensin1 zu gewählten Zeiten und in ausgewählten Zelltypen abgeschaltet werden kann, ohne die verwirrenden Entwicklungsprobleme, die auftreten, wenn das Gen von Geburt an fehlt. Dieses Werkzeug ermöglicht es Forschern, zu untersuchen, wie Tensin1 Reaktionen auf Lungenverletzung, Infektion und Vernarbung beeinflusst, und könnte letztlich klären, warum genetische Veränderungen in Tensin1 mit menschlichen Lungenkrankheiten und Krebs verbunden sind.
Zitation: Bernau, K., Holbert, K., McDermott, I.S. et al. Development and characterization of an inducible Tensin1 deficient transgenic murine model. Sci Rep 16, 8639 (2026). https://doi.org/10.1038/s41598-026-41319-3
Schlüsselwörter: Tensin1, transgenes Mausmodell, Lungenimmunität, Makrophagenfunktion, bedingter Gen-Knockout