Clear Sky Science · de
Erster Vergleich kommerzieller Systeme zur Herstellung von Nanofett: technische Leistung und biologische Qualität unterscheiden sich zwischen den erzielten Produkten
Warum das für die tägliche Medizin wichtig ist
Ärzte verwenden zunehmend körpereigenes Fett, nicht nur um Volumen im Gesicht oder am Körper wiederherzustellen, sondern auch um geschädigte Haut und Weichteile bei der Heilung zu unterstützen. Eine spezielle Form, genannt „Nanofett“, wird in sehr kleinen Mengen injiziert, um Narben zu glätten, die Hautbeschaffenheit zu verbessern und die Gewebereparatur zu fördern. Kliniken können jedoch verschiedene Kits zur Herstellung von Nanofett kaufen, und bislang wusste niemand genau, ob sie alle das gleiche regenerative Material erzeugen. Diese Studie ist der erste direkte Vergleich populärer kommerzieller Systeme und stellt eine einfache, aber wichtige Frage: Produzieren unterschiedliche Geräte unterschiedliche Nanofette?
Von normalem Fett zu heilenden Mikrotransplantaten
Nanofett beginnt als gewöhnliches Fett, das bei einer Fettabsaugung meist vom Bauch, den Hüften oder den Oberschenkeln entnommen wird. Anstatt als klumpige „Füller“ injiziert zu werden, wird das Fett kräftig hin und her durch enge Verbindungen oder scharfe Gitter gepresst, manchmal gefolgt von einer Filtration. Diese mechanische Aufbereitung zerkleinert es zu einer feineren, injizierbaren Suspension, die durch sehr dünne Nadeln in die oberen Hautschichten gelangen kann. Es geht weniger darum, Volumen hinzuzufügen, sondern lebende Stütz‑ und Regenerationszellen sowie Gewebsfragmente zu liefern, die Wachstumsfaktoren freisetzen, das Gefäßwachstum anregen, Entzündungen dämpfen und Narben umgestalten.
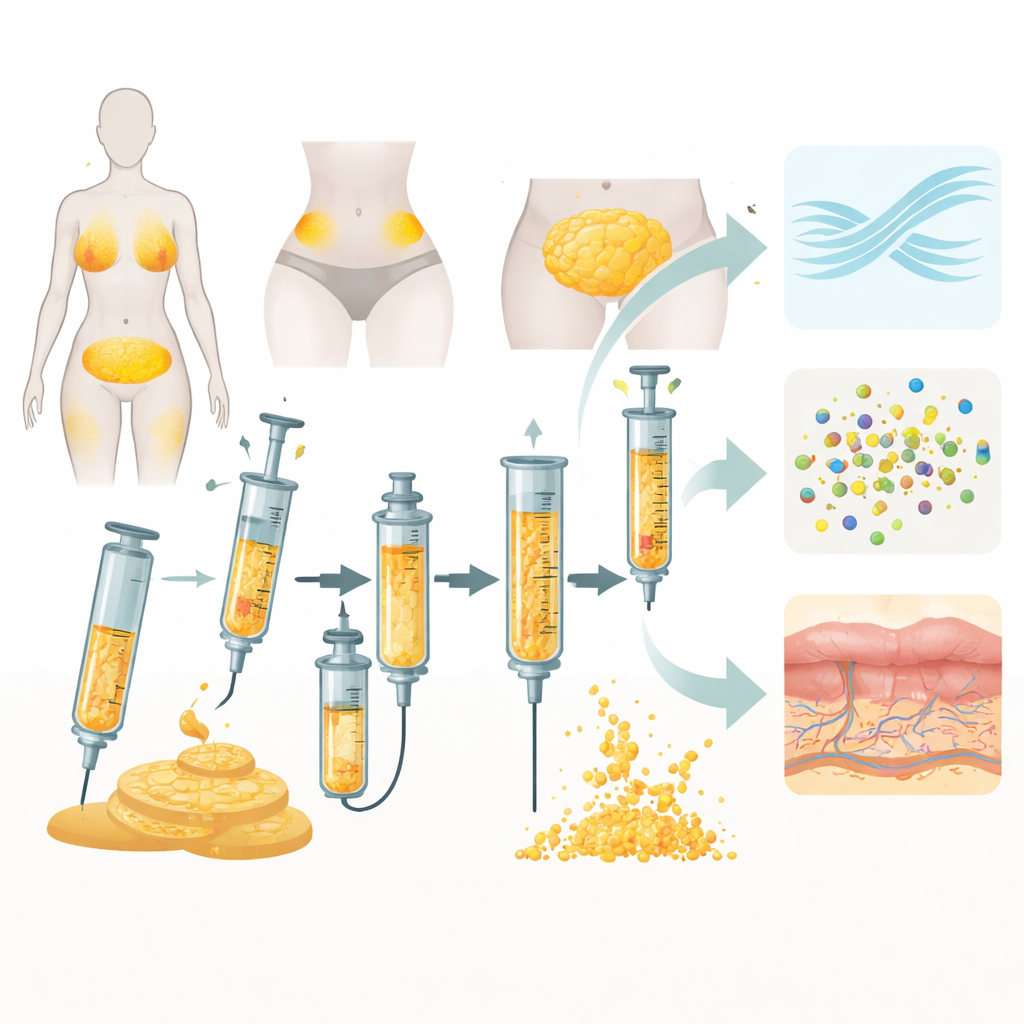
Acht Geräte im Vergleich
In dieser Studie wurde Fett von fünf gesunden Frauen, die sich einer kosmetischen Fettabsaugung unterzogen, mit acht weithin verfügbaren Geräten verarbeitet, die entweder „Emulgierung“ (hauptsächlich Gewebe durch Strömung zerreißen) oder „Mikronisierung“ (Durchpressen durch scharfe Gitter) verwenden. Das Team betrachtete praktische Aspekte, die im Operationssaal wichtig sind, wie Vorbereitungszeit, Handhabungsaufwand, wie reibungslos das Produkt injizierbar war, wie viel nutzbares Nanofett gewonnen wurde und wie wässrig es war. Zudem wurden detaillierte Labortests durchgeführt: wie viele Zellen überlebten, wie viele lebensfähige Zellen pro Milliliter gewonnen wurden, welche Zelltypen vorhanden waren, ob sich stammzellähnliche Zellen noch zu Kolonien bilden konnten und welche Arten winziger Signalpartikel, so genannter extrazellulärer Vesikel, freigesetzt wurden.
Technischer Komfort versus biologische Fülle
Technisch funktionierten alle Geräte ziemlich gut, doch einige zeichneten sich deutlich aus. Das Emulsfat‑System und das neuere Puregraft Boost V2 waren am schnellsten in der Anwendung, produzierten konzentriertes Fett mit wenig Restflüssigkeit und wurden als am einfachsten zu handhaben und zu injizieren bewertet. Biologisch am besten schnitt jedoch Adinizer ab: Es lieferte den höchsten Anteil an regenerativen stromalen bzw. stammzellähnlichen Zellen, während die Zellüberlebensrate über 85 % lag — ein Wert, den alle Systeme erreichten. Im Gegensatz dazu erzeugte Hy‑Tissue Nanofat insgesamt weniger Zellen und einen höheren Anteil an weißen Blutkörperchen, was nicht immer wünschenswert sein muss. Diese Ergebnisse zeigen, dass ein Kit, das sich gut in der Hand des Chirurgen anfühlt, nicht automatisch das biologisch reichste Produkt hervorbringt; die Wahl eines Systems erfordert möglicherweise einen Abwägungsprozess zwischen technischem Komfort und dem gewünschten biologischen Profil.
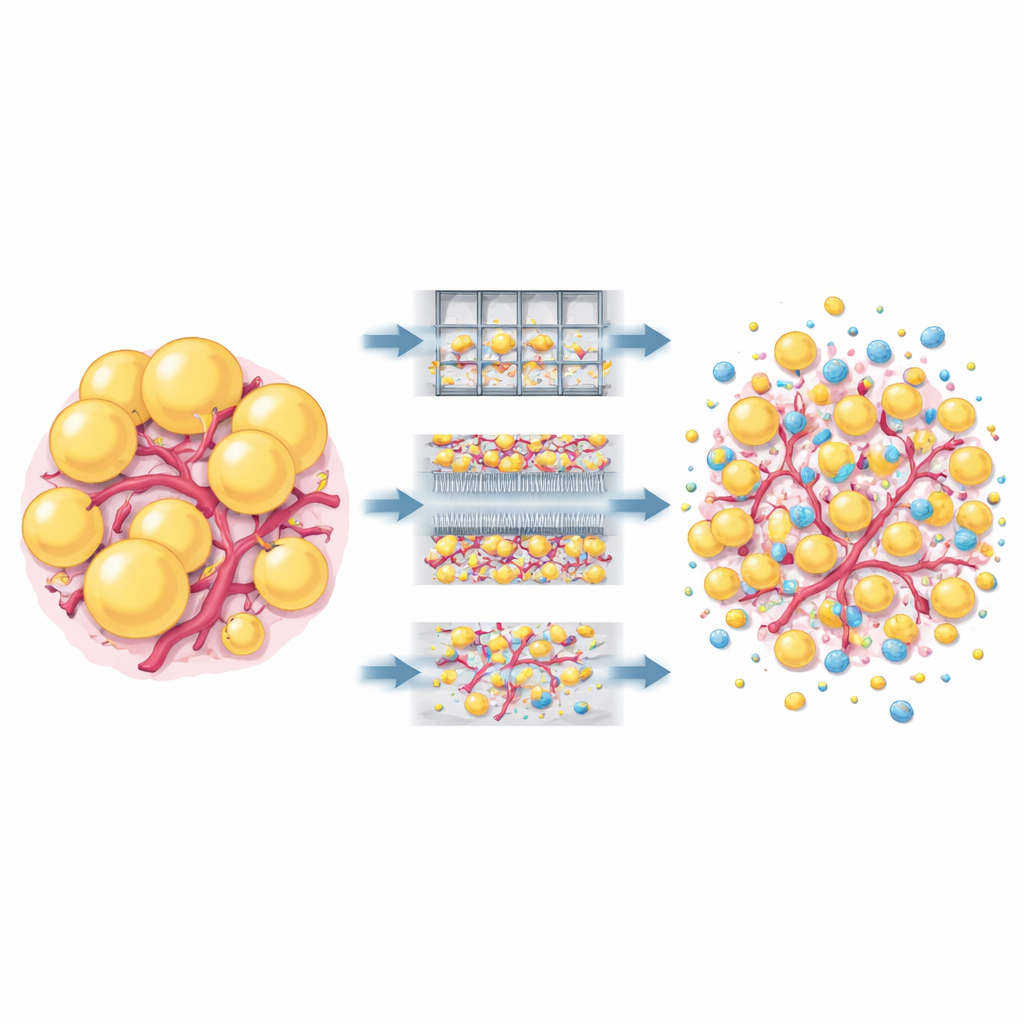
Verborgene Struktur und winzige Botenstoffe
Mikroskopische Aufnahmen lieferten eine überraschende Erkenntnis: Trotz der intensiven mechanischen Behandlung enthielt Nanofett aus den meisten Geräten weiterhin intakte Fettzellen, kleine Blutgefäße und ein erhaltenes Geflecht von Matrixproteinen. Das stellt die weitverbreitete Annahme in Frage, Nanofett sei einfach eine zellreiche Flüssigkeit, deren gesamte Struktur zerstört sei. Die Forscher sammelten außerdem die Flüssigkeit, in der Nanofett kurz kultiviert wurde, und zählten extrazelluläre Vesikel — nanoskalige Bläschen, die Proteine und genetische Signale transportieren. Die Gesamtzahl der Vesikel war geräteübergreifend ähnlich und variierte stärker zwischen den Spendern als zwischen den Methoden, obwohl Emulsfat‑Proben etwas reicher an Vesikeln aus Fettzellen waren.
Was das für künftige Behandlungen bedeutet
Für Patienten lautet die Kernbotschaft, dass „Nanofett“ kein einheitliches Produkt ist; was letztlich in der Spritze landet, hängt stark davon ab, wie es hergestellt wurde. Manche Systeme setzen auf Geschwindigkeit, leichte Injektierbarkeit und hohes Volumen, während andere regenerativen Zellen besser erhalten. Die kombinierte Bewertung technischer und biologischer Merkmale liefert Klinikern eine Orientierung, um Geräte an spezifische Ziele anzupassen, etwa um stammzellähnliche Zellen für anspruchsvolle regenerative Eingriffe zu maximieren oder für oberflächliche Hautbehandlungen eine einfache Verabreichung zu priorisieren. Allgemeiner unterstreicht die Arbeit die Notwendigkeit klarer Standards, damit Ärzte und Forscher, wenn sie über Nanofett sprechen, wirklich vergleichbare Therapien meinen — und so die fettbasierte regenerative Medizin sicherer, wirkungsvoller und vorhersehbarer machen.
Zitation: Arcani, R., Abellan, M., Simoncini, S. et al. First comparison of commercial systems to prepare nanofat: technical performances and biological quality differ among obtained products. Sci Rep 16, 9998 (2026). https://doi.org/10.1038/s41598-026-40847-2
Schlüsselwörter: nanofett, Fetttransplantation, adipöse Stammzellen, Regenerative Medizin, extrazelluläre Vesikel