Clear Sky Science · de
Möglicher gonadenschützender Effekt von Sitagliptin gegen paclitaxelinduzierte Hodenfunktionsstörung über Vermittlung des PERK/CHOP/NLRP3/Sestrin2-Signalwegs
Warum diese Studie für Krebspatienten wichtig ist
Chemotherapie rettet Leben, kann aber still die Fruchtbarkeit schädigen, besonders bei Männern. Ein weit verbreitetes Krebsmedikament, Paclitaxel, ist dafür bekannt, die Hoden zu schädigen und die Spermienqualität zu verringern. Diese Studie an Ratten stellt eine praktische Frage mit klarer menschlicher Relevanz: Kann eine bereits zugelassene Diabetes‑Tablette, Sitagliptin, umfunktioniert werden, um das männliche Fortpflanzungssystem vor den Nebenwirkungen von Paclitaxel zu schützen, ohne seine krebsbekämpfende Wirkung zu beeinträchtigen?
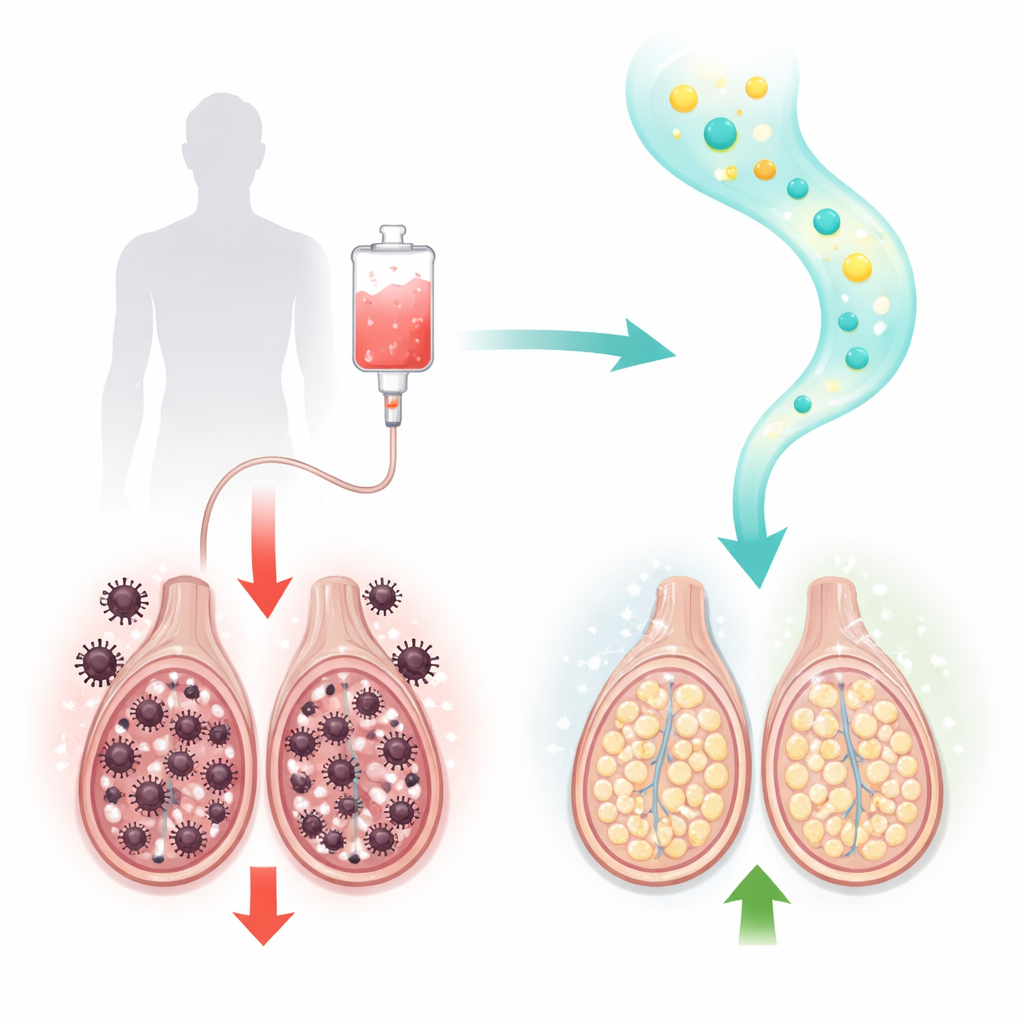
Ein gängiges Krebsmedikament mit versteckten Kosten
Paclitaxel ist ein Standardmedi-kament bei Brust-, Eierstock-, Lungen- und anderen soliden Tumoren. Es wirkt, indem es die Zellteilungsmaschinerie schnell wachsender Krebszellen einfriert. Leider sind auch teilende Zellen in gesunden Organen anfällig. Bei männlichen Ratten führte eine Paclitaxel‑Behandlung zu typischen Zeichen hodenbedingter Schädigung: Spermienzahl, Beweglichkeit und Lebensfähigkeit sanken deutlich, während missgestaltete Spermien zunahmen. Unter dem Mikroskop beobachteten die Forschenden geschädigte Samenkanälchen (in denen Spermien entstehen) und verletzte hormonproduzierende Leydig‑Zellen sowie geschrumpfte Gewebsschichten. Bluttests bestätigten, dass Testosteron und ein für seine Synthese wichtiges Enzym, 17β‑Hydroxy‑Steroid‑Dehydrogenase, stark reduziert waren.
Ein Diabetes‑Medikament als unerwarteter Schutz
Sitagliptin wird häufig zur Kontrolle des Blutzuckers bei Menschen mit Typ‑2‑Diabetes verschrieben. Frühere Arbeiten deuteten darauf hin, dass Sitagliptin über seine metabolischen Effekte hinaus schädlichen oxidativen Stress, Entzündungen und Zelltod in Organen wie Leber, Niere und Gehirn abschwächen kann. Aufbauend darauf teilten die Forschenden männliche Ratten in vier Gruppen ein: unbehandelte Kontrollen, eine Paclitaxel‑Gruppe sowie zwei Gruppen, die Paclitaxel plus entweder eine niedrige oder eine höhere Dosis Sitagliptin für zwei Wochen erhielten. Anschließend verglichen sie Spermienqualität, Hormonspiegel, Gewebestruktur und eine Reihe molekularer „Alarmsysteme“ in den Hoden, die Stress wahrnehmen und Entzündung sowie Zelltod auslösen.
Wie Sitagliptin zellulären Stress und Entzündung dämpfte
Paclitaxel versetzte die Hoden in einen Zustand oxidativen und innerzellulären Stresses: Schadstoffabbauprodukte (gemessen als Malondialdehyd) nahmen zu, während körpereigene Abwehrmechanismen wie reduziertes Glutathion und das Enzym Katalase sanken. Tief in den Zellen schaltete das Proteinfaltungs‑Werk, das endoplasmatische Retikulum, einen Gefahrenweg namens PERK–CHOP ein — ein Signal dafür, dass anhaltender Stress Zellen in Richtung Zelluntergang drängt. Gleichzeitig wurde ein entzündungsfördernder Proteinkomplex (NLRP3) stark aktiviert und trieb entzündliche Botenstoffe wie Interleukin‑1β sowie eine Kaskade von Zelltod‑Proteinen, darunter Cytochrom c und Caspase‑3, voran. Sitagliptin kehrte vieles davon um. Beide Dosen verringerten oxidative Schäden und stellten antioxidative Abwehrmechanismen wieder her. Sie senkten deutlich die Aktivierung des PERK–CHOP‑Stresswegs und bremsten NLRP3‑vermittelte Entzündung und Apoptose. Ein schützendes Protein namens Sestrin2, das bei der Beseitigung reaktiver Moleküle hilft und mit gesünderem Samen in Verbindung gebracht wird, wurde durch Sitagliptin auf Gen‑ und Proteinebene erhöht.
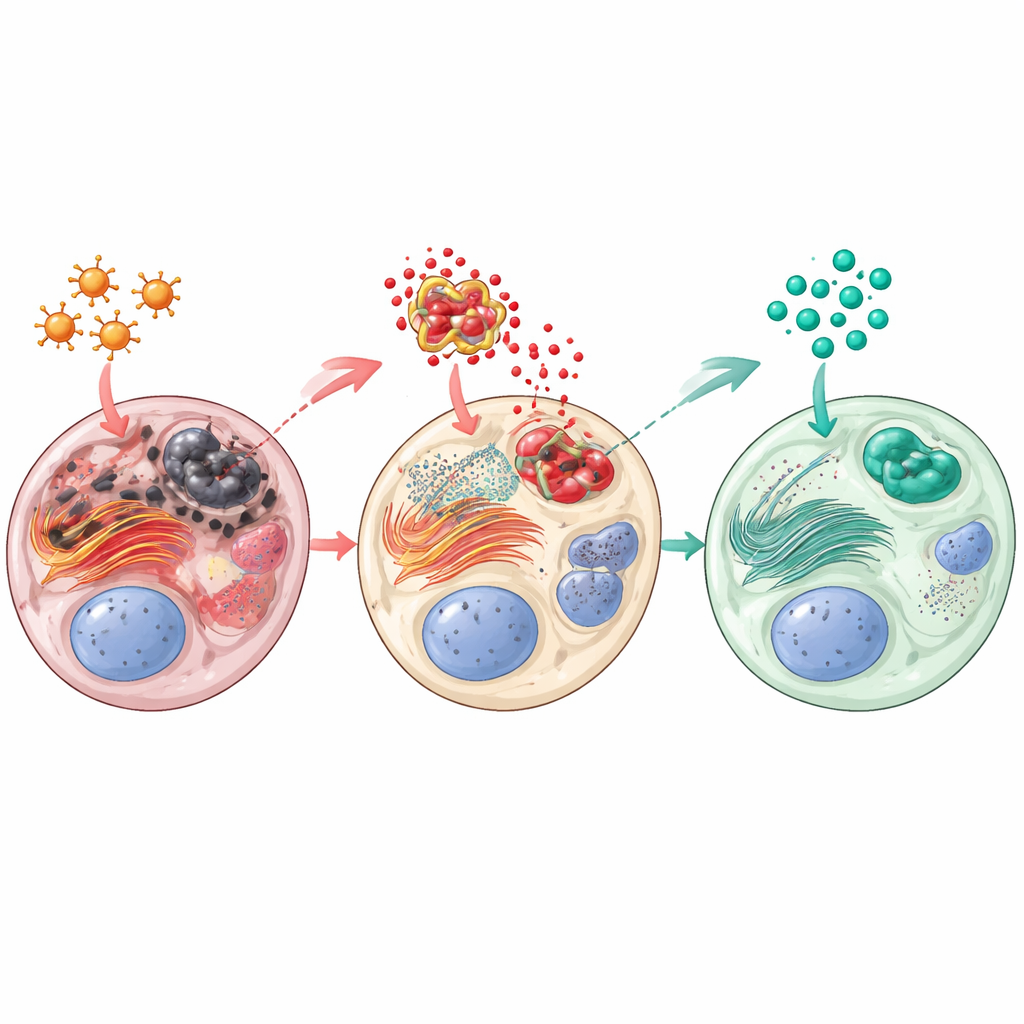
Bessere Spermien, gesünderes Gewebe, stärkere Hormone
Die biochemischen Verbesserungen zeigten sich auch funktionell. Ratten, die nach Paclitaxel Sitagliptin erhielten, hatten höhere Spermienzahlen, bessere Beweglichkeit und weniger abnorme Spermien als Tiere, die nur Paclitaxel bekamen; die höhere Sitagliptin‑Dosis kam dem Normalzustand am nächsten. Testosteron und 17β‑Hydroxysteroid‑Dehydrogenase erholten sich, was darauf hindeutet, dass die Steroidhormonproduktion der Leydig‑Zellen sich wieder normalisiert. Unter Licht‑ und Elektronenmikroskop zeigten die Sitagliptin‑behandelten Hoden geordneter strukturierte Samenkanälchen, mehr Leydig‑Zellen, dickere und gesündere Zellschichten und weniger strukturelle Verzerrungen. Insgesamt trug das Medikament dazu bei, die Architektur und Funktion zu bewahren, die für die fortlaufende Spermienproduktion notwendig sind.
Was das für Männer unter Chemotherapie bedeuten könnte
Diese Tierstudie legt nahe, dass Sitagliptin die durch Paclitaxel ausgelöste Hodenschädigung deutlich abmildern kann, indem es ein Netzwerk schädlicher Signale — oxidativen Stress, innerzellulären Proteinfaltungsstress, Entzündung und programmierten Zelltod — dämpft, größtenteils durch die Erhöhung von Sestrin2 und die Abschwächung der PERK/CHOP/NLRP3‑Achse. Da Sitagliptin bereits klinisch bei Diabetes eingesetzt wird, bietet es sich als realistischer Kandidat an, um als fruchtbarkeitsschützendes Add‑on bei Männern unter Paclitaxel geprüft zu werden, insbesondere bei solchen mit gleichzeitiger Diabeteserkrankung. Die Autorinnen und Autoren betonen, dass noch Studien am Menschen nötig sind, doch ihre Ergebnisse eröffnen eine hoffnungsvolle Möglichkeit: Eine vertraute Tablette könnte Krebspatienten eines Tages nicht nur das Leben retten, sondern auch die Chance erhalten, Vater zu werden.
Zitation: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Schlüsselwörter: paclitaxel, sitagliptin, männliche Fruchtbarkeit, oxidativer Stress, hoden Toxizität