Clear Sky Science · de
Störung der Neutrophilen‑Homöostase ist mit funktionellen Veränderungen der Mitochondrien bei kritisch kranken COVID‑19‑Patienten verbunden
Warum das für COVID‑19‑Patienten wichtig ist
Die meisten wissen inzwischen, dass COVID‑19 mehr ist als eine Lungeninfektion, aber wie genau das Virus die körpereigenen Abwehrkräfte gegen sich selbst wendet, wird noch aufgeklärt. Diese Studie betrachtet Neutrophile, eine häufige Art weißer Blutkörperchen, bei Patienten mit lebensbedrohlichem COVID‑19 auf der Intensivstation. Indem die Forschenden untersuchen, wie diese Zellen leben, sterben und ihre winzigen „Kraftwerke“ (Mitochondrien) nutzen, zeigen sie ein Muster von hartnäckigen, überaktiven Neutrophilen, das helfen könnte, anhaltende Entzündung, Gefäßschäden und Organverletzungen bei schwerer Krankheit zu erklären.
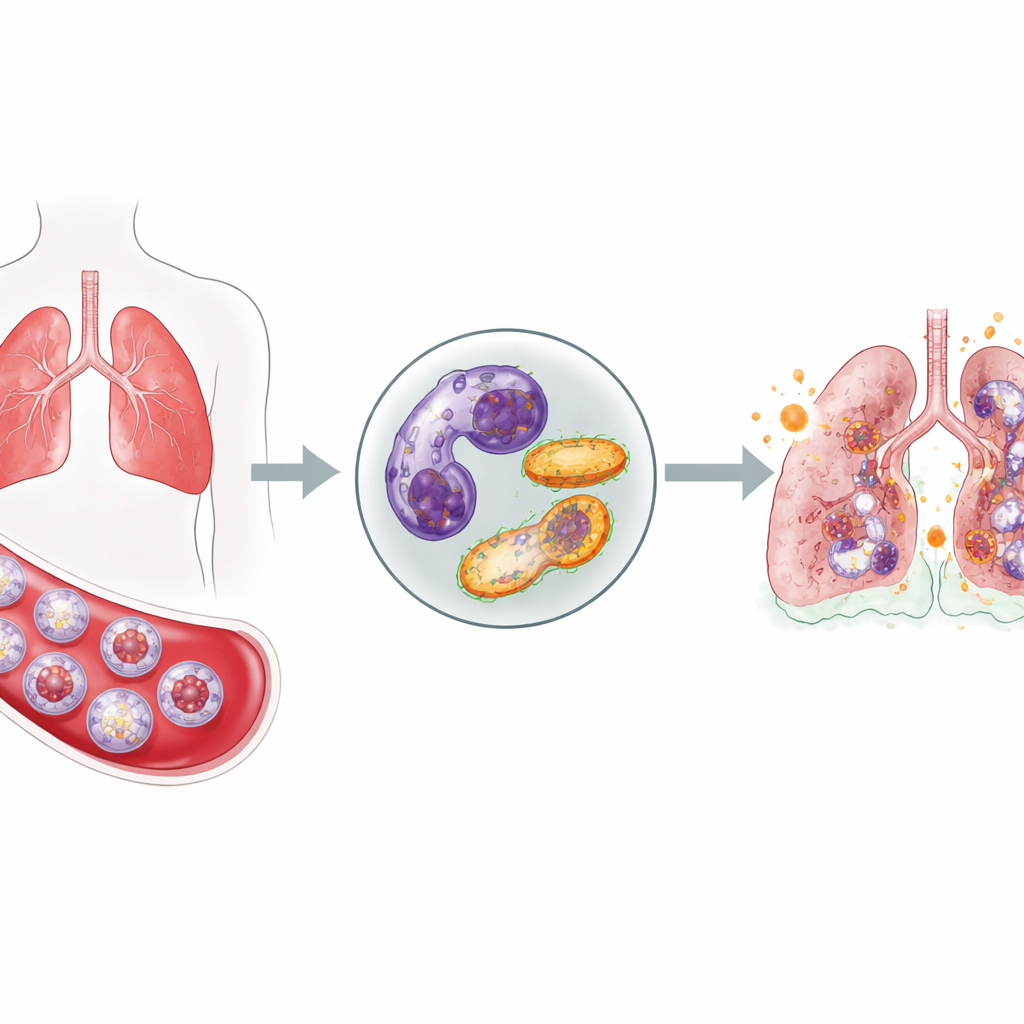
Vorderste Zellen, die nicht abschalten
Neutrophile gehören zu den ersten Einsatzkräften des Körpers bei einer Infektion: Sie strömen in den Blutkreislauf, wandern ins Gewebe und setzen toxische Moleküle frei, um eindringende Mikroben zu töten. Normalerweise zerstören sie sich nach ihrer Aufgabe selbst und werden beseitigt, wodurch Schäden am gesunden Gewebe vermieden werden. Bei kritisch kranken COVID‑19‑Patienten zeigten die Forschenden ein sehr anderes Bild. Im Vergleich zu gesunden Versuchspersonen fanden sie einen Anstieg der Neutrophilen im Blut und, wichtig, viele davon waren unreife Zellen, die eilig aus dem Knochenmark ausgeschwemmt worden waren. Gleichzeitig wiesen verschiedene Tests darauf hin, dass weniger Neutrophile dem normalen programmierten Zelltod unterlagen, was darauf hindeutet, dass diese aggressiven Zellen länger verweilen, als sie sollten.
Feine genetische Signale, aber ein klares Überlebensmuster
Die Forschenden untersuchten außerdem winzige regulatorische Moleküle, sogenannte microRNAs, in Neutrophilen von Intensivpatienten, die überlebten, und solchen, die nicht überlebten. Einige dieser Moleküle waren in einer Weise verändert, die theoretisch auf gestörte Signalwege hinweist, die den Zelltod und das Kalziumgleichgewicht steuern. Als sie jedoch direkte Marker des Zelltods maßen, fanden sie keine großen Unterschiede zwischen Überlebenden und Nicht‑Überlebenden — beide Gruppen zeigten im Vergleich zu gesunden Personen eine ähnlich reduzierte Neutrophilen‑Selbstzerstörung. Das bedeutet, dass die microRNA‑Muster eher Hinweise für zukünftige Untersuchungen als sichere Prädiktoren für das Überleben sind und unterstreichen, dass das allgemeine Versagen der Neutrophilen, sich abzuschalten, ein gemeinsames Merkmal schwerer COVID‑19‑Verläufe ist.
Kalziumverschiebungen und überladene Kraftwerke
Um zu verstehen, warum Neutrophile nicht zum vorgesehenen Zeitpunkt starben, konzentrierte sich das Team auf zwei eng verknüpfte Systeme innerhalb der Zellen: Kalziumsignale und Mitochondrien. Kalziumionen fungieren als winzige Ein/Aus‑Schalter für viele Zellentscheidungen, einschließlich des programmierten Zelltods. Die Forschenden stellten fest, dass Neutrophile aus schweren COVID‑19‑Fällen weniger freies Kalzium im Inneren aufwiesen, zusammen mit reduzierten Mengen wichtiger Proteine, die normalerweise dabei helfen, Kalzium in Mitochondrien zu transportieren und ein Sicherheitsventil zu öffnen, das den Zelltod auslösen kann. Gleichzeitig waren die Mitochondrien selbst ungewöhnlich „aufgeladen“, mit einem höheren elektrischen Gradienten über ihren Membranen und einer erhöhten Sauerstoffaufnahme, besonders über einen wichtigen Atmungsweg. Statt sich abzuschalten, produzierten diese überaktiven Mitochondrien mehr reaktive Sauerstoffmoleküle, die umliegendes Gewebe schädigen und Entzündungen anheizen können.
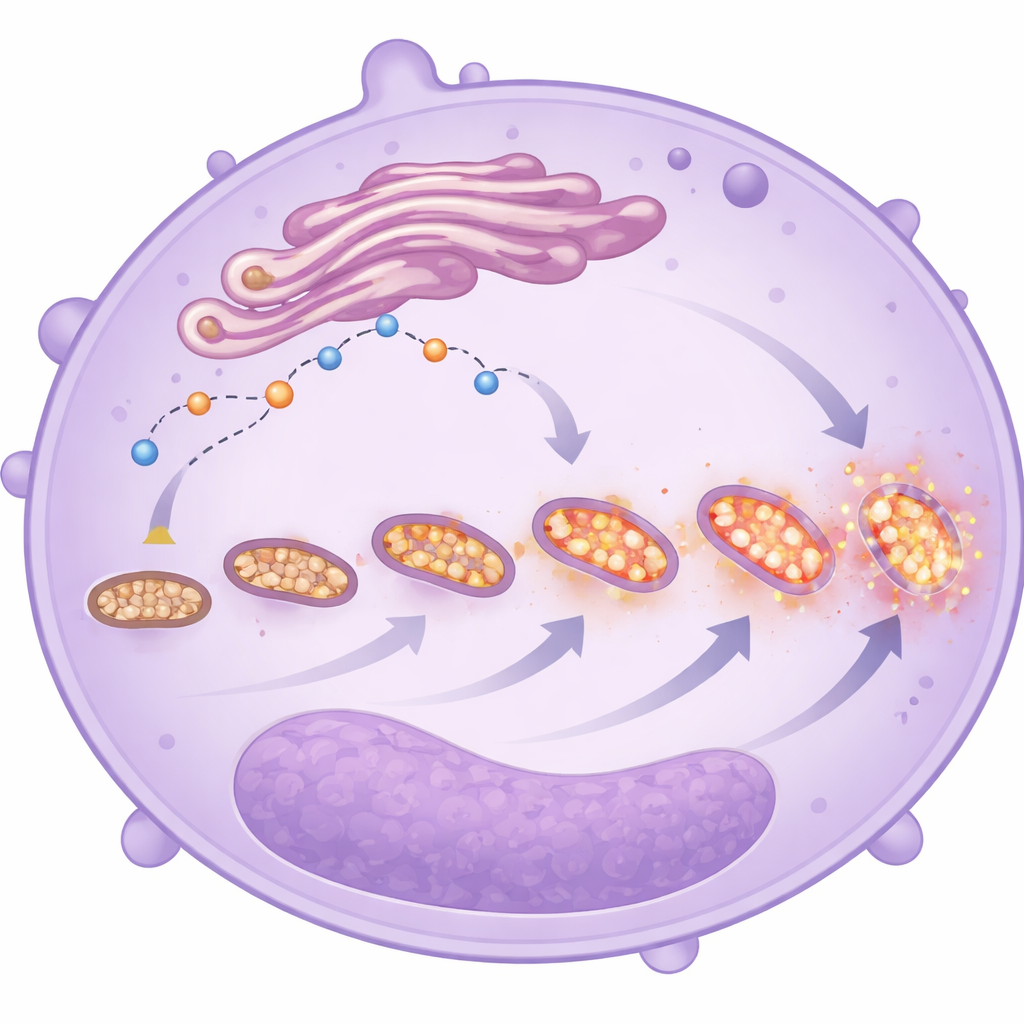
Gestresste und fragmentierende Mitochondrien
Elektronenmikroskop‑Bilder und fluoreszierende Farbstoffe lieferten einen genaueren Blick auf Form und Verhalten dieser Mitochondrien. Bei Neutrophilen der schwersten Patienten waren die Mitochondrien zahlreicher, aber kleiner und stärker fragmentiert — Merkmale, die oft Stress signalisieren. Diese Zellen zeigten außerdem höhere Mengen mitochondrialer reaktiver Sauerstoffspezies, unabhängig davon, ob der Patient letztlich überlebte. Zusammen mit der veränderten Kalziumhandhabung und dem verzögerten Zelltod zeichnen diese Veränderungen das Bild von Neutrophilen, die ihre Energiestrategie umgestellt haben: Anstatt sich hauptsächlich auf einfachen Zuckerabbau zu verlassen, stützen sie sich stärker auf mitochondriale Stoffwechselprozesse, besonders in unreifen Zellen. Dieser Wechsel könnte ihre Fähigkeit erhöhen, zu migrieren, länger zu verharren und schädliche Moleküle in Lunge und anderen Organen freizusetzen, auch wenn die Studie nicht nachweist, dass sie direkt die Ursache schlechterer Verläufe sind.
Was das für die zukünftige Behandlung bedeuten könnte
Einfach ausgedrückt legt die Studie nahe, dass bei kritisch kranken COVID‑19‑Patienten Neutrophile zu zahlreich, zu jung und zu schwer abzuschalten sind. Ihre internen Kalziumsignale und Mitochondrien sind so umgestellt, dass sie die Zellen am Leben und hochaktiv halten, wodurch Schübe schädlicher, auf Sauerstoff basierender Chemikalien entstehen. Obwohl die Arbeit beobachtend ist und keinen Ursache‑Wirkungs‑Zusammenhang beweist, hebt sie mehrere potenzielle „Regelknöpfe“ in diesen Zellen hervor — etwa Kalziumregulatoren und mitochondriale Kontrollpunkte —, die eines Tages angepeilt werden könnten, um Neutrophile behutsam wieder in ein normales Verhalten zu lenken. Wenn zukünftige Forschung diese Ideen bestätigt, könnten Behandlungen, die das ordnungsgemäße Abschalten von Neutrophilen wiederherstellen oder ihre überladenen Mitochondrien beruhigen, dazu beitragen, den Kollateralschaden zu verringern, den diese wichtigen Zellen bei schwerer COVID‑19 und möglicherweise auch bei anderen kritischen Erkrankungen verursachen.
Zitation: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Schlüsselwörter: COVID-19, Neutrophile, Mitochondrien, Entzündung, kritische Erkrankung