Clear Sky Science · de
Synthese und biologische Bewertung von Ibuprofen/o‑Vanillin‑Schiff‑Basen‑Komplexen mit entzündungshemmenden, antiproliferativen und anti‑SARS‑CoV‑19‑Aktivitäten
Warum die Aufwertung eines vertrauten Schmerzmittels wichtig ist
Ibuprofen zählt zu den weltweit am häufigsten verwendeten Schmerz‑ und Fiebermitteln, kann bei Langzeitanwendung jedoch den Magen reizen und wurde nie dafür entwickelt, Infektionen, Krebs oder neue Viren zu bekämpfen. In dieser Studie bauen Chemiker Ibuprofen um, indem sie es an ein natürliches, vanilleähnliches Molekül binden und anschließend verschiedene Metalle einführen. Das Ergebnis ist eine Familie neuer Verbindungen, die nicht nur als Schmerzmittel wirken, sondern potenziell auch als Antibiotika, Antikrebsmittel, entzündungshemmende Wirkstoffe und sogar als Blocker eines wichtigen SARS‑CoV‑2‑Enzyms fungieren — und zugleich Hinweise liefern, wie man aus Alltagsmedikamenten intelligentere Arzneien entwerfen kann.
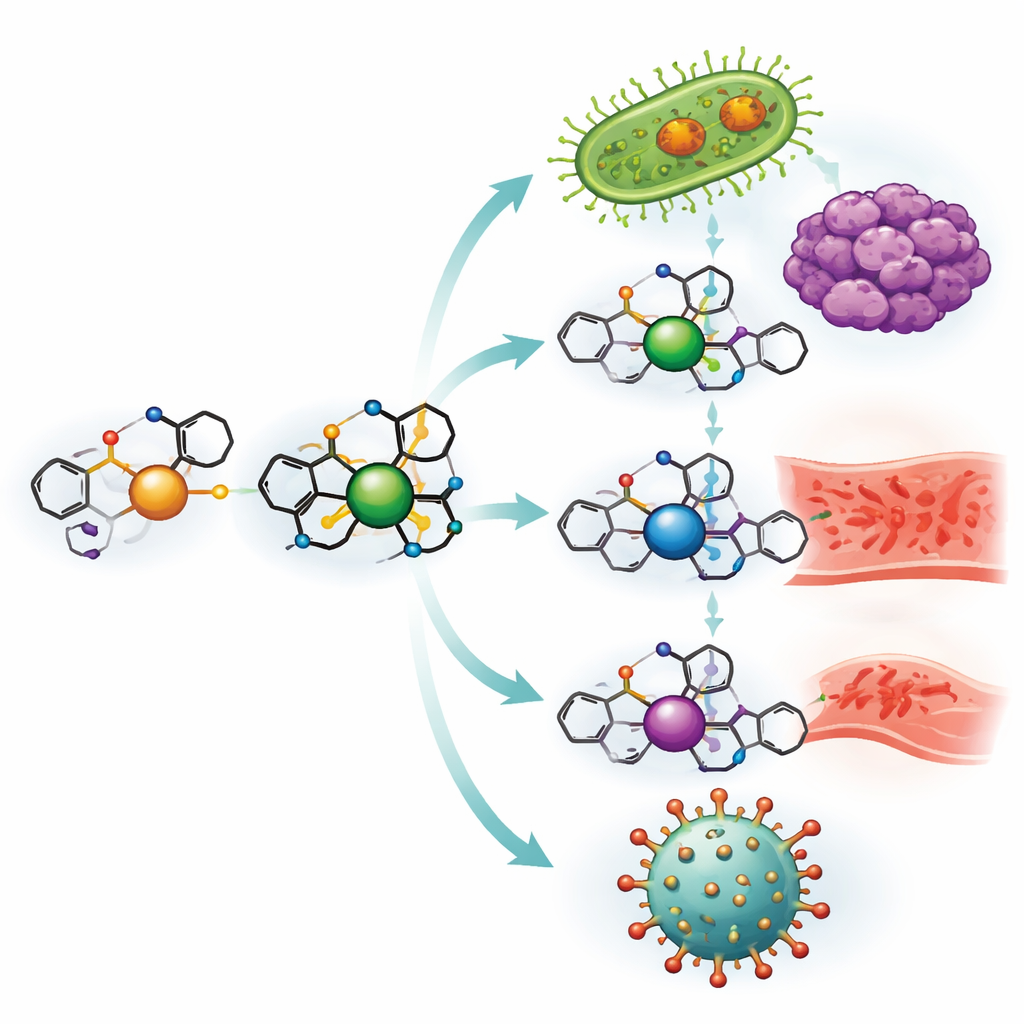
Neue, arzneimittelähnliche Moleküle aus Ibuprofen aufbauen
Das Team begann damit, Ibuprofen in einen vielseitigeren Baustein umzuwandeln und diesen dann mit o‑Vanillin zu verknüpfen, einem chemischen Verwandten der Vanille‑Duft‑Substanz. Zusammen bilden sie eine „Schiff‑Base“‑Ligandstruktur — im Grunde eine maßgeschneiderte Klaue, die Metallionen greifen kann. Dieser Ligand wurde dann separat mit Kupfer‑, Nickel‑, Zink‑ und Vanadiumsalzen kombiniert, um vier unterschiedliche Metallkomplexe zu erzeugen. Sorgfältige Labortests, darunter Schmelzpunktmessungen, spektroskopische Untersuchungen, magnetische Eigenschaften und Kristallstrukturanalysen, bestätigten, wie der Ligand jedes Metall umschließt und wie stabil die resultierenden Komplexe sind — selbst bei hohen Temperaturen und über einen weiten pH‑Bereich.
Wie die Komplexe mit Zellen und DNA wechselwirken
Da die Wirkung eines Wirkstoffs oft davon abhängt, wie er biologische Ziele erreicht, untersuchten die Forschenden, wie diese neuen Komplexe mit DNA und lebenden Zellen interagieren. In Reagenzglas‑Experimenten band insbesondere der Kupferkomplex eng an DNA‑Stränge und konnte diese beschädigen bzw. „spalten“ — ein Verhalten, das häufig bei potenten Antikrebs‑ und antibakteriellen Agenzien beobachtet wird. Bei Tests an humanen Krebszelllinien aus Brust‑, Darm‑ und Lebertumoren waren alle vier Komplexe toxischer für Krebszellen als der alleinige ibuprofenbasierte Ligand, wobei der Kupferkomplex bei ähnlichen Dosen an die Wirksamkeit des Chemotherapeutikums Vinblastin heranreichte.
Gegen Keime, Pilze und Entzündung
Die gleichen Verbindungen wurden gegen verbreitete Krankheitserreger getestet, darunter grampositive und gramnegative Bakterien sowie zwei problematische Pilzarten. Auch hier übertrafen die Metallkomplexe den freien Liganden, wobei Kupfer die besten Hemmwirkungen gegen Bakterien und Pilze zeigte. Die Autoren erklären dies mit der Chelat‑Theorie: Sobald das Metall vom Liganden gebunden ist, wird seine Ladung teilweise abgeschirmt und der gesamte Komplex lipidlöslicher, sodass er leichter in mikrobielle Membranen eindringen und lebenswichtige Enzyme stören kann. In einem einfachen Entzündungsnachweis, der auf hitzedenaturiertem Eiweiß basiert, reduzierten die neuen Komplexe außerdem die Proteindenaturierung wirksamer als Ibuprofen selbst, was darauf hindeutet, dass sie entzündliche Prozesse bei geringeren Dosen dämpfen könnten.
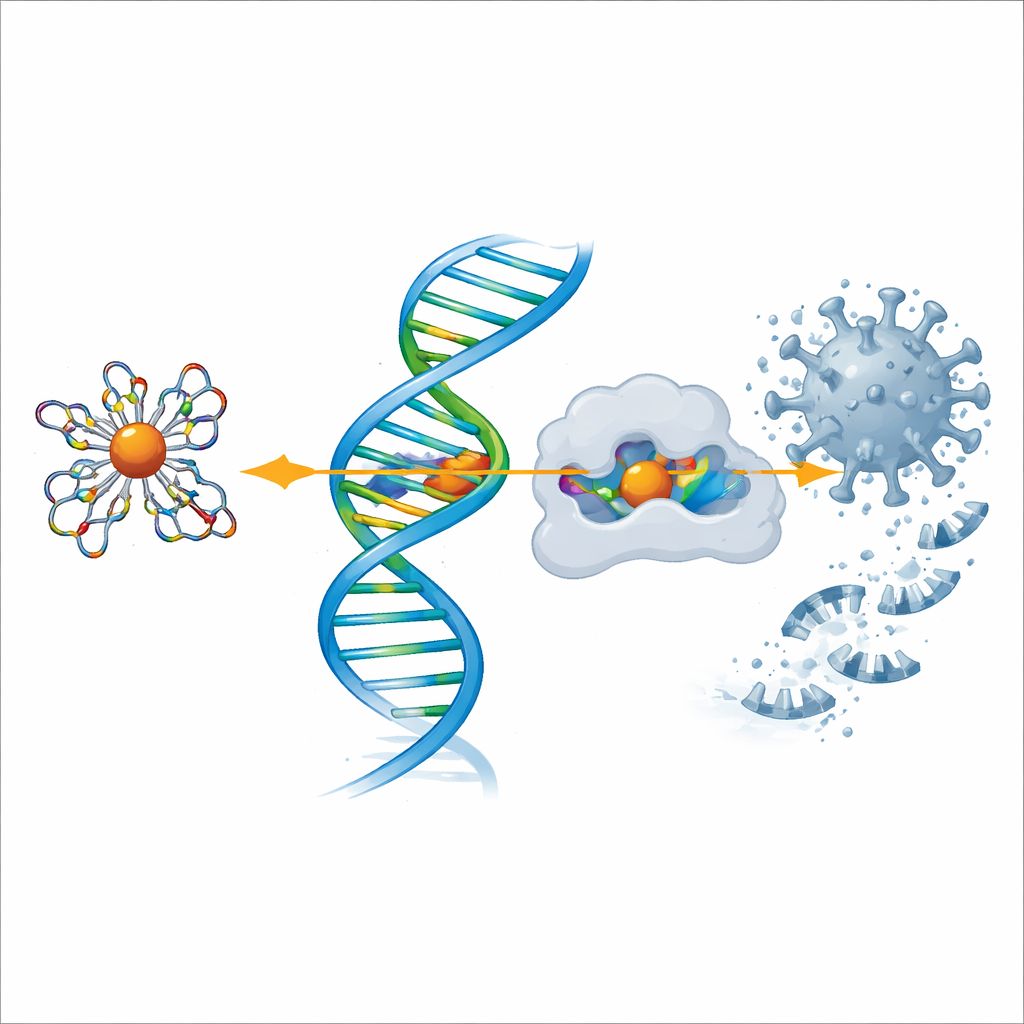
Untersuchung der Wirkung gegen COVID‑19‑ und Schmerz‑Enzyme
Um das antivirale Potenzial zu beurteilen, nutzte das Team Computermodellierung, um den Liganden und jeden Metallkomplex in die dreidimensionalen Formen zweier Schlüsselenzyme zu „docken“: die Hauptprotease von SARS‑CoV‑2, die das Virus zur Zerschneidung seiner Polyproteine verwendet, und Cyclooxygenase‑2 (COX‑2), ein Enzym, das an Schmerz und Entzündung beteiligt ist. Die Simulationen zeigten, dass die Komplexe, insbesondere Kupfer‑ und Zinkkomplexe, gut in die aktiven Taschen dieser Proteine passen und mehrere stabilisierende Wechselwirkungen ausbilden. Je negativer die berechnete Bindungsenergie, desto stärker die vorhergesagte Bindung — und erneut hob sich der Kupferkomplex hervor, dicht gefolgt von Zink und Nickel, was die Laborergebnisse zu entzündungshemmendem und antimikrobiellem Verhalten stützt.
Was das für künftige Arzneien bedeuten könnte
In der Summe zeigt die Arbeit, dass sich ein vertrautes rezeptfreies Medikament in ein vielseitiges chemisches Werkzeug verwandeln lässt, indem man es mit einem gezielt gewählten organischen Partner und dem passenden Metallion verbindet. Unter den vier untersuchten Metallen ergab Kupfer den vielversprechendsten Kandidaten mit starken antibakteriellen, antifungalen, antitumoralen, entzündungshemmenden und rechnerisch vorhergesagten anti‑SARS‑CoV‑2‑Aktivitäten, während Nickel und Zink etwas mildere, aber dennoch bemerkenswerte Effekte zeigten. Zwar liegen diese Ergebnisse derzeit noch auf Labor‑ und Computermodell‑Ebene, doch sie weisen auf eine Strategie hin, bei der Alltagsmedikamente in gezielte Metallkomplexe „aufgerüstet“ werden, die möglicherweise bei niedrigeren Dosen und gegen ein breiteres Krankheitsspektrum wirken als die ursprünglichen Wirkstoffe.
Zitation: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Schlüsselwörter: Ibuprofen‑Derivate, Metall‑Arzneimittel‑Komplexe, Antikrebswirkstoffe, antimikrobielle Therapie, COVID‑19‑Protease