Clear Sky Science · de
Strukturelle Grundlage des Transports von Prostaglandinen und Arzneimitteln über SLCO2A1
Wie ein molekularer Türsteher die Wirkung von Medikamenten und Hormonen formt
Viele Alltagsmedikamente und hormonähnliche Moleküle müssen durch winzige Tore in unseren Zellen, bevor sie wirken können. Diese Arbeit untersucht ein solches Tor — ein Protein namens SLCO2A1, das dabei hilft, starke Signallipide, die Prostaglandine genannt werden, sowie einige gängige Medikamente in Zellen zu transportieren. Durch die Aufklärung der 3D‑Struktur dieses Proteins und der Art, wie es seine Fracht greift, zeigen die Forscher, warum einige Arzneistoffe befördert werden, während andere das Tor blockieren. Diese Einsichten können die sichere Arzneimittelentwicklung und neue Therapien für Erkrankungen mit Entzündungen, Schmerzen, Darmerkrankungen und schlechtem Wundverschluss voranbringen.
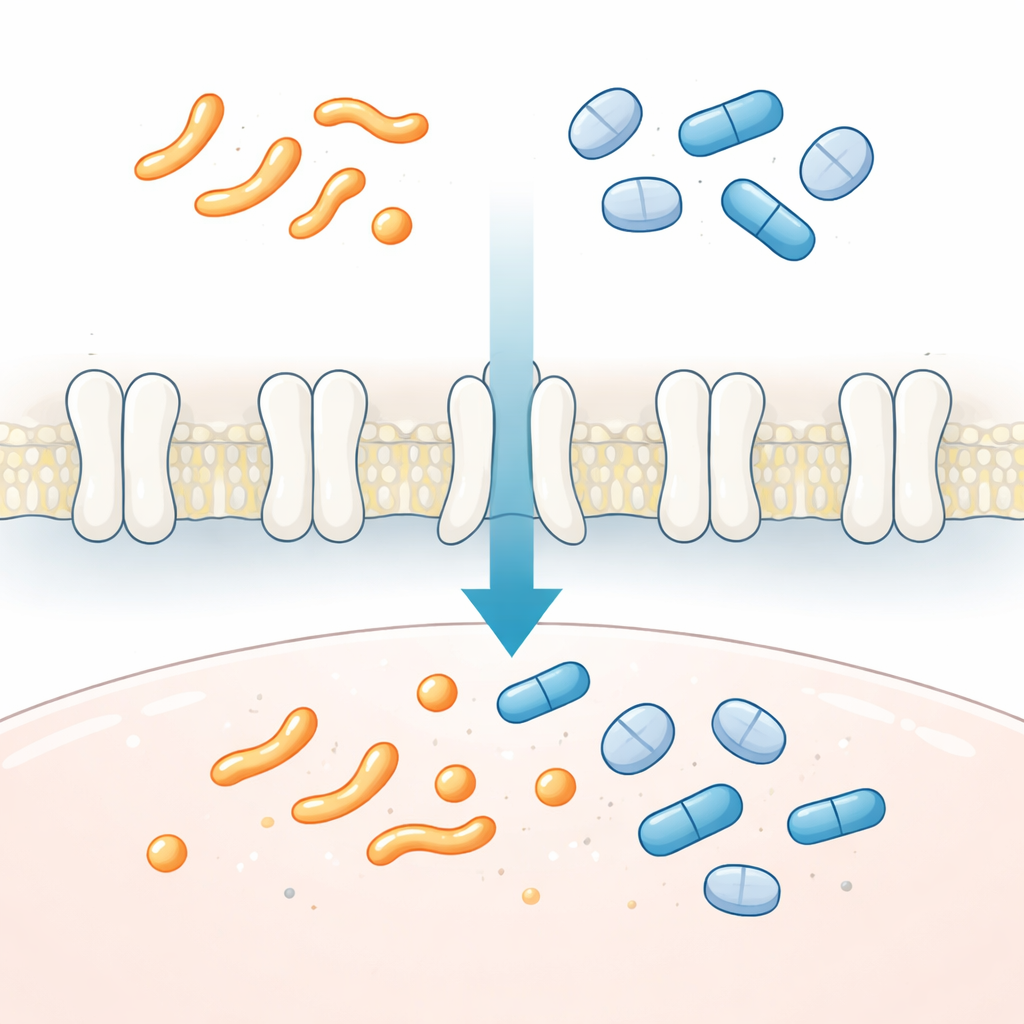
Die Verkehrsregelung des Körpers für Schmerz‑ und Entzündungssignale
Prostaglandine sind kurzlebige, hormonähnliche Fette, die Entzündung, Schmerz, Fieber, Durchblutung und Organentwicklung steuern. Sie wirken lokal und müssen rasch entfernt werden, sobald ihre Aufgabe erfüllt ist. SLCO2A1 sitzt in der Zellmembran und hilft, Prostaglandine und verwandte Moleküle wie Thromboxane aus der umgebenden Flüssigkeit in die Zelle zu holen, wo sie abgebaut werden können. Scheitert dieser Transport, bleiben Prostaglandinspiegel oft erhöht. Erbliche Defekte in SLCO2A1 stehen im Zusammenhang mit seltenen Knochen‑ und Hautüberwucherungen, chronischen Darmerkrankungen und schlechtem Heilungsverhalten von Geschwüren. Da Prostaglandine und viele weitverbreitete Medikamente denselben Weg in Zellen nutzen, ist das Verständnis der Funktion von SLCO2A1 entscheidend, um Arzneimittelwirkungen und Nebenwirkungen im Körper vorherzusagen.
Das Tor in atomarer Detailauflösung sehen
Um herauszufinden, wie SLCO2A1 seine Fracht erkennt und transportiert, verwendete das Team kryogene Elektronenmikroskopie, eine Technik, die eingefrorene Proteine in nahezu atomarer Auflösung darstellt. Sie untersuchten eine eng verwandte Rattenvariante des Transporters, die dem menschlichen sehr ähnelt. Sie hielten Strukturen des Proteins fest, gebunden an zwei natürliche Prostaglandine und vier Medikamente, die gegen Asthma, Bluthochdruck, Entzündung und Parkinson eingesetzt werden. In all diesen Aufnahmen erscheint SLCO2A1 als Bündel aus zwölf membranüberspannenden Helices, die eine zentrale Kavität bilden, die zur Außenseite der Zelle offen ist. Die Prostaglandine liegen tief in dieser Tasche; ihr ringförmiger Kern ruht nahe einer Gruppe wichtiger Aminosäuren, während ihre Fettschwänze in eine überwiegend ölige Rinne einlaufen, die zu ihrer fettliebenden Natur passt.
Der Greifer, der auswählt, was hindurch darf
Durch den Vergleich von Strukturen und lange Computermodelle identifizierten die Forscher Merkmale, die SLCO2A1 erlauben, echte Fracht von ähnlichen Verbindungen zu unterscheiden. Eine positiv geladene Aminosäure, Arginin 561, sowie ein angrenzendes Tryptophan und Phenylalanin bilden einen wichtigen „Greifer“ für das negativ geladene Ende der Prostaglandine. Wenn das Team diese Reste veränderte, scheiterte der Transport weitgehend, was die Bedeutung dieses Kontakts unterstreicht. Die umgebende Kavität ist überwiegend hydrophob und begünstigt ölige, membranliebe Moleküle; sie enthält außerdem ein „Band“, das während der Formänderung des Proteins als Drehachse wirkt. Zwei Wirkstoffe, Zafirlukast und Losartan, werden tatsächlich transportiert, weil sie imitieren, wie Prostaglandine eine negative Gruppe dem Arginin präsentieren und dabei dieselben hydrophoben Flächen nutzen. Im Gegensatz dazu binden das entzündungshemmende Fentiazac und das Parkinson‑Medikament Tolcapon weniger eng und stabilisieren die richtige Lage nicht, sodass sie die Stelle blockieren, statt durchgereicht zu werden.
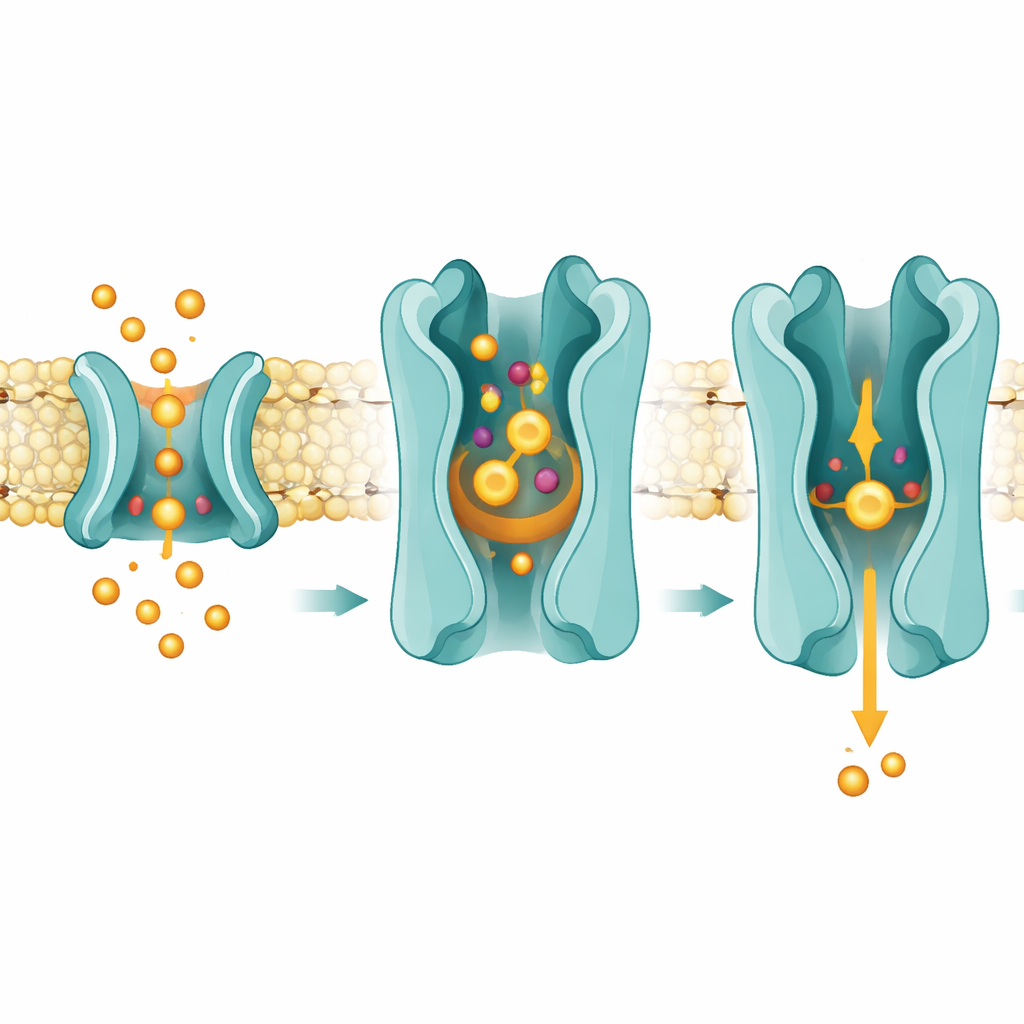
Eine Seitentür durch die Membran
Die Strukturen deuten außerdem darauf hin, dass Prostaglandine SLCO2A1 nicht aus dem freien Wasser erreichen, sondern seitlich durch den fetthaltigen Membrankern gleiten. Die Forscher beobachteten Dichten, die zu lipidähnlichen Molekülen passen und in einer lateralen Öffnung zwischen zwei Helices liegen, direkt oberhalb der Bindestelle der Prostaglandine. Krankheitsverursachende Mutationen und funktionelle Tests benennen diese Region als entscheidend für den Transport. Der vorgeschlagene Mechanismus lautet, dass Prostaglandine zunächst in der äußeren Membranschicht löslich werden und dann durch diese Öffnung in den Transporter gleiten. Einmal im zentralen Fach gebunden, stören sie eine konservierte Salzbrücke zwischen Arginin 561 und einer Glutamat‑Rest, was wiederum hilft, den Transporter von einer nach außen offenen zu einer nach innen offenen Form schwingen zu lassen und so das Prostaglandin Richtung innerer Membran und Zellinneres freizusetzen.
Warum das für Medikamente und Krankheiten wichtig ist
Für Laien lautet die Hauptbotschaft: SLCO2A1 wirkt als fein abgestimmtes Tor, das steuert, wie stark chemische Signale für Schmerz, Fieber und Entzündung abgeschaltet werden und wie bestimmte Medikamente in Zellen gelangen. Diese Studie zeigt auf molekularer Ebene, wie das Tor Prostaglandine erkennt und warum nur manche Medikamente mithilfe dieses Systems transportiert werden, während andere die Tür verkeilen. Durch die Kartierung der entscheidenden Kontaktpunkte und der seitlichen Eintrittsroute durch die Membran liefert die Arbeit einen Bauplan, um neue Arzneimittel zu entwickeln, die entweder dieses Transportsystem effizient nutzen oder es gezielt und kontrolliert blockieren. Letztlich könnte dieses Wissen Therapien für entzündliche Erkrankungen, darmerkrankungen im Zusammenhang mit Prostaglandinungleichgewicht und Medikationsregime verbessern, bei denen Wechselwirkungen mit dem Transporter bisher zu unvorhersehbaren Reaktionen führen.
Zitation: Joshi, C., Deme, J.C., Nakamura, Y. et al. Structural basis for prostaglandin and drug transport via SLCO2A1. Nat Commun 17, 2285 (2026). https://doi.org/10.1038/s41467-026-70227-3
Schlüsselwörter: Prostaglandintransport, Arzneimitteltransporter, SLCO2A1, Membranproteine, Cryo‑EM-Struktur