Clear Sky Science · de
Katalytische asymmetrische Funktionalisierung von Bicyclo[1.1.0]butan‑Boronsäureestern ermöglicht durch 1,2‑Sauerstoffwanderung
Warum winzige quadratische Ringe wichtig sind
Chemiker bauen gern neue Arzneistoffe und Materialien, indem sie kleine molekulare Bausteine zusammenfügen, ähnlich wie mit Lego‑Steinen. Viergliedrige Kohlenstoffringe, sogenannte Cyclobutane, sind besonders wertvoll, weil sie viel Energie und räumliche Information auf kleinem Raum speichern — Eigenschaften, die das Verhalten eines Wirkstoffs im Körper beeinflussen können. Dieser Artikel beschreibt eine neue Methode, solche Ringe in sehr kontrollierter, „einhändiger“ (chiral) Form herzustellen, indem eine clevere Reaktion ein sauerstoffhaltiges Fragment dazu zwingt, von einem Atom zum nächsten zu springen. Die Arbeit eröffnet Wege, komplexere und präzisere Moleküle für die Pharmaforschung und fortgeschrittene Materialien zu entwerfen.
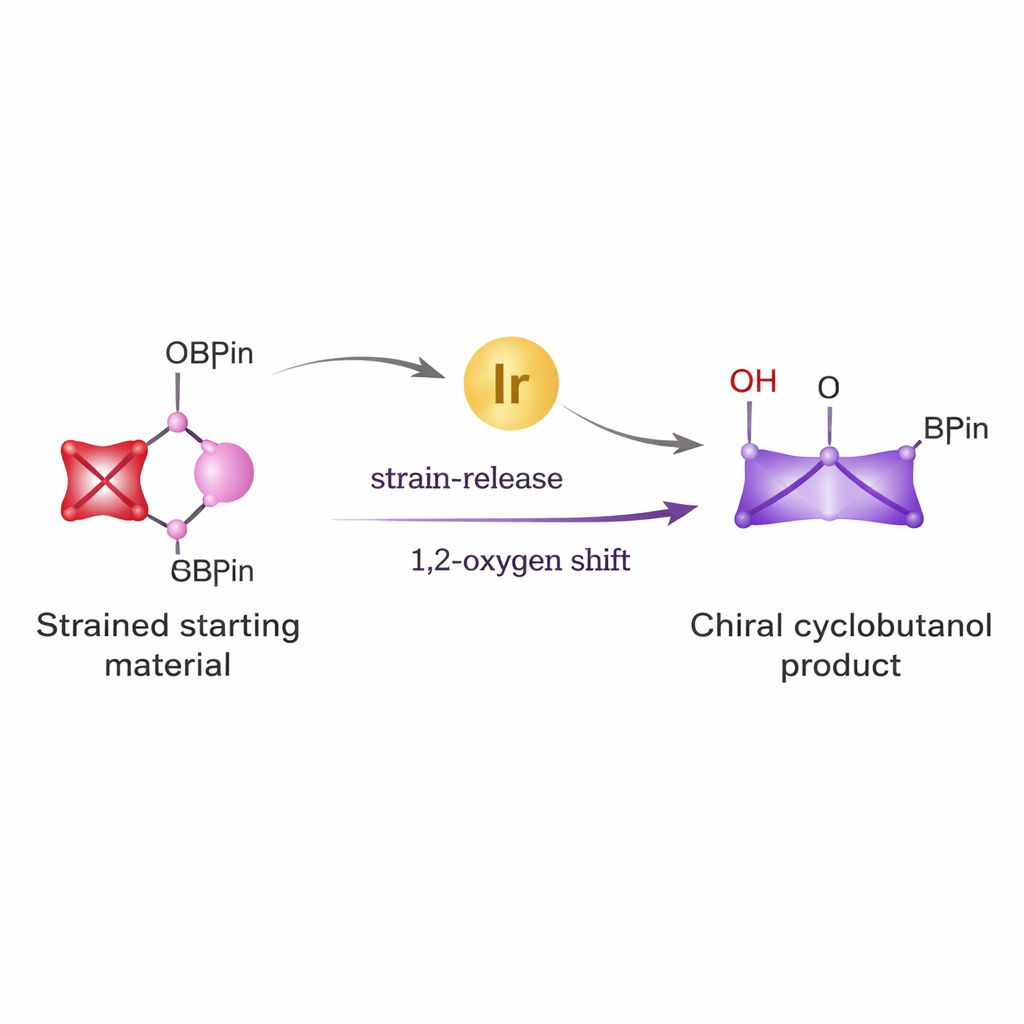
Von einfachen Bausteinen zu leistungsfähigen Ringen
Cyclobutane finden sich in einer Reihe von antiviralen Mitteln, Krebswirkstoffkandidaten und anderen bioaktiven Molekülen. Sie mit der genau benötigten dreidimensionalen Anordnung für die Medizin herzustellen, war jedoch schwierig. Traditionelle Routen erfordern oft aggressive Reagenzien und liefern Gemische aus Spiegelbildprodukten, die schwer zu trennen sind. Die Autoren wollten dieses Problem lösen, indem sie zwei kraftvolle Konzepte kombinierten: die ungewöhnliche Reaktivität eines winzigen, stark gespannten Rings namens bicyclo[1.1.0]butan und die Vielseitigkeit von Boronsäureestern, einer gut etablierten Reagenzienfamilie, die in Kopplungsreaktionen zur Ausbildung von Kohlenstoff–Kohlenstoff‑Bindungen häufig eingesetzt wird.
Aus einem Nachteil einen neuen Reaktionsweg machen
In typischen metallkatalysierten Kupplungsreaktionen bilden Boronsäureester ein Zwischenprodukt mit einem Alkoxid (einer sauerstoffbasierten Base). Dieses Komplex folgt fast immer dem vertrauten Pfad der Transmetallierung, die dann direkt zu neuen Kohlenstoff–Kohlenstoff‑ oder Kohlenstoff–Halogen‑Bindungen führt. Dieser „Standard“‑Weg erschwerte es, andere Möglichkeiten zu erkunden, etwa die Wanderung der Sauerstoffgruppe selbst. Das Team erkannte, dass, wenn man von einem ringgespannten bicyclo[1.1.0]butan‑Boronsäureester ausgeht, die im kleinen Ring gespeicherte Spannung den üblichen Pfad außer Kraft setzen könnte. Indem sie dieses gespannte System mit einem Iridiumkatalysator und einem sorgfältig ausgewählten chiralen Liganden kombinierten, hofften sie, den Sauerstoff kontrolliert zum Wandern zu bewegen, während sich der Ring öffnet und wieder zu einem Cyclobutan schließt.
Ein schrittweiser Tanz, gelenkt durch Spannung
Experimente bestätigten, dass diese Strategie funktioniert. Mit Lithiumalkoxiden, die aus einer großen Vielfalt von Alkoholen gewonnen wurden — darunter Zucker, Terpene, Steroide und einfache aliphatische Alkohole — verwandelten die Autoren bicyclo[1.1.0]butan‑Boronsäureester in cis‑Cyclobutanol‑Produkte mit hoher Ausbeute und ausgezeichneter Kontrolle über die Chiralität. Der Iridiumkatalysator bildet zunächst aus einem allylischen Carbonatpartner einen reaktiven Allylkomplex. Dieser Komplex greift dann das gespannte bicyclo[1.1.0]butan‑System an und bildet beim Öffnen des winzigen Rings eine neue Kohlenstoff–Kohlenstoff‑Bindung. Entscheidend ist, dass das resultierende borhaltige Zwischenprodukt nicht sofort der üblichen Transmetallierung folgt, sondern eine subtile Rotation der Kohlenstoff–Bor‑Bindung durchläuft, die die angehängte Sauerstoffgruppe so positioniert, dass sie sauber zu einem benachbarten Kohlenstoffatom verschieben kann. Diese 1,2‑Sauerstoffwanderung fixiert die gewünschte cis‑Anordnung im neuen Cyclobutanring.
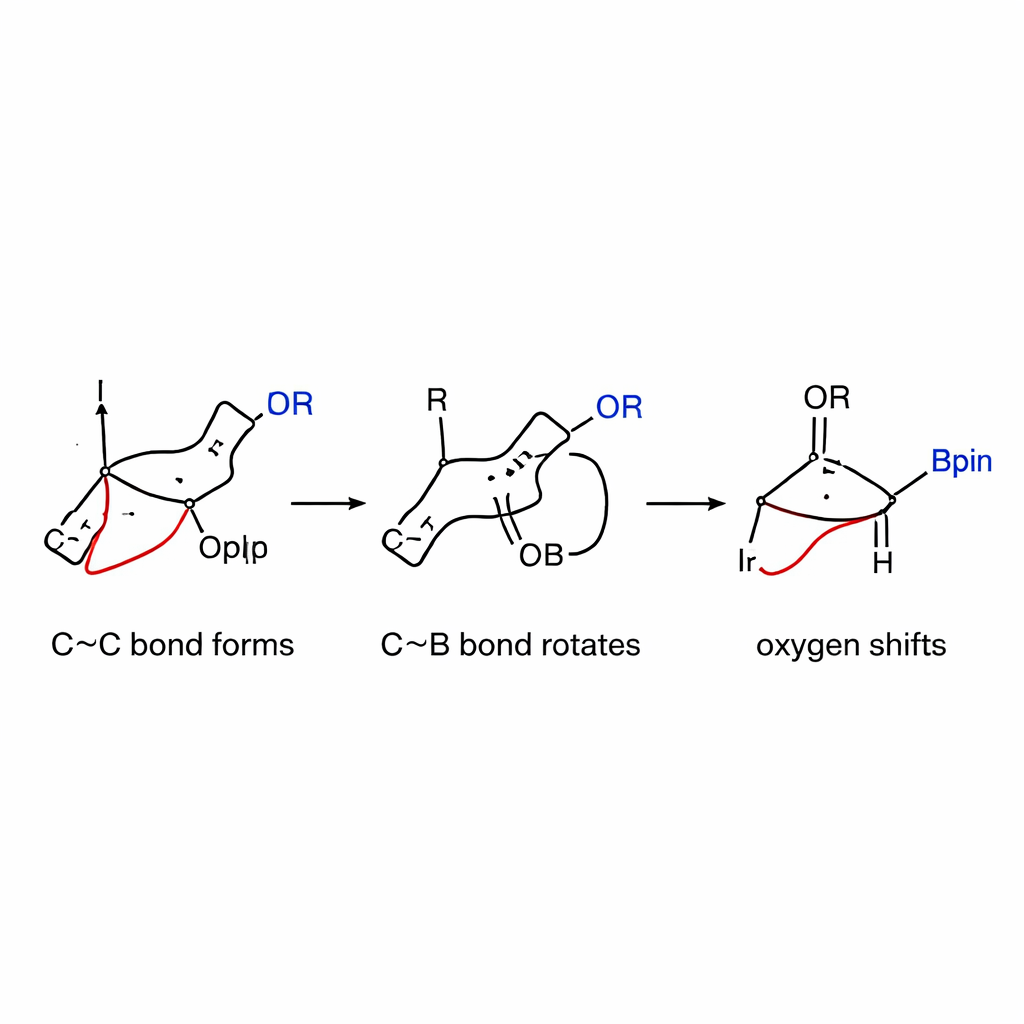
Ein Blick unter die Haube des Mechanismus
Um zu verstehen, warum die Reaktion so selektiv ist, kombinierten die Autoren kinetische Messungen mit detaillierten Computersimulationen. Sie fanden heraus, dass der langsame, geschwindigkeitsbestimmende Schritt die anfängliche Kohlenstoff–Kohlenstoff‑Bindungsbildung zwischen der Iridium–Allyl‑Spezies und dem gespannten Boronatkomplex ist, nicht die frühere Aktivierung des allylischen Carbonats. Elektronische Untersuchungen zeigten, dass Allylpartner, die positive Ladung stabilisieren, schneller reagieren — ein Hinweis auf einen Mechanismus mit einem teilweise geladenen Zwischenzustand. Rechnungen zeigten ferner, dass die Rotation um die Kohlenstoff–Bor‑Bindung — früher als schwierig angesehen — in diesem System eine überraschend niedrige Energiebarriere aufweist, dank der im Ring gespeicherten Spannung. Sobald die Rotation die Sauerstoffgruppe ausgerichtet hat, verläuft die 1,2‑Verschiebung glatt und bevorzugt das cis‑Produkt statt der häufiger auftretenden trans‑Form.
Neue Werkzeuge zur Gestaltung zukünftiger Arzneimittel
Über den rein mechanistischen Nachweis hinaus liefert die Reaktion vielseitige Produkte. Die Cyclobutanole behalten eine Boronsäureester‑Einheit, die mit etablierten Methoden in viele andere Funktionsgruppen überführt werden kann. Die Autoren zeigten zahlreiche „Spät‑Stadium“‑Modifikationen, wie Hydrierung, Oxidation, Olefinmetathese und weitere Kupplungen, wobei die präzise dreidimensionale Form des Rings erhalten bleibt. Einfach ausgedrückt verwandelt diese Arbeit einen einst problematischen Nebenpfad — die Sauerstoffmigration in Boronatkomplexen — in ein kraftvolles synthetisches Werkzeug. Durch das Nutzen von Ringspannung und einem feinabgestimmten Iridiumkatalysator bieten die Forscher Chemikern eine zuverlässige Methode, komplexe, chirale Cyclobutane herzustellen, die in der nächsten Generation von Arzneimitteln und advanceden molekularen Materialien eine Schlüsselrolle spielen könnten.
Zitation: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Schlüsselwörter: Cyclobutan, Organoboron‑Chemie, asymmetrische Katalyse, Bicyclobutan, Sauerstoffmigration