Clear Sky Science · de
Tumorassoziierte CD19+-Makrophagen erzeugen ein immunsuppressives Mikroumfeld beim hepatozellulären Karzinom
Warum die Verteidiger des Körpers manchmal dem Leberkrebs helfen
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, zum Teil weil Tumoren das Immunsystem des Körpers gegen ihn selbst wenden können. Diese Studie deckt eine überraschende Untergruppe von Immunzellen in Lebertumoren auf, die statt Krebs zu bekämpfen diesen aktiv beim Verstecken und Wachsen unterstützen. Zu verstehen, wer diese „Verräter“-Zellen sind und wie sie funktionieren, eröffnet neue Wege, die Immuntherapie für Patientinnen und Patienten mit hepatozellulärem Karzinom, der häufigsten Form von Leberkrebs, wirksamer zu machen.
Eine spezielle Gruppe von Immunzellen innerhalb von Tumoren
Die Autorinnen und Autoren konzentrierten sich auf tumorassoziierte Makrophagen, Immunzellen, die normalerweise Erreger und Zellreste aufnehmen, sich aber in Tumoren häufig korrumpieren. Durch die Analyse von Lebertumorproben vieler Patientinnen und Patienten entdeckten sie eine eigene Untergruppe von Makrophagen, die ein Oberflächenmolekül namens CD19 tragen, das üblicherweise bei B‑Zellen vorkommt und nicht bei Makrophagen. Diese CD19-positiven Makrophagen waren in Lebertumoren deutlich häufiger als in benachbartem gesundem Lebergewebe oder im Blut und zeigten sich auch in mehreren anderen soliden Tumoren angereichert. Einzelzellanalysen bestätigten, dass es sich um echte Makrophagen mit einem einzigartigen Gen‑ und Proteinprofil handelt und nicht um fehlidentifizierte B‑Zellen.
Wie diese Zellen ein tumorförderliches Umfeld schaffen
Patientinnen und Patienten, deren Tumoren viele CD19-positive Makrophagen enthielten, wiesen tendenziell größere, aggressivere Tumoren und kürzere Überlebenszeiten auf. Tumorproben mit hoher Dichte dieser Zellen zeigten weniger krebsabtötende CD8‑T‑Zellen und mehr regulatorische T‑Zellen — ein Muster, das typisch ist für ein stark immunsuppressives Umfeld. In Mausmodellen beschleunigte das Zufügen von CD19-positiven Makrophagen das Tumorwachstum und reduzierte das Vorkommen hilfreicher T‑Zellen, während andere immunsuppressive myeloide Zellen zunahmen. Wichtig ist, dass die Forschenden mit gentechnisch veränderten T‑Zellen, die CD19 erkennen, diese Makrophagen selektiv eliminieren konnten und die Lebertumoren schrumpften — selbst in Mäusen ohne normale B‑Zellen — was die Makrophagen selbst als therapeutisches Zielpunkt klarstellte.
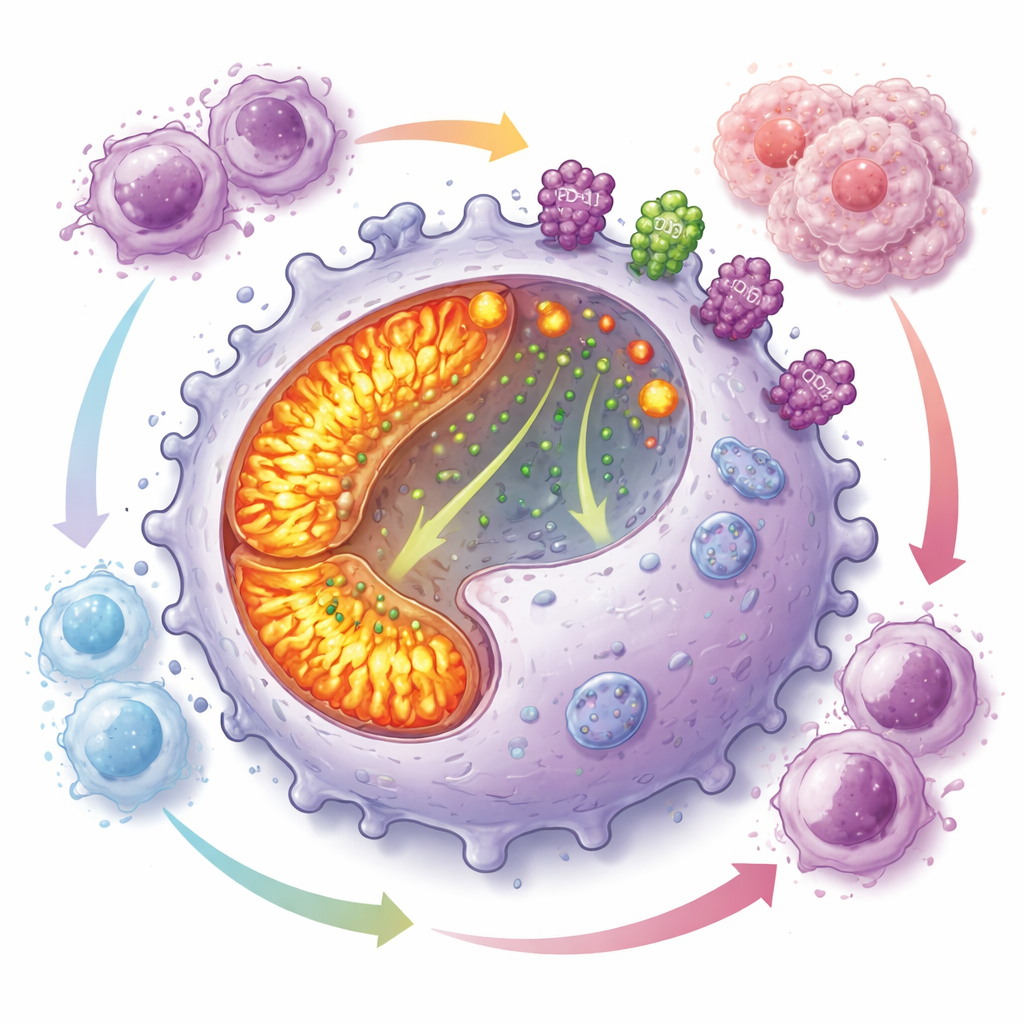
Ein energiehungriges Programm, das Immunangriffe abmildert
Tiefergehende Untersuchungen zeigten, dass CD19-positive Makrophagen ihre inneren „Kraftwerke“ mit hoher Leistung betreiben. Ihre Mitochondrien — die Organellen zur Energiegewinnung — waren zahlreicher und aktiver als in anderen Makrophagen, mit gesteigerter oxidative Phosphorylierung und erhöhten reaktiven Sauerstoffspezies. Trotz dieses energetischen Zustands hatten diese Zellen eine schlechte Fähigkeit zur Phagozytose, teilten sich aber schnell, was zu ihrer Anreicherung in Tumoren beitrug. Gleichzeitig zeigten sie hohe Oberflächenpegel von PD-L1 und CD73 — zwei Moleküle, die T‑Zell‑Antworten unterdrücken und Adenosin erzeugen, ein kleines Molekül, das die Immunität stark dämpft. Ko‑Kultur-Experimente zeigten, dass diese Makrophagen das Wachstum verschiedener T‑Zell‑Typen stark hemmen.
Der Schalter hinter den verräterischen Makrophagen
Die Forschenden identifizierten einen Transkriptionsfaktor namens PAX5 als zentralen Treiber dieses schädlichen Makrophagenprogramms. PAX5 ist vor allem für die Steuerung der B‑Zell‑Entwicklung bekannt, war hier jedoch hochaktiv in CD19-positiven Makrophagen. Das Erzwingen von PAX5‑Expression in makrophagenähnlichen Zellen förderte die Mitochondrienbiogenese, steigerte die Energieproduktion und erhöhte die Protein‑ — nicht jedoch mRNA‑ — Spiegel von PD-L1, CD73 und CD19. Mechanistische Experimente zeigten, dass PAX5 Calcium in die Mitochondrien zieht, wodurch das Calcium im Zellplasma abgesenkt wird und ein wichtiger Regulator namens TFEB am Eintritt in den Zellkern gehindert wird. Wird TFEB zurückgehalten, sinken Lysosomenproduktion und -funktion, sodass Proteine wie PD-L1 und CD73 nicht mehr effizient abgebaut werden und stattdessen an der Zelloberfläche akkumulieren, was die Immunsuppression verstärkt.
Vom Befund zu besseren Behandlungsoptionen
Da diese Makrophagen stark von CD73‑Aktivität und mitochondrialem Stoffwechsel abhängig sind, prüften die Autorinnen und Autoren, ob die Blockade dieser Wege die Wirksamkeit der Immuntherapie verbessern könnte. In Mausmodellen des Leberkrebses führte die Kombination von PD‑L1‑Blockade mit entweder CD73‑Antikörpern oder einem CD73‑Inhibitor zu kleineren Tumoren, mehr einwandernden T‑Zellen und geringerer Tumorzellproliferation. Ebenso verbesserte das Kombinieren von PD‑L1‑Antikörpern mit einem Inhibitor der mitochondrialen oxidativen Phosphorylierung die Tumorkontrolle und förderte das Eindringen von Immunzellen in die Tumoren. Auffällig war, dass diese Vorteile bei Mäusen, deren Makrophagen kein PAX5 exprimierten, verschwanden — ein Beleg dafür, dass die Medikamenteneffekte an die Ausschaltung des CD19‑positiven, PAX5‑gesteuerten Makrophagenprogramms gebunden sind. Zusammen deuten die Ergebnisse darauf hin, dass das selektive Anvisieren dieser Makrophagenuntergruppe — etwa durch CD19‑gerichtete Zelltherapien, CD73‑Hemmung oder metabolische Wirkstoffe — helfen könnte, einen immunologisch „kalten" Lebertumor in einen Tumor zu verwandeln, der deutlich besser auf bestehende Checkpoint‑Blockade‑Therapien anspricht.
Zitation: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Schlüsselwörter: hepatozelluläres Karzinom, tumorassoziierte Makrophagen, Immuntherapie, PD-L1 und CD73, mitochondriale Stoffwechsel