Clear Sky Science · de
Heterobifunktionelle proteomimetische Polymere für den gezielten Abbau von MYC und KRAS
Neue Werkzeuge, um die hartnäckigsten Krebsproteine zu Fall zu bringen
Viele der gefährlichsten krebstreibenden Proteine, etwa MYC und KRAS, gelten lange Zeit als „nicht druggable“, weil Arzneistoffe sich nur schwer an sie anlagern können. Diese Studie stellt eine neue Art weicher, synthetischer Materialien vor – sogenannte HYDRAC-Polymere –, die diese schwer fassbaren Proteine greifen und zur Müllentsorgungsanlage der Zelle schicken können. Für Leser bietet diese Arbeit einen Einblick, wie Chemie und Nanotechnologie Behandlungsoptionen für Krebserkrankungen eröffnen könnten, die resistent gegen traditionelle Medikamente sind.
Ein flexibles Gerüst statt einer einzelnen Pille
Die meisten gezielten Krebsmedikamente sind kleine Moleküle, die in Taschen auf der Proteinoberfläche passen, ähnlich wie ein Schlüssel ins Schloss. Proteine wie MYC sind jedoch flexibel und besitzen kaum geeignete Taschen, während KRAS oft so mutiert, dass klassische Medikamente versagen. Die Autoren entwarfen stattdessen lange, kettenartige Polymere aus wiederholten Bausteinen. Entlang dieser Ketten befestigten sie zwei Arten von Komponenten: kurze proteinbindende Segmente, die ein Ziel wie MYC oder RAS erkennen, und „Degron“-Segmente, die die Entsorgungsmaschinerie der Zelle rekrutieren. Weil viele Kopien jeder Komponente dieselbe Kette schmücken, kann ein einziges HYDRAC-Molekül gleichzeitig mehrere Proteine und Enzyme erreichen – etwas, das mit einem einzelnen, starren Arzneistoff nur schwer zu erreichen ist.
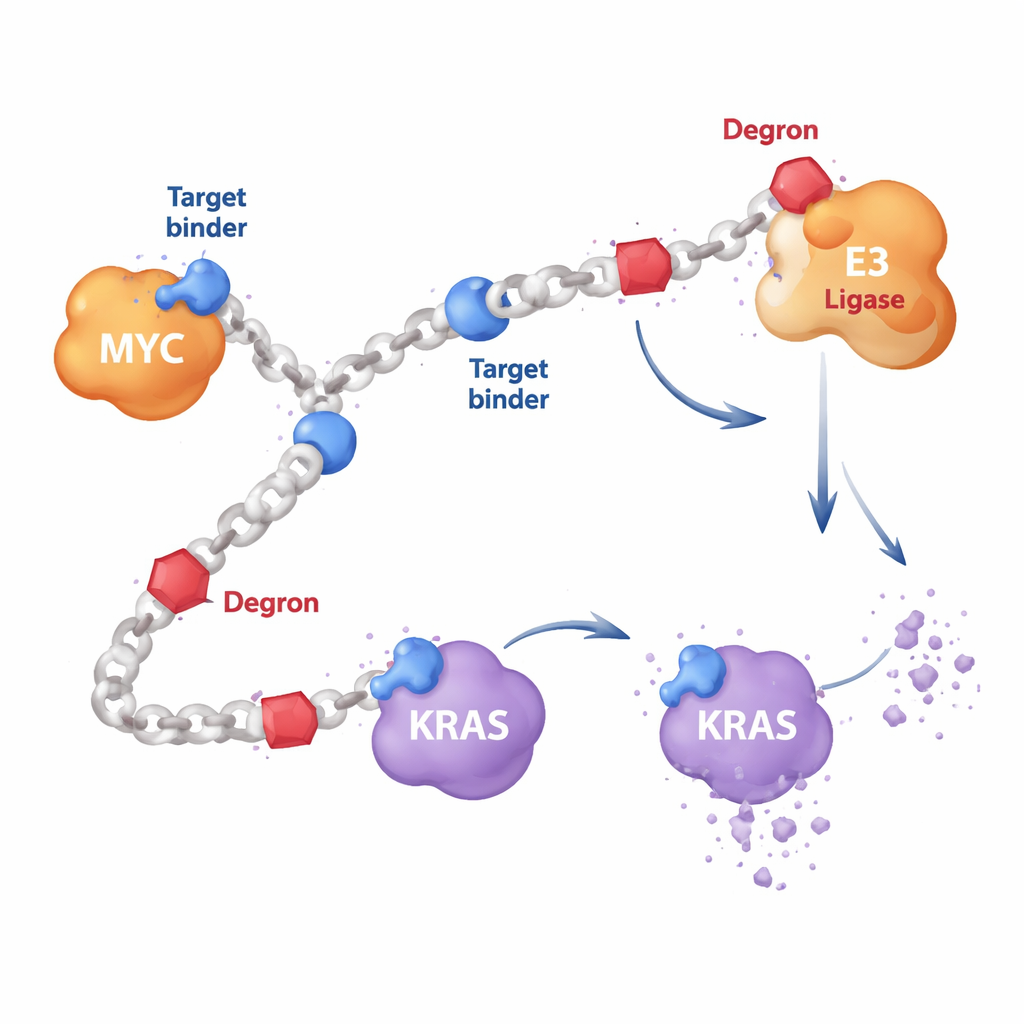
Zellen beibringen, MYC zu zersetzen
Als ersten Test konzentrierten sich die Forschenden auf MYC, einen Masterregler, der in vielen Krebsarten Wachstum antreibt, aber jahrzehntelang direkte Angriffe widerstanden hat. Sie bauten HYDRAC-Polymere, die ein bekanntes MYC-bindendes Peptid neben einem einfachen Degron-Motiv tragen, das Proteine für den Abbau durch das Proteasom der Zelle kennzeichnet – ihren wichtigsten Proteinzerkleinerer. In Reagenzgläsern falten sich diese Polymere zu kompakten, proteinähnlichen Formen und banden stark an MYC, nicht jedoch an unbeteiligte Proteine. In Krebszellen gelangten die HYDRACs leicht hinein, störten MYC-gesteuerte Genprogramme und lösten den Zelltod aus – Effekte, die davon abhingen, dass sowohl die Zielerkennungs- als auch die Degron-Komponenten auf derselben Polymerkette vorhanden waren.
Von Zellkultur zu schrumpfenden Tumoren
Innerhalb der Zellen führte die Behandlung mit HYDRACs zu einem starken Abfall der MYC-Proteinkonzentration, ohne dass MYC-mRNA reduziert wurde, was auf echten Abbau statt bloßes Herunterregeln hinweist. Die Blockade des Proteasoms oder wichtiger Enzyme, die bestimmte Abbauwege aktivieren, stellte MYC-Spiegel wieder her und zeigte damit, dass die Polymere durch Umlenkung der zellulären Entsorgungssysteme wirken. Proteomweite Analysen zeigten, dass nur sehr wenige andere Proteine betroffen waren, was auf eine bemerkenswerte Selektivität hindeutet. In Mausmodellen mit MYC-getriebenen Tumoren reichern sich fluoreszenzmarkierte HYDRACs nach Injektion bevorzugt in den Tumoren an und bleiben dort über Tage. Wiederholte Gaben verlangsamten das Tumorwachstum ohne nennenswerten Gewichtsverlust oder offensichtliche Gewebeschäden; Tumorproben zeigten weniger teilende Zellen und mehr Anzeichen programmierter Zellnekrose.
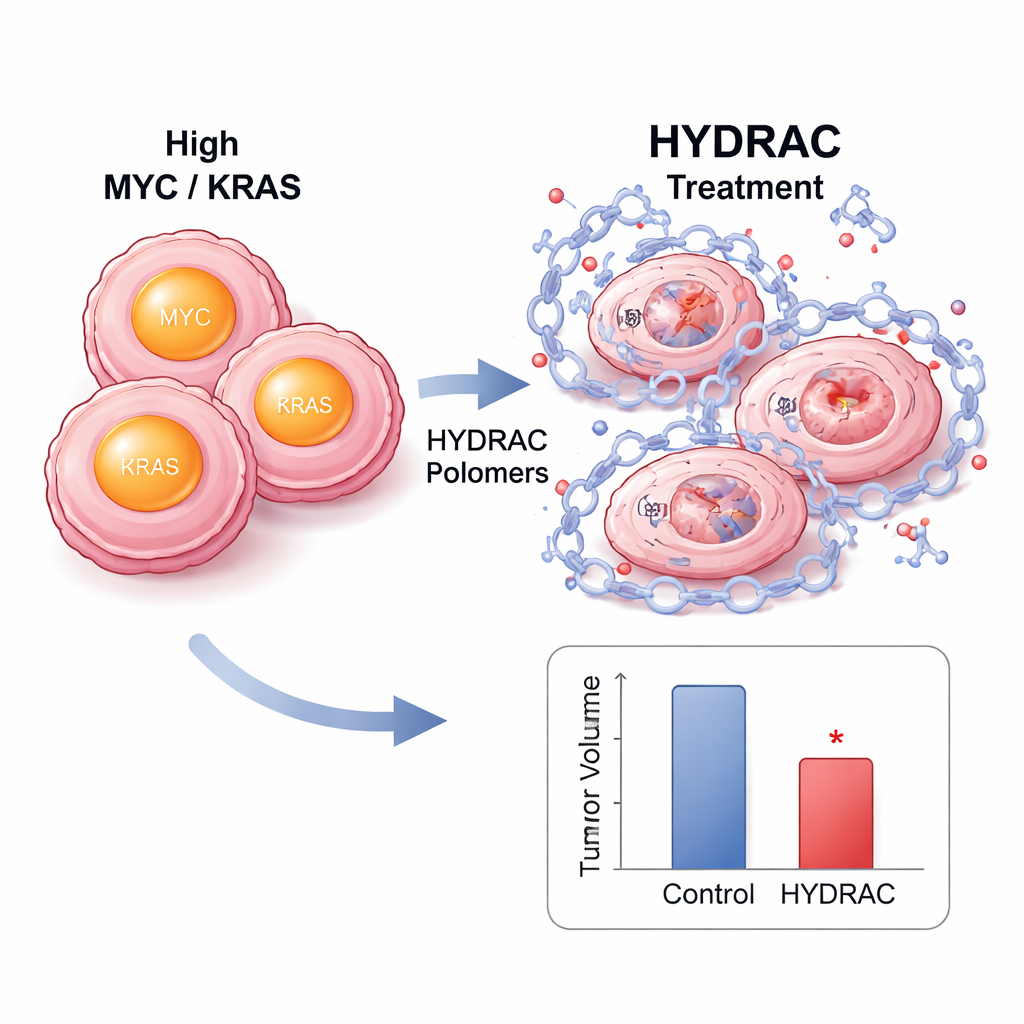
Eine Plug-and-Play-Plattform für viele Krankheitsziele
Eine Stärke des HYDRAC-Ansatzes liegt darin, dass seine Seitenketten wie austauschbare Teile getauscht werden können. Das Team ersetzte das ursprüngliche Degron durch andere Rekrutierungselemente, die verschiedene zelluläre Enzyme ansprechen, einschließlich solcher, die das Medikament Thalidomid erkennen. Jede Version degradierte MYC nur dann, wenn das jeweils vorgesehene Enzym vorhanden und funktionstüchtig war, was bestätigt, dass die Polymere so abgestimmt werden können, dass sie unterschiedliche zelluläre Routen nutzen. Zur Prüfung der Allgemeingültigkeit bauten die Forschenden anschließend RAS-zielende HYDRACs mithilfe eines Peptids, das RAS-Proteine erkennt. Diese Konstrukte bauten mutiertes KRAS in zwei verschiedenen Krebszelllinien erfolgreich ab und deuten auf ein „Pan-KRAS“-Potenzial hin, das nicht von einer spezifischen Mutation abhängt – ein wichtiger Schritt für Krebsarten, in denen viele KRAS-Varianten nebeneinander existieren.
Warum das für die künftige Krebsbehandlung wichtig ist
Diese Arbeit führt HYDRACs als neue Klasse programmierbarer Materialien ein, die nicht nur problematische Proteine blockieren, sondern Zellen dabei helfen, sie zu löschen. Indem viele Ziel- und Abbaueinheiten auf einem flexiblen Polymer kombiniert werden, umgehen HYDRACs die Gestaltungsgrenzen traditioneller Kleinmolekülmedikamente und PROTACs, die typischerweise nur je eine Einheit tragen können. Obwohl noch viel zu tun ist, bevor diese Materialien in die Klinik gelangen, legen die Ergebnisse in MYC- und KRAS-getriebenen Modellen nahe, dass lange als „undruggable“ betrachtete Krebsproteine tatsächlich verwundbar sein könnten, wenn Medizin eher wie eine maßgeschneiderte molekulare Bürste als wie eine einzelne kleine Pille gedacht wird.
Zitation: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Schlüsselwörter: gezielte Proteinabbausteuerung, MYC, KRAS, Polymertherapeutika, Krebs-Nanomedizin