Clear Sky Science · de
Integrierte epigenomische Landkarte von Alzheimer-Geweben enthüllt oligodendrozytäre molekulare Störungen, die mit Tau assoziiert sind
Warum diese Hirnforschung wichtig ist
Die Alzheimer-Krankheit ist vor allem für Gedächtnisverlust und die Anhäufung zweier problematischer Proteine im Gehirn bekannt: Amyloid und Tau. Dennoch zeigen Menschen mit Alzheimer sehr unterschiedliche Schadensmuster, selbst bei gleicher Diagnose. Diese Studie stellt eine zentrale Frage: Welche Schalter innerhalb von Gehirnzellen beeinflussen, wie stark sich diese schädlichen Proteine ansammeln und wie sie verschiedene Zelltypen betreffen? Indem die Forschenden chemische Markierungen auf der DNA in hunderten Gehirnen untersuchten, entdeckten sie eine überraschende Verbindung zwischen Tau und den Zellen, die das „Verdrahtungssystem“ des Gehirns funktionstüchtig machen.
Chemische Markierungen auf der DNA als verborgene Schalter
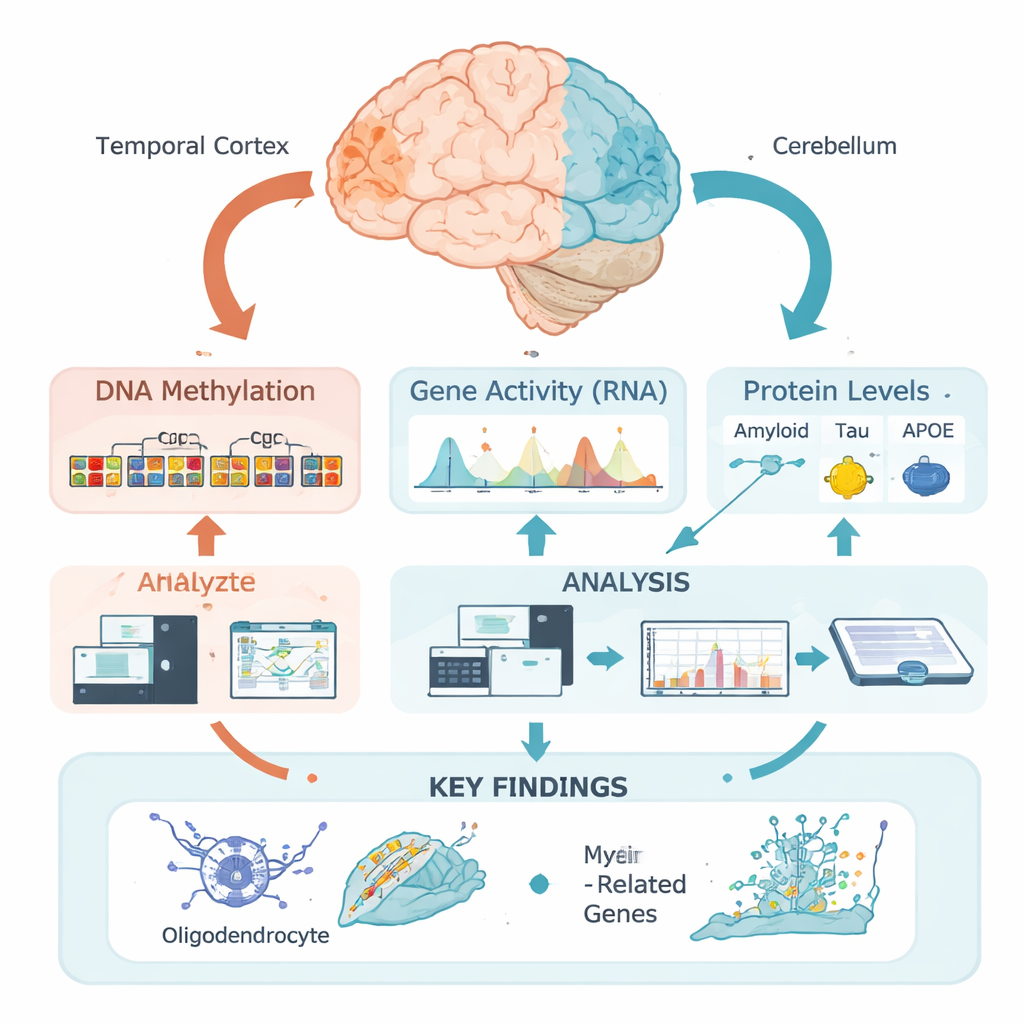
Unsere DNA enthält die grundlegenden Anweisungen zum Aufbau und Betrieb von Gehirnzellen, doch diese Anweisungen werden durch epigenetische Markierungen gesteuert—chemische Tags, die nahegelegene Gene hoch- oder herunterregeln können, ohne den genetischen Code zu verändern. Eine der wichtigsten Markierungen ist die DNA-Methylierung, bei der kleine chemische Gruppen an spezifische DNA-Stellen binden. Statt einzelne Stellen isoliert zu betrachten, verwendete dieses Team einen neuen „regionalen“ Ansatz: Sie gruppierten viele benachbarte Stellen zu funktionellen Zonen auf Grundlage der DNA-Packung im Temporallappen, einer stark von Alzheimer betroffenen Region, und dem Kleinhirn, das relativ verschont bleibt. So konnten sie biologisch fragen, an welchen Orten sich Methylierungsmuster in Beziehung zu Krankheitsmerkmalen ändern.
Verknüpfung von DNA-Markierungen mit Alzheimer-Proteinen
Die Forschenden analysierten Hirngewebe von 472 Personen mit postmortaler Alzheimer-Bestätigung. Für jede Probe aus dem Temporallappen maßen sie detaillierte Mengen von Amyloid, Tau und APOE-Proteinen in verschiedenen biochemischen Formen sowie klassische mikroskopische Scores für Amyloid-Plaques und Tau-Fibrillen. Anschließend führten sie epigenomweite Assoziationsstudien durch, um zu prüfen, ob regionale DNA-Methylierungsniveaus mit diesen Messungen zusammenhängen. Auffällig war, dass nahezu alle starken Assoziationen nicht mit Amyloid, sondern mit Tau verknüpft waren—insbesondere mit gesamtem löslichem Tau und einer membrangebundenen, phosphorylierten (chemisch veränderten) Form, die als besonders toxisch gilt.
Ein starkes Signal in den Zellen der Gehirnverdrahtung
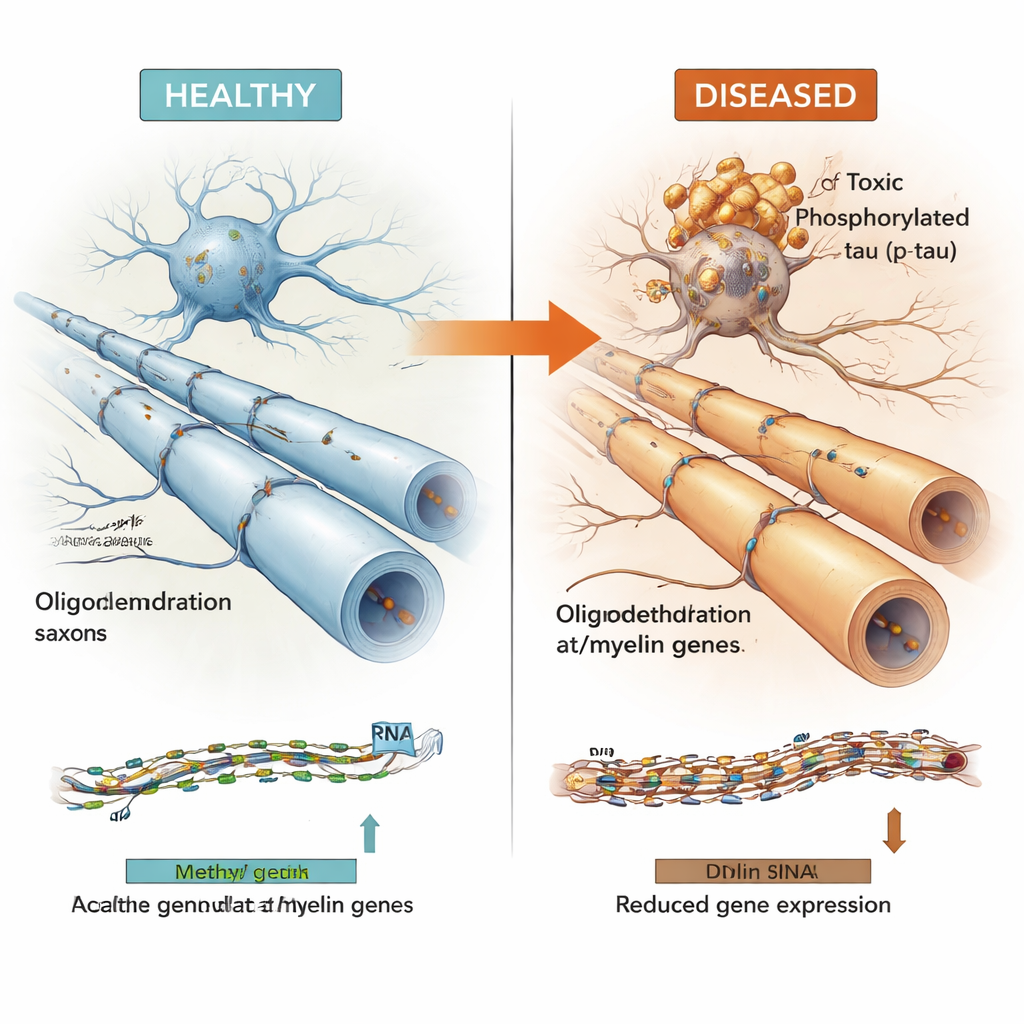
Viele der DNA-Regionen, die mit Tau in Verbindung standen, lagen in „aktiven“ Bereichen des Genoms, die nahegelegene Gene beeinflussen. Durch die Kombination von Methylierungsdaten mit Genaktivitätsmessungen aus denselben Gehirnen zeigte das Team, dass diese Regionen häufig Gene steuern, die von Oligodendrozyten genutzt werden—den Zellen, die Nervenfasern mit isolierendem Myelin umhüllen, damit elektrische Signale schnell und zuverlässig weitergeleitet werden. Wichtige myelinhafte Gene wie MBP, MAG und MYRF sowie das Alzheimer-Risikogen BIN1 und ein neueres Kandidatengen namens LDB3 erschienen in dieser Gruppe. Höhere Werte des toxischen phosphorylierten Tau gingen tendenziell mit mehr Methylierung in diesen Regionen und einer geringeren Expression der zugehörigen Oligodendrozyten- und Myelin-Gene einher, während die weniger schädliche Menge an löslichem Gesamttau das gegenteilige Muster zeigte.
Ein Muster, das bei mehreren Hirnerkrankungen zu sehen ist
Um zu prüfen, ob diese Befunde robust und allgemein gültig sind, untersuchten die Autorinnen und Autoren große, unabhängige Datensätze aus anderen Alzheimer-Gewebesammlungen und aus Gehirnen, die von primären „Tauopathien“ wie progressiver supranukleärer Blickparese und Pick-Krankheit betroffen sind. Obwohl diese Kohorten mit unterschiedlichen Technologien und oft in verschiedenen Hirnregionen gemessen wurden, zeigten viele der gleichen DNA-Regionen und Oligodendrozyten-Gene ein konsistentes Verhalten: Ihre Methylierungsniveaus standen in Beziehung zur Tau-Fibrillenlast, und ihre Expression war in erkrankten Gehirnen sowie in Einzelzellstudien, die sich speziell auf Oligodendrozyten konzentrierten, reduziert. Wichtig ist, dass sich diese Muster nicht einfach durch genetische Unterschiede oder durch einen generellen Zellverlust erklären ließen, was auf eine echte epigenetische Verschiebung in der Funktionsweise der Oligodendrozyten hindeutet.
Was das für das Verständnis von Alzheimer bedeutet
Zusammengefasst stützen die Ergebnisse ein Modell, in dem steigende Mengen schädlichen Taus eng mit epigenetischen Veränderungen in Oligodendrozyten verbunden sind, die myelinbezogene Gene dämpfen—möglicherweise schwächt dies die „Verdrahtung“ des Gehirns und trägt zum kognitiven Abbau bei. Noch ist unklar, was zuerst auftritt—Tau-Akkumulation oder die Störung dieser Myelin-Gene—, doch die starken, wiederholten Assoziationen über tausende Proben und mehrere Erkrankungen deuten auf einen gemeinsamen Mechanismus hin. Durch das Kartieren dieser DNA-Schalter und deren Integration in einen öffentlichen „Multiomic Atlas“ hebt diese Arbeit Oligodendrozyten und ihre epigenetische Regulation als vielversprechende Ziele für künftige Therapien hervor, die darauf abzielen, Hirnschaltkreise zu stabilisieren, anstatt sich allein auf Neuronen oder Amyloid-Plaques zu konzentrieren.
Zitation: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Schlüsselwörter: Alzheimer-Krankheit, Tau-Protein, DNA-Methylierung, Oligodendrozyten, Myelin