Clear Sky Science · de
Strukturelle Grundlage der Signalübertragung und Modulation des menschlichen zinkaktivierten Kanals (ZAC)
Wie ein Spurenelement Nervenzellen beim Sprechen hilft
Zink ist vor allem als Nährstoff in Multivitaminpräparaten bekannt, doch im Körper fungiert dieses Metall auch als schneller chemischer Bote im Gehirn. Die hier beschriebene Studie enthüllt auf atomarer Auflösung, wie ein wenig bekanntes Protein, der zinkaktivierte Kanal (ZAC), Zink außerhalb der Zellen erkennt und dieses Signal in eine elektrische Antwort umwandelt. Das Verständnis dieses speziellen Tores in der Zellmembran könnte klären, wie Zink die Gehirnaktivität formt, und neue Wege aufzeigen, nervöse Signale in Gesundheit und Krankheit gezielter zu steuern.
Ein besonderes Tor für Zink‑Signale
Viele schnelle Nachrichten zwischen Nervenzellen werden von bekannten Botenstoffen wie Serotonin oder Acetylcholin getragen, die ringförmige Kanäle in der Zellmembran öffnen. ZAC ist ein entfernter Verwandter dieser Rezeptoren, reagiert aber statt auf ein organisches Molekül auf Metallionen wie Zink, Kupfer und Protonen. ZAC kommt in vielen menschlichen Geweben vor, auch im Gehirn, fehlt jedoch in üblichen Labortieren wie Mäusen und Ratten, was den Fortschritt verlangsamte. Diese Arbeit nutzt hochauflösende Kryo‑Elektronenmikroskopie, um mehrere dreidimensionale Momentaufnahmen des menschlichen ZAC einzufangen: im Ruhezustand, mit gebundenem Zink und mit zwei verschiedenen Wirkstoffen, die den Kanal abschalten. Zusammengenommen zeigen diese Strukturen, wie Zink an der Spitze des Kanals andockt, wie Ionen hindurchtreten und wie Blocker das Tor zuschnüren oder in einen nicht leitenden Zustand aufspreizen.
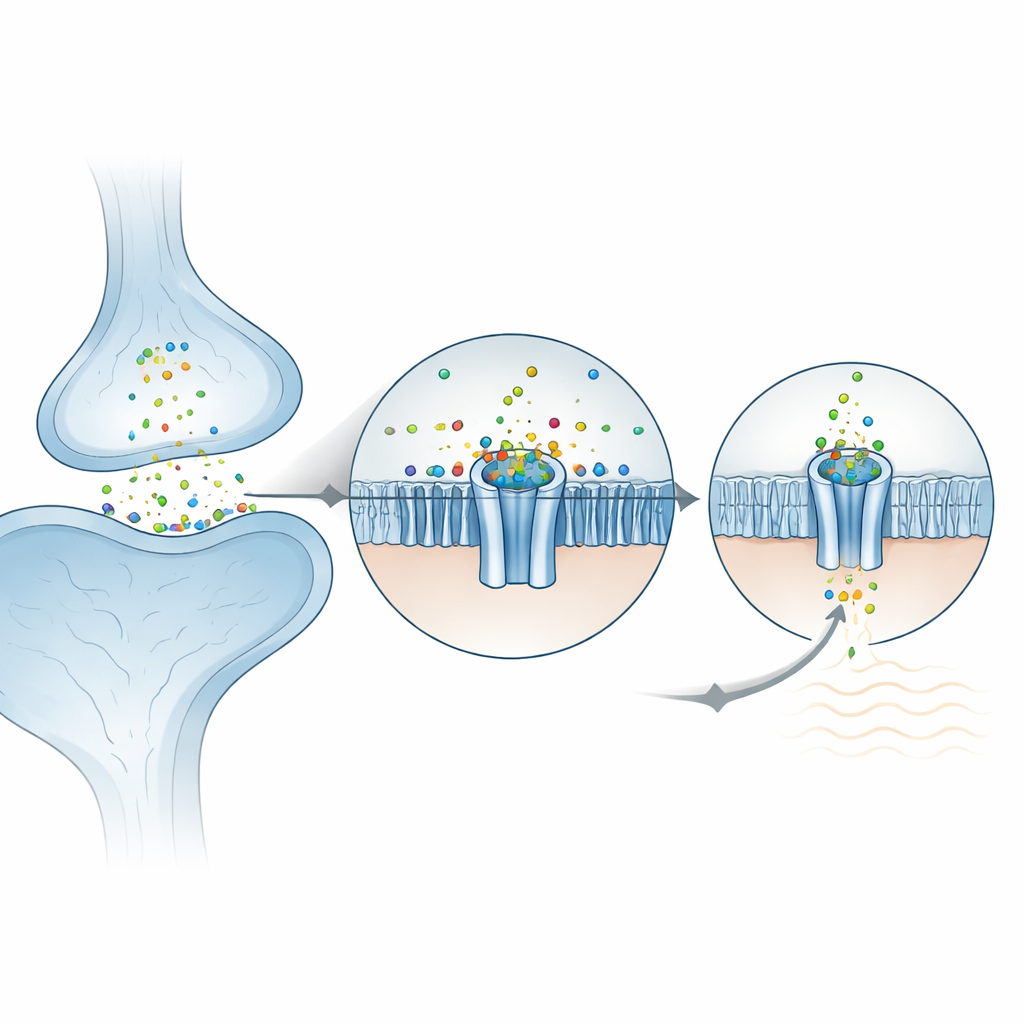
Wie Zink im Kanal einrastet
An der Außenseite der Zelle besteht ZAC aus fünf identischen Untereinheiten, die eine Rosette bilden. Die Forscher fanden, dass Zinkionen in fünf äquivalenten Taschen Platz nehmen, von denen sich jeweils eine zwischen zwei benachbarten Untereinheiten im äußeren Bereich befindet. Überraschenderweise wird Zink nicht von den üblichen „Greifer“-Aminosäuren gehalten, die oft Metalle binden (wie Histidin oder Cystein). Stattdessen wird es hauptsächlich von zwei ringförmigen, aromatischen Seitenketten umschlossen, die das positiv geladene Ion durch sogenannte Kation–π‑Wechselwirkungen stabilisieren. Wenn diese Schlüsselreste in Froscheizellen, die für elektrische Messungen genutzt wurden, mutiert wurden, reagierte der Kanal nicht mehr auf Zink, was ihre zentrale Rolle bestätigt. Die umgebende Struktur ist bereits vororganisiert, was erklärt, warum ZAC auch ohne Zink bemerkenswerte spontane Aktivität zeigt: das Protein liegt nahe am Kipppunkt zwischen geschlossen und offen, und Zink schiebt das Gleichgewicht nur noch in die eine Richtung.
Der Weg für Ionen und eine verbreitete genetische Variante
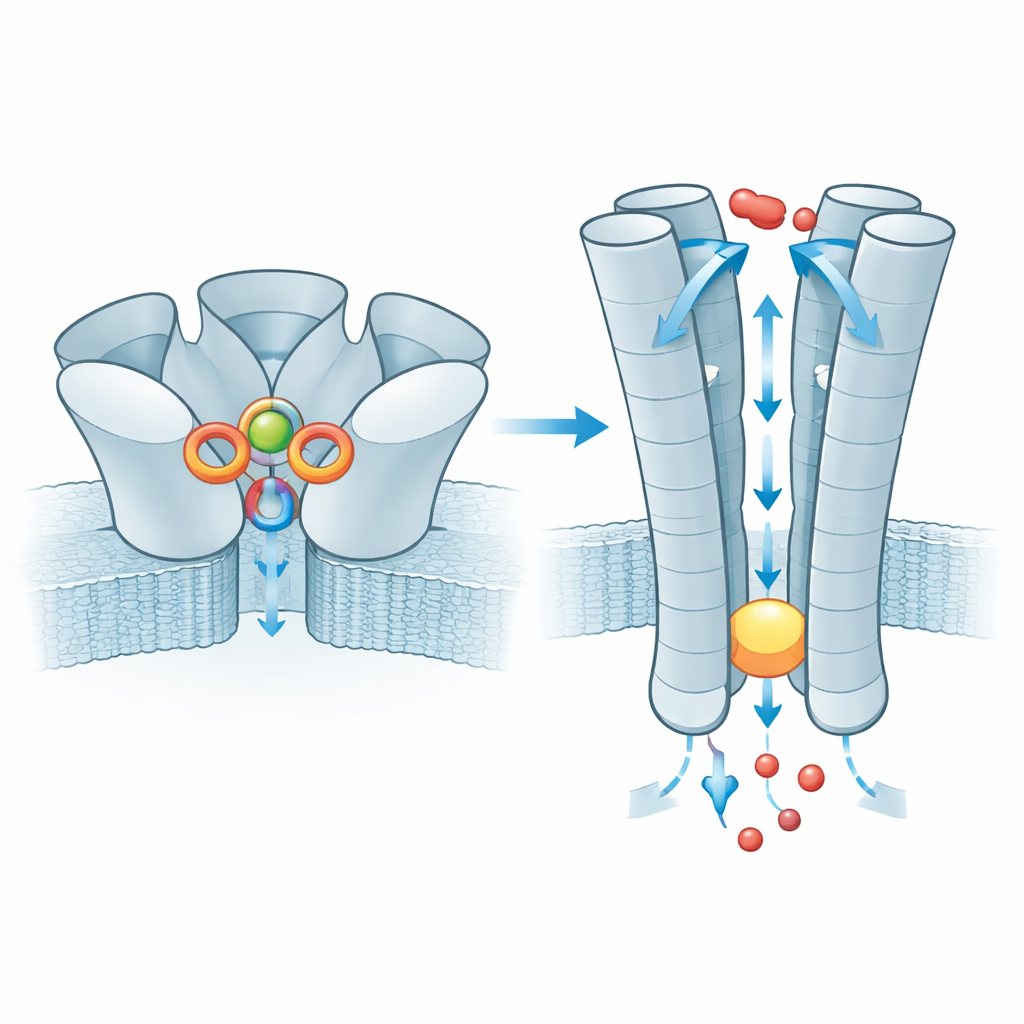
Sobald Zink gebunden ist, wird die Wirkung bis in den membranüberspannenden Teil von ZAC weitergegeben, wo fünf innere Helices den Porus bilden. Im Ruhezustand verengt sich dieses Rohr an einem Ring aus Leucinresten und bildet einen hydrophoben Pfropfen, der den Ionenfluss blockiert. Mit gebundenem Zink weitet sich der Pfropfen gerade genug, damit kleine positive Ionen wie Natrium und Kalium hindurchschlüpfen können, während die geladene Auskleidung des Porus bei der Auswahl dieser Ionen hilft. Das Team untersuchte außerdem eine sehr verbreitete menschliche Variante von ZAC, bei der eine einzelne Aminosäure (Threonin) in einem kurzen Strang oberhalb des Pfropfens gegen Alanin ausgetauscht ist. Diese kleine Änderung schwächt ein Vernetzungsgefüge zwischen benachbarten Untereinheiten, das normalerweise hilft, Zinkbindung an das Tor weiterzuleiten, und elektrische Messungen zeigen, dass Kanäle aus dieser Variante deutlich geringere Ströme leiten. Die Variante wirkt daher als weniger effizienter Signalkonverter, wobei ihre Auswirkungen auf die menschliche Physiologie noch unbekannt sind.
Wie zwei Medikamente den Kanal zum Schweigen bringen
Über Zink hinaus untersucht die Studie auch, wie zwei Antagonisten, TTFB und d‑Tubocurarin (d‑TC), ZAC abschalten. TTFB ist ein maßgeschneidertes kleines Molekül, das sich tief in der Membranregion einnistet und zwischen zwei der porenbildenden Helices knapp über dem Tor hindurchschlüpft. Dort interagiert es mit einer engen hydrophoben Tasche und benachbarten polaren Resten und stützt die Helices so, dass sie sich nicht in einen vollständig offenen, leitfähigen Zustand bewegen können. d‑TC, ein älteres Arzneimittel, das einst als Muskelrelaxans verwendet wurde, wirkt breiter. Ein d‑TC‑Molekül bindet in derselben äußeren Tasche, die normalerweise Zink aufnimmt, imitiert die positive Ladung von Zink, blockiert jedoch das richtige Andocken von echtem Zink. Ein zweites d‑TC‑Molekül sitzt im Eingang des Porus selbst und verstopft physisch den Tunnel. Zusammen fangen diese Bindungen ZAC in einer desensibilisierten, nicht leitenden Konformation ein, während die Form des Proteins relativ offen bleibt.
Was die Ergebnisse für Zink und Gesundheit bedeuten
Diese strukturelle Arbeit zeigt in klaren molekularen Details, dass ZAC ein echter Zinksensor ist, der eine ungewöhnliche aromatische Umfassung nutzt, um das Metall an derselben Art von Stelle zu erkennen, an der andere Familienmitglieder Neurotransmitter binden. Sie identifiziert außerdem spezifische Interaktionsnetzwerke, die einstellen, wie leicht der Kanal öffnet und schließt, und kartiert zwei unterschiedliche Wirkstoffbindungsstellen, die das Tor entweder verkeilen oder den Porus blockieren können. Für Nicht‑Spezialisten ist die zentrale Botschaft, dass Zink nicht nur ein statischer Nährstoff ist, sondern ein aktives Signal, und ZAC einer seiner dedizierten Empfänger. Während Wissenschaftler nach den Rollen von ZAC im menschlichen Körper und bei neurologischen Störungen suchen, die mit Zinkungleichgewicht verbunden sind, liefern diese atomaren Blaupausen eine Landkarte zum Entwurf präziserer Moleküle, um diesen Kanal zu modulieren und potenziell gestörte Zink‑Signalgebung zu korrigieren.
Zitation: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Schlüsselwörter: Zink‑Signalgebung, ligandenaktivierte Ionenkanäle, Neurowissenschaft, Cryo‑EM‑Struktur, Kanalmobilisierung