Clear Sky Science · de
ASCT2-Palmitoylierung, reguliert durch die JNK1-ZDHHC14-Achse, steuert den Glutaminstoffwechsel und das Fortschreiten von NSCLC
Den Brennstoff des Lungenkrebses anheizen
Viele schnell wachsende Lungenkrebsarten sind von Glutamin abhängig, einer verbreiteten Aminosäure, die als wichtiger Brennstoff und Baustein dient. Diese Studie zeigt, wie Tumorzellen ein zentrales Glutamin‑„Ventil“ auf ihrer Oberfläche feinregulieren und wie die Störung dieses Kontrollsystems das Krebswachstum verlangsamen könnte. Das Verständnis dieser verborgenen Kraftstoffklappe erklärt, warum einige Tumoren so schwer zu „verhungern“ sind, und weist auf neue Wirkstoffkombinationen hin, die ihre Energiezufuhr effektiver abschneiden könnten.
Ein zelluläres Tor für Glutamin
Glutamin gelangt hauptsächlich über ein Transportprotein namens ASCT2 in die Zelle, das in der Außenseite der Membran sitzt und Glutamin hineinbefördert. Das nicht‑kleinzellige Lungenkarzinom (NSCLC), die häufigste Form von Lungenkrebs, ist oft stark auf Glutamin angewiesen, um schnelle Zellteilung und Überleben zu unterstützen. Hohe ASCT2‑Spiegel in Tumoren stehen im Zusammenhang mit aggressiver Krankheit und schlechterer Prognose. ASCT2 selbst wird jedoch ständig neu hergestellt, modifiziert und abgebaut, sodass sich die Frage stellt: Was entscheidet, wie viel von diesem Torwächter zu einem bestimmten Zeitpunkt an der Zelloberfläche verbleibt?
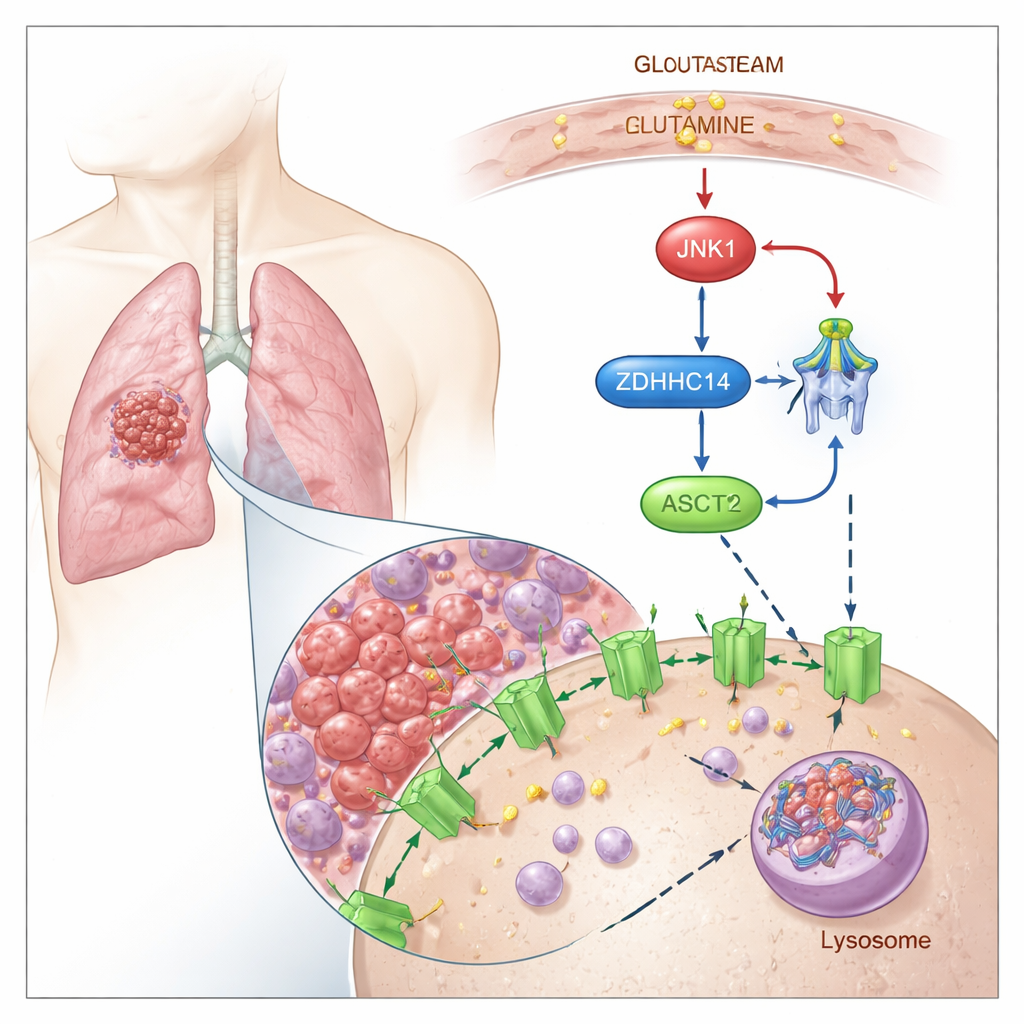
ASCT2 für den Abbau markieren
Die Forschenden zeigen, dass ASCT2 durch einen chemischen „Marker“ namens Palmitoylierung kontrolliert wird, wobei eine Fettsäure an spezifische Cystein‑Reste des Proteins angehängt wird. Sie fanden heraus, dass ein Enzym namens ZDHHC14 diesen Lipid‑Marker an zwei konservierten Stellen von ASCT2 (Cys39 und Cys48) anbringt. Einmal markiert, wird ASCT2 von der Zelloberfläche in zelluläre Recyclingzentren, die Lysosomen, umgeleitet und dort abgebaut. Wird die Palmitoylierung blockiert, bleibt ASCT2 unmarkiert und wird nicht abgebaut, was zu höheren ASCT2‑Proteinspiegeln und erhöhter Glutaminaufnahme führt, ohne die zugrundeliegende Genaktivität zu verändern.
Ein Gegenenzym, das das Tor schützt
Entgegenwirkend zu ZDHHC14 steht ein weiteres Enzym, ABHD17B, das das Fettsäure‑Tag von ASCT2 entfernt. Ist ABHD17B aktiv, ist ASCT2 weniger palmitoyliert, stabiler und wird eher zur Zelloberfläche zurückrecycelt, statt zum Lysosom geschickt zu werden. Dieses Hin‑ und Her von Markierung und Entfernung wirkt wie ein fein einstellbares Rädchen für den Glutaminfluss: ZDHHC14 drängt ASCT2 in Richtung Abbau, während ABHD17B es rettet und den Glutamintransport aufrechterhält. In Lungenkrebszellen führt eine Verschiebung dieses Gleichgewichts zugunsten geringerer Palmitoylierung zu gesteigerter Glutaminaufnahme und unterstützt das Tumorwachstum in Zellkulturen und Mäusen.
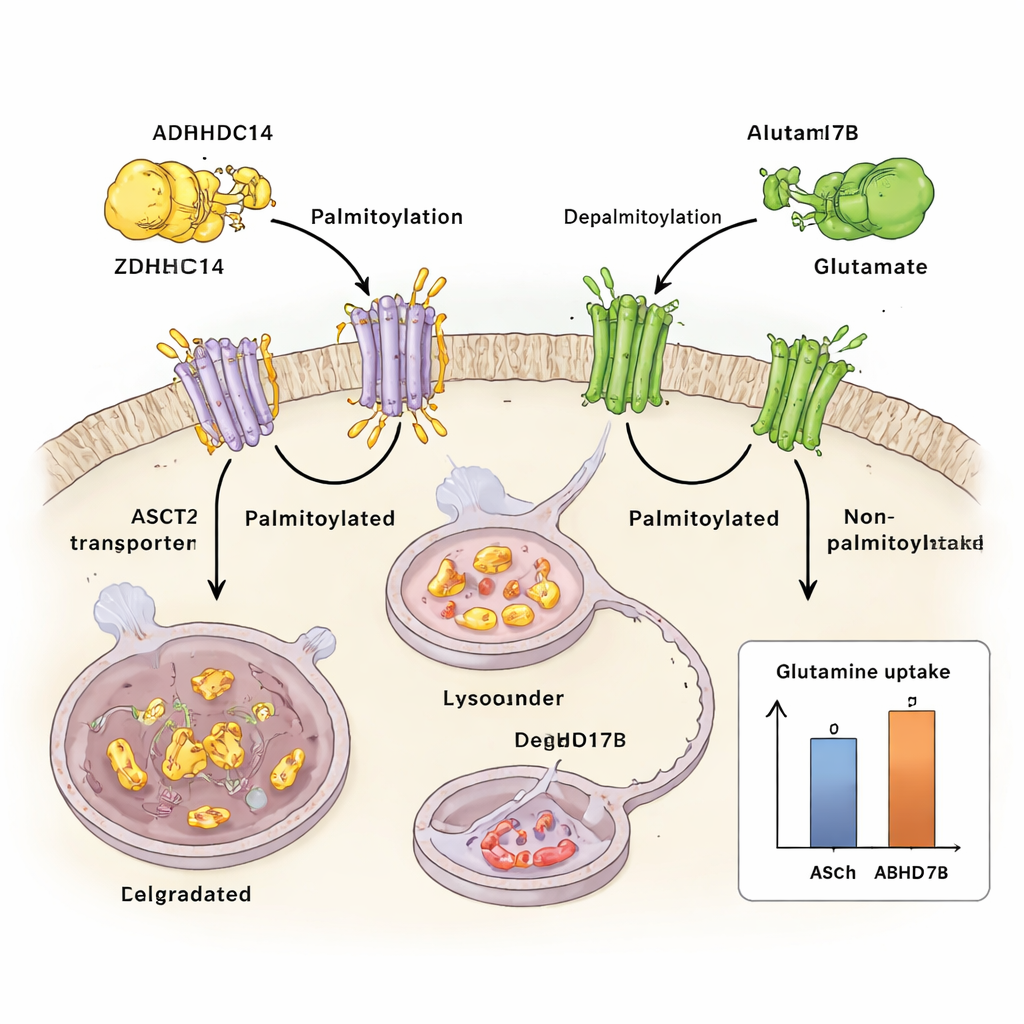
Wie Nährstoffstress das System umschaltet
Das Team untersuchte dann, was passiert, wenn Tumorzellen wenig Glutamin zur Verfügung haben. Unter Glutaminmangel schaltet sich ein stresssensitives Signalmolekül namens JNK1 ein. JNK1 bindet physisch an ZDHHC14 und fügt an einer spezifischen Stelle (Thr440) eine Phosphatgruppe an, wodurch ZDHHC14 zur lysosomalen Degradation markiert wird. Wenn die ZDHHC14‑Spiegel sinken, erhält ASCT2 weniger Palmitoylierungstags, entgeht dem Abbau und sammelt sich an der Zelloberfläche an – genau dann, wenn die Zelle knappes Glutamin am dringendsten aufspüren muss. Die Mutation dieser einzigen JNK1‑empfindlichen Stelle stabilisiert ZDHHC14, stellt die ASCT2‑Markierung wieder her und reduziert die Glutaminaufnahme, was unterstreicht, wie eng Nährstoffstress in diesen Regelkreis eingebunden ist.
Mechanismus in Therapie übersetzen
Da ASCT2 für den Tumorstoffwechsel so wichtig ist, werden Wirkstoffe, die es blockieren, wie die experimentelle Verbindung V9302, als Krebstherapie untersucht. Diese Studie zeigt, dass JNK1‑Signalgebung den ASCT2‑Abbau kontern und damit das Glutamintor effektiv schützen kann. In Zell‑ und Mausmodellen von NSCLC reduzierte die Kombination eines JNK‑Inhibitors mit V9302 die Glutaminaufnahme, das Tumorzellwachstum und die Tumorgröße stärker als eines der beiden Mittel allein. Patientenproben und öffentliche Datensätze zeigen außerdem, dass niedrige ZDHHC14‑ und hohe ASCT2‑Spiegel in NSCLC häufig vorkommen und mit schlechterem Überleben verbunden sind, was darauf hindeutet, dass dieses molekulare Muster helfen könnte, Patienten zu identifizieren, die am ehesten von einer gezielten Therapie dieser Achse profitieren.
Was das für Patientinnen und Patienten bedeutet
Anschaulich zeigt diese Arbeit, dass bestimmte Lungenkrebse ihren bevorzugten Brennstoff steuern, indem sie ein molekulares Ventil an ihrer Oberfläche justieren. Ein Trio aus JNK1, ZDHHC14 und ABHD17B entscheidet, ob das Glutamin‑Tor ASCT2 zur Zerstörung markiert wird oder offenbleibt. Wenn Glutamin knapp wird, verschiebt das System die Balance zugunsten von ASCT2‑Erhalt und hält so die Energiezufuhr aufrecht, wodurch Tumoren unter widrigen Bedingungen überleben können. Durch die gleichzeitige Blockade von ASCT2 und des JNK‑Wegs, der es schützt, konnten Forschende Krebszellen in Labor‑ und Tiermodellen effektiver „verhungern“. Zwar sind weitere Studien nötig, doch diese Phosphorylierungs–Palmitoylierungs‑Achse bietet einen vielversprechenden neuen Ansatz, um die Nährstoffversorgungen von glutaminabhängigen Lungentumoren abzuschneiden.
Zitation: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Schlüsselwörter: Glutaminstoffwechsel, nicht-kleinzelliges Lungenkarzinom, ASCT2-Transporter, Proteinpalmitoylierung, JNK-Signalübertragung