Clear Sky Science · de
Die molekularen Mechanismen und potenziellen therapeutischen Implikationen des Zusammenspiels zwischen DNA-Methylierung und metabolischer Umprogrammierung bei Schilddrüsenkrebs
Warum diese Forschung über das Labor hinaus wichtig ist
Schilddrüsenkrebs zählt zu den weltweit am schnellsten zunehmenden Krebsarten. Während viele Fälle gut behandelbar sind, sprechen die aggressivsten Formen oft nicht mehr auf Radiojod an, eine Standardtherapie, sodass Patienten nur noch wenige sinnvolle Optionen verbleiben. Dieser Übersichtsartikel erklärt, wie zwei unsichtbare Kräfte innerhalb der Zellen – chemische Markierungen auf der DNA und Veränderungen in der Art, wie Tumorzellen Energie nutzen – gemeinsam das Wachstum von Schilddrüsenkrebs und die Resistenz gegen Therapien antreiben. Das Verständnis dieser verborgenen Partnerschaft könnte den Weg für präzisere und nachhaltigere Behandlungen öffnen.
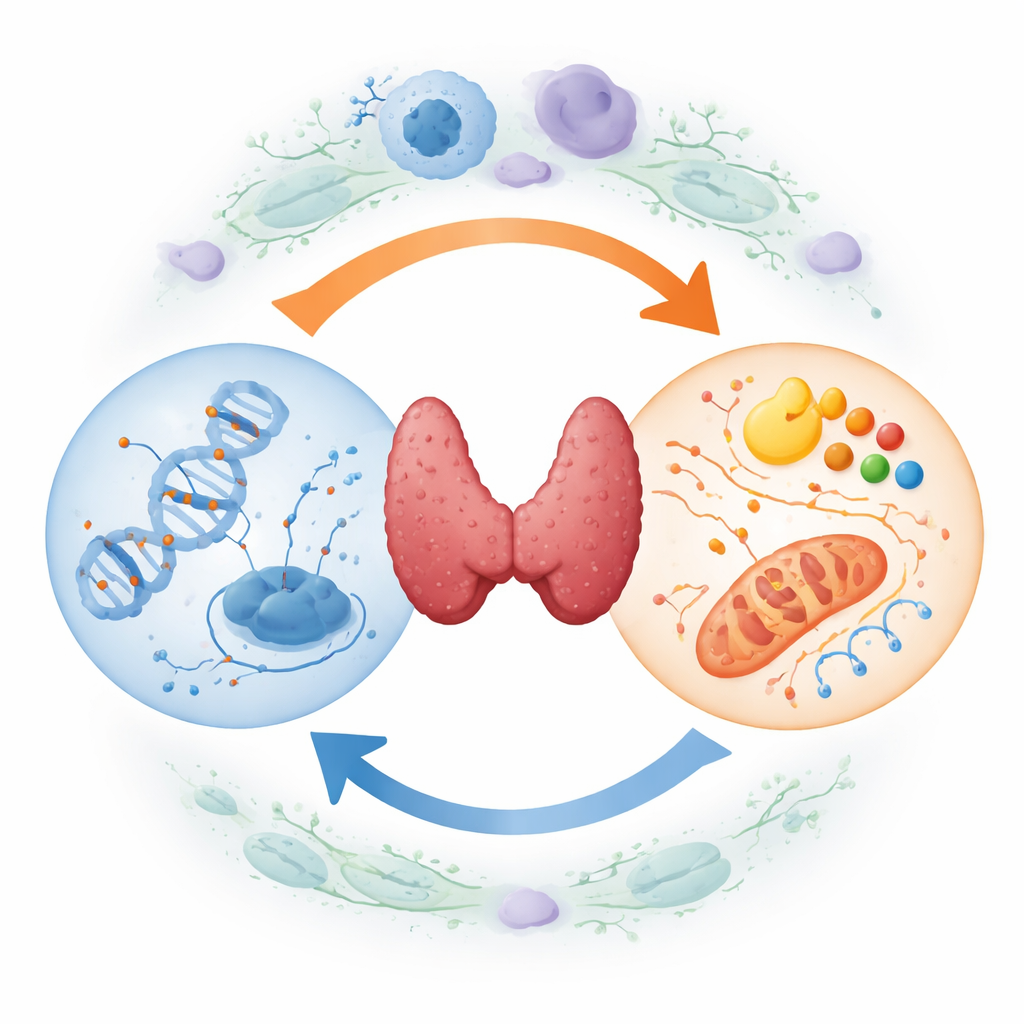
Wie Krebszellen ihr Regelwerk umschreiben
Jede Zelle trägt dieselbe DNA, doch chemische Markierungen, sogenannte Methylgruppen, können Gene ein- oder ausschalten, ohne den genetischen Code zu verändern. Beim Schilddrüsenkrebs ist diese DNA-„Markup“-Landschaft stark verzerrt. Große Bereiche des Genoms verlieren Methylmarken, was Chromosomen destabilisieren kann, während wichtige Bremsen des Wachstums und schilddrüsenspezifische Gene übermäßig markiert und damit stillgelegt werden. Dazu gehören Tumorsuppressorgene und schilddrüsenspezifische Gene, die normalerweise die Jodaufnahme unterstützen. Das Ergebnis ist ein genetisches Instruktionsbuch, in dem viele Kapiteln zur Sicherheit geschwärzt sind, was unkontrolliertes Wachstum und den Verlust normaler Schilddrüsenidentität fördert.
Wie Krebszellen ihre Treibstoffleitungen neu verdrahten
Zeitgleich überarbeiten Schilddrüsentumorzellen, wie sie Energie beschaffen und nutzen. Anstatt hauptsächlich Kraftstoff effizient in den Mitochondrien zu verbrennen, setzen sie stark auf schnellen, aber ineffizienten Zuckerabbau und erzeugen saure Nebenprodukte, die ihnen helfen, dem Immunsystem zu entgehen. Sie erhöhen außerdem die Synthese und den Abbau von Fetten und leiten Aminosäuren wie Serin und Glutamin um, um schnelles Teilen zu unterstützen. Diese Verschiebungen sind nicht zufällig: Sie werden von krebsfördernden Signalen gesteuert und schaffen ein flexibles metabolisches Netzwerk, das Tumorzellen erlaubt, niedrigen Sauerstoffzuständen zu trotzen, Medikamenten zu widerstehen und an neuen Orten zu wachsen.
Wechselverkehr zwischen DNA-Markierungen und Zellstoffwechsel
Eine zentrale Botschaft des Artikels ist, dass DNA-Markierung und Energieverbrauch keine getrennten Geschichten sind — sie bilden eine sich selbst verstärkende Schleife. Einerseits erzeugt der veränderte Stoffwechsel der Tumorzellen bestimmte kleine Moleküle, die als Schalter für die Enzyme wirken, die Methylmarken auf der DNA anbringen oder entfernen. Wenn die Konzentration dieser Moleküle sich ändert, kann das Genom an empfindlichen Stellen zu mehr oder weniger Methylierung gedrängt werden. Andererseits kann DNA-Methylierung direkt Gene stilllegen oder verstärken, die Zuckerstoffwechsel, Fettverarbeitung und Aminosäuretransport steuern. Im Laufe der Zeit verriegelt dieser bidirektionale Verkehr einen krebsfreundlichen Zustand, in dem abnormale DNA-Markierungen und gestörter Stoffwechsel sich ständig gegenseitig stärken.
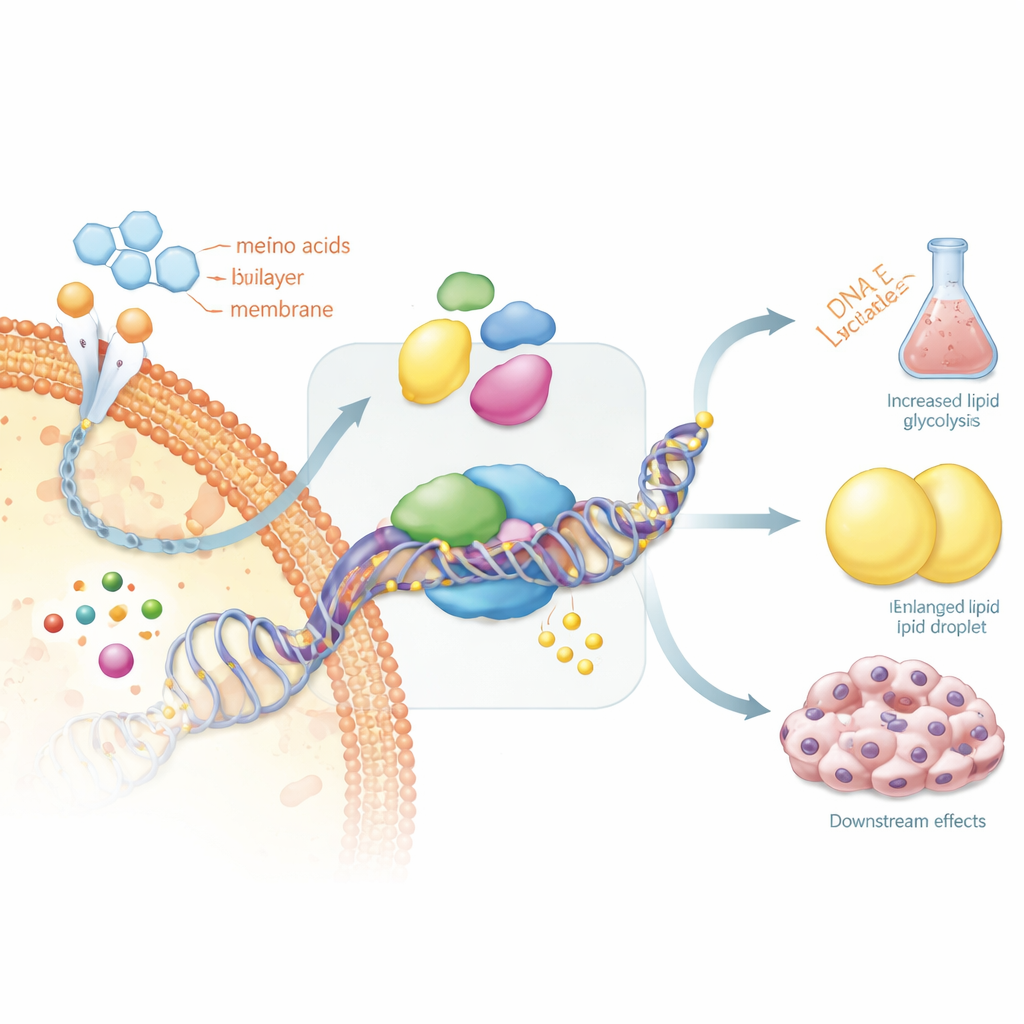
Warum einige Schilddrüsenkrebse aufhören, Jod aufzunehmen
Diese Rückkopplungsschleife hat sehr konkrete Folgen für Patienten. Radiojodtherapie wirkt nur, wenn Tumorzellen die molekulare Maschinerie zur Aufnahme von Jod behalten. Die Übersichtsarbeit zeigt, dass zentrale Schilddrüsengene, die dafür verantwortlich sind—einschließlich des thyreoidea-stimulierenden Hormonrezeptors und des Natrium–Iodid-Transporters—oft durch starke Methylierung ihrer Kontrollregionen abgeschaltet werden. Sobald dies geschieht, „vergessen“ die Krebszellen, dass sie Schilddrüsenzellen sind, und nehmen kein Jod mehr auf, sodass die Standardtherapie versagt. Die Autoren schlagen vor, diese DNA-Markierungen gezielt rückgängig zu machen oder die metabolischen Wege, die sie unterstützen, zu blockieren, um die Jodaufnahme wieder zu erwecken und die Empfindlichkeit gegenüber der Behandlung wiederherzustellen.
Neue Therapieideen auf Grundlage einer integrierten Sichtweise
Die Betrachtung von Schilddrüsenkrebs als Erkrankung einer „DNA-Methylierung–Metabolismus-Achse“ führt zu neuen therapeutischen Strategien. Anstatt sich auf einzelne Wirkstoffe zu verlassen, plädieren die Autoren für Kombinationen, die mehrere Teile der Schleife gleichzeitig angreifen — epigenetische Medikamente, die schädliche DNA-Markierungen lockern, metabolische Wirkstoffe, die zentrale Treibstoffwege blockieren, und Signalblocker, die die wichtigsten krebsfördernden Pfade dämpfen. Die Ergänzung durch moderne Immuntherapien und fortschrittliche Wirkstoffabgabesysteme, etwa intelligente Nanopartikel, könnte das Gleichgewicht weiter zugunsten des Patienten verschieben, indem das Tumor-Immunsystem umgestaltet und Nebenwirkungen reduziert werden. Erste Labor- und klinische Daten deuten darauf hin, dass solche koordinierte Angriffe das Fortschreiten verlangsamen, die Radiojodaufnahme bei einigen Patienten wiederherstellen und Resistenzen hinauszögern können.
Was das für die zukünftige Versorgung bedeutet
Für eine sachverständige Leserschaft lautet die Kernbotschaft, dass aggressive Schilddrüsenkrebse womöglich nicht durch eine einzelne Wunderwaffe heilbar sind, sondern dadurch, dass man den Teufelskreis zwischen DNA-Markierungen und Zellstoffwechsel versteht und unterbricht. Durch detailliertes Kartieren dieser Achse und das Nachverfolgen dieser Veränderungen in Blut- und Tumorproben könnten Ärzte eines Tages Patienten maßgeschneiderten Kombinationen aus epigenetischen, metabolischen, zielgerichteten und Immuntherapien zuordnen. Gelingt dies, könnte dieser integrierte Ansatz die heute hartnäckigsten Schilddrüsenkrebse wieder behandelbar machen — und möglicherweise verhindern, dass sie überhaupt so aggressiv werden.
Zitation: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Schlüsselwörter: Schilddrüsenkrebs, DNA-Methylierung, Krebsstoffwechsel, Radiojod-Resistenz, zielgerichtete Therapie