Clear Sky Science · de
AdipoR1–AMPK-Achse unterdrückt Brustkrebs über molekulare Subtypen hinweg durch multimodale Zelltodwege, einschließlich Ferroptose und Apoptose
Warum Fettzellen für Brustkrebs wichtig sind
Die meisten von uns sehen Körperfett als passiven Energiespeicher, doch Fettzellen sind aktive Fabriken, die Hormone und Signalstoffe ins Blut abgeben. Diese Studie untersucht, wie eines dieser fett‑abgeleiteten Signale über ein Molekül namens AdipoR1 auf Brustkrebszellen das Tumorwachstum verlangsamen kann. Die Arbeit ist bedeutsam, weil sie einen neuen Behandlungsansatz für viele Formen von Brustkrebs nahelegt, indem sie die Kommunikation zwischen Fettgewebe und Tumoren nutzt und dadurch möglicherweise die Wirkung bestehender Medikamente verstärkt.
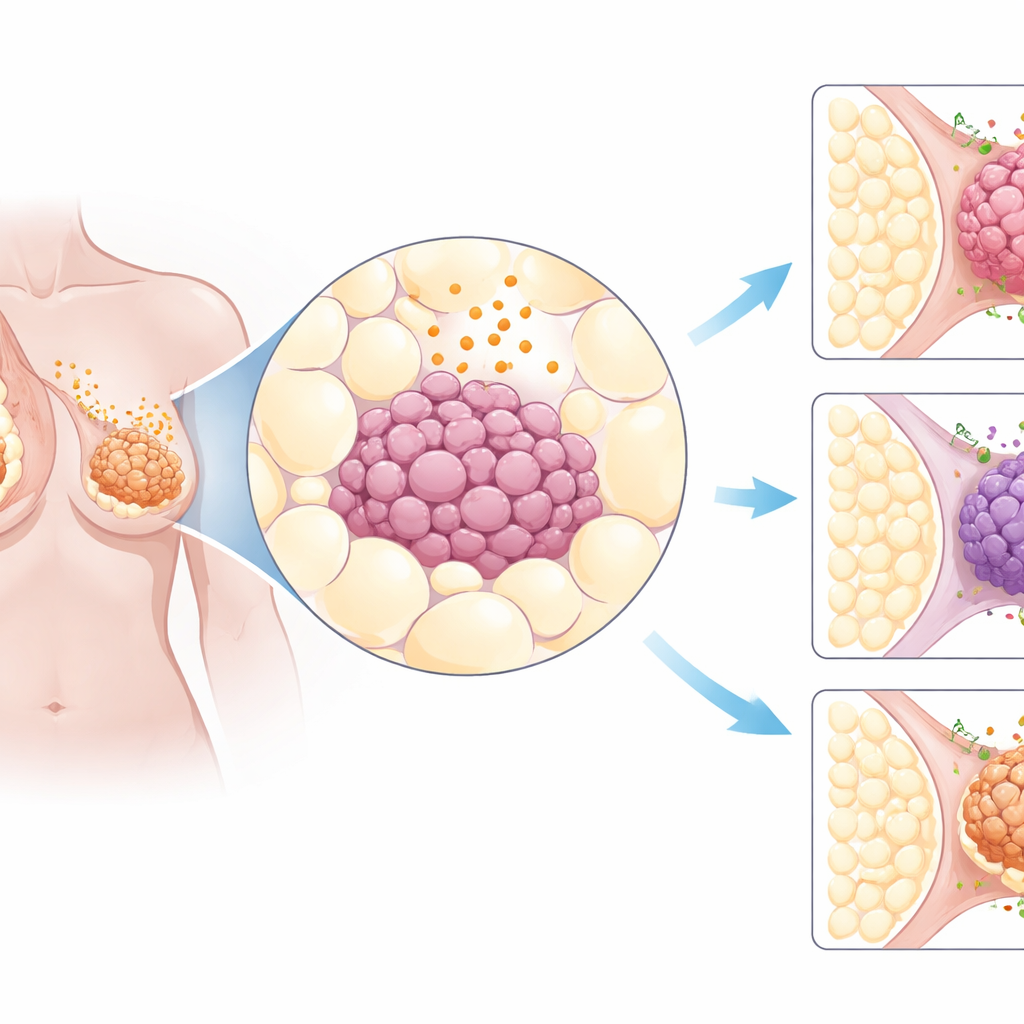
Blick über viele Krebsarten hinweg
Die Forschenden begannen damit, große öffentliche Krebsdatenbanken auszuwerten, die genetische Informationen aus Tausenden von Patiententumoren enthalten. Sie konzentrierten sich auf etwa drei Dutzend Gene, die an Signalen aus dem Fettgewebe und an den zellulären Empfängern dieser Signale beteiligt sind. Beim Vergleich von Tumoren aus 31 verschiedenen Organen mit gesundem Gewebe fiel ein Muster besonders auf: Brustkrebserkrankungen zeigten besonders ausgeprägte Veränderungen in diesen fettbezogenen Signalwegen. Insbesondere war der Rezeptor AdipoR1 häufig in höheren als normalen Mengen in Brusttumoren vorhanden, unabhängig davon, ob diese hormongetrieben, HER2‑positiv oder der aggressiveren triple‑negativen Form angehörten. Gewebeproben von mehr als 600 Brusttumoren bestätigten, dass AdipoR1‑Protein in Tumorzellen weit verbreitet war.
Test eines Fett‑Signal‑Medikaments an Krebszellen
Um zu prüfen, was AdipoR1 tatsächlich in Tumoren bewirkt, nutzte das Team in Zellkultur gezüchtete Brustkrebszelllinien, die mehrere gängige Subtypen repräsentieren. Sie behandelten diese Zellen mit AdipoRon, einem kleinen Molekül, das AdipoR1 aktiviert. AdipoRon löste schnell einen bekannten energieempfindlichen Schalter in Zellen aus, genannt AMPK, was zeigte, dass das Signal weitergeleitet wurde. Mit steigender Dosis von AdipoRon teilten sich die Krebszellen langsamer, bewegten sich in Wundheilungstests weniger und viele unterlagen einem programmierten Selbstzerstörungsprozess. Führten die Forschenden gezielt eine Reduktion von AdipoR1 in den Zellen herbei, verlor AdipoRon einen Großteil seiner Wirksamkeit, während eine Verstärkung von AdipoR1 das Medikament wirksamer machte — ein direkter Zusammenhang mit diesem Rezeptor.
Mehrere Wege, Krebszellen in Richtung Tod zu drängen
Durch die Analyse der Genaktivität nach der Behandlung stellten die Wissenschaftler fest, dass AdipoRon Stressantworten in Brustkrebszellen aktivierte. Es wurden Gene hochreguliert, die mit dem klassischen programmierten Zelltod verbunden sind, ebenso wie solche, die an einer neuer anerkannten, eisenabhängigen Form des Zelltods, der Ferroptose, beteiligt sind. Wichtige Marker dieses Prozesses stiegen sowohl auf RNA‑ als auch auf Proteinebene, insbesondere in hormonempfindlichen Brustkrebszellen, und chemische Messungen geschädigter Zelllipide stützten diese Beobachtung. Gleichzeitig verringerte AdipoRon die Spiegel von Proteinen, die normalerweise Krebszellen beim Überleben helfen, darunter DNA‑Reparaturhelfer (BRCA1 und BRCA2), der Östrogenrezeptor, der das Wachstum vieler Tumoren antreibt, und TROP2, ein Oberflächenmolekül, das mit aggressivem Verhalten verknüpft ist.
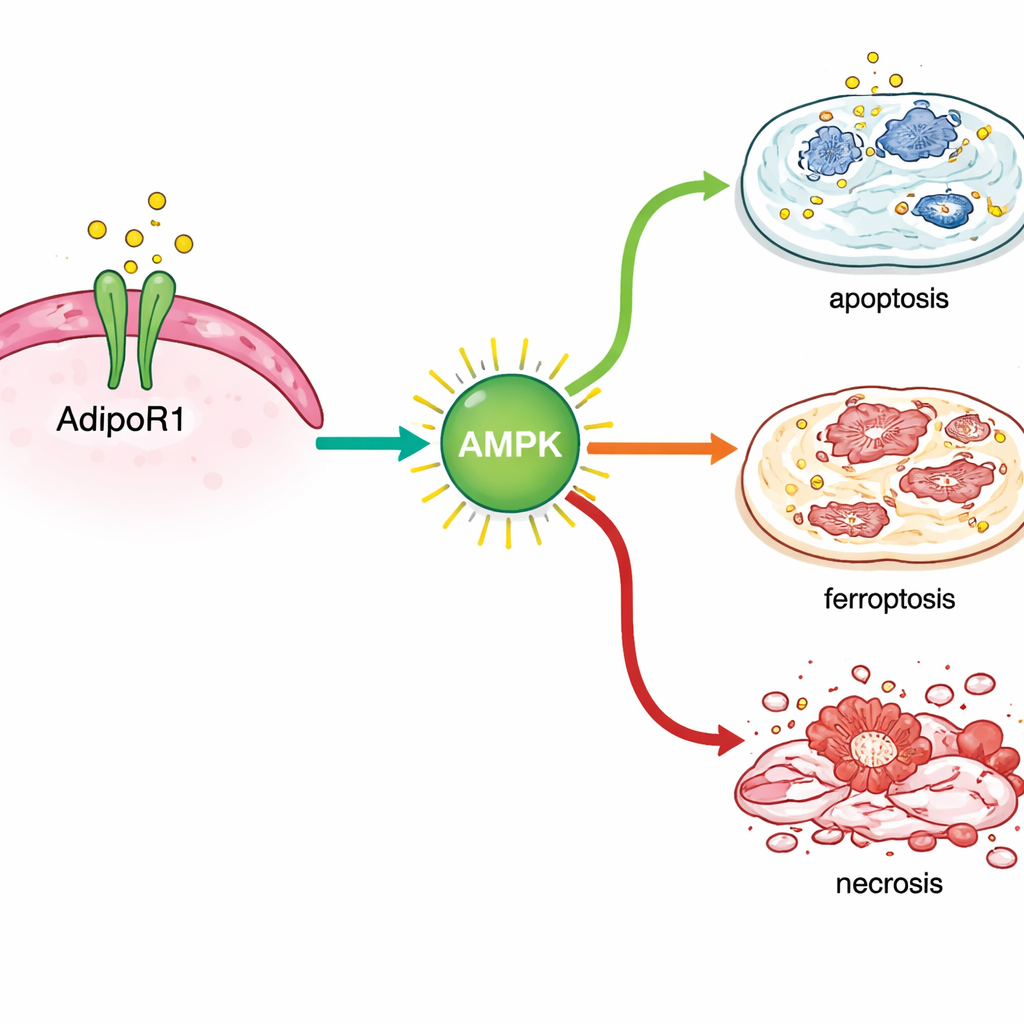
Zusammenwirken mit vorhandenen Therapien
Das Team fragte dann, ob die Aktivierung von AdipoR1 Standardmedikamente ergänzen könnte. Bei hormonempfindlichen Brustkrebszellen führte die Kombination von AdipoRon mit Tamoxifen zu stärkerer Wachstumshemmung als jedes der beiden Medikamente allein. In triple‑negativen Zelllinien verstärkte AdipoRon die Wirkung gängiger Chemotherapeutika wie Paclitaxel und Doxorubicin. In Mäusen mit hormonempfindlichen Brusttumoren verabreichten die Forschenden AdipoRon oral. Tumoren in behandelten Tieren wuchsen langsamer und zeigten unter dem Mikroskop größere Bereiche abgestorbenen Gewebes. Wichtig war, dass die Mäuse während der Behandlung keine offensichtlichen Nebenwirkungen im Verhalten, Gewicht oder der Lebergesundheit zeigten.
Was das für Patientinnen bedeuten könnte
Insgesamt deuten die Befunde darauf hin, dass die Aktivierung von AdipoR1 in Brustkrebszellen mehrere sich überschneidende Wege zum Zelltod aktiviert und gleichzeitig zentrale Überlebensmechanismen schwächt, und dass dieser Ansatz über verschiedene genetische Formen der Erkrankung hinweg wirkt. Anstatt bestehende Therapien zu ersetzen, könnten AdipoR1‑aktivierende Wirkstoffe wie AdipoRon als Zusatz wirken, die Tumoren anfälliger für Hormontherapie, Chemotherapie oder künftige zielgerichtete Mittel machen. Bevor diese Strategie in die Klinik gelangen kann, müssen Forschende jedoch potentere und selektivere AdipoR1‑Aktivatoren entwickeln, klären, bei welchen Patientinnen die Tumoren den Rezeptor besonders stark exprimieren, und die Sicherheit sorgfältig prüfen. Dennoch weist diese Arbeit auf eine interessante Idee hin: Signale aus unserem eigenen Fettgewebe könnten umgelenkt werden, um beim Kampf gegen Brustkrebs zu helfen, statt ihn zu befeuern.
Zitation: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Schlüsselwörter: Brustkrebs, Adipokine, AdipoR1, Zelltodwege, Krebsmetabolismus