Clear Sky Science · de
Rolle von Lipidrafts in der FGFR2c-vermittelten onkogenen Signalgebung durch Einbeziehung des TRPA1-Kanals in Zellen des duktalen Pankreasadenokarzinoms
Warum kleine Inseln in Zellmembranen wichtig sind
Pankreaskrebs gehört zu den tödlichsten Krebsarten, zum Teil weil seine Zellen ungewöhnlich gut darin sind, vom ursprünglichen Tumor abzulösen und in benachbartes Gewebe einzudringen. Diese Studie untersucht winzige „Inseln“ in der äußeren Hülle von Krebszellen, die aus Cholesterin und Lipiden bestehen, und stellt eine einfache Frage mit großer Tragweite: Helfen diese Inseln dabei, ein Wachstumssignal einzuschalten, das den Pankreaskrebs aggressiver macht, und kann das Stören dieser Inseln den Prozess verlangsamen?
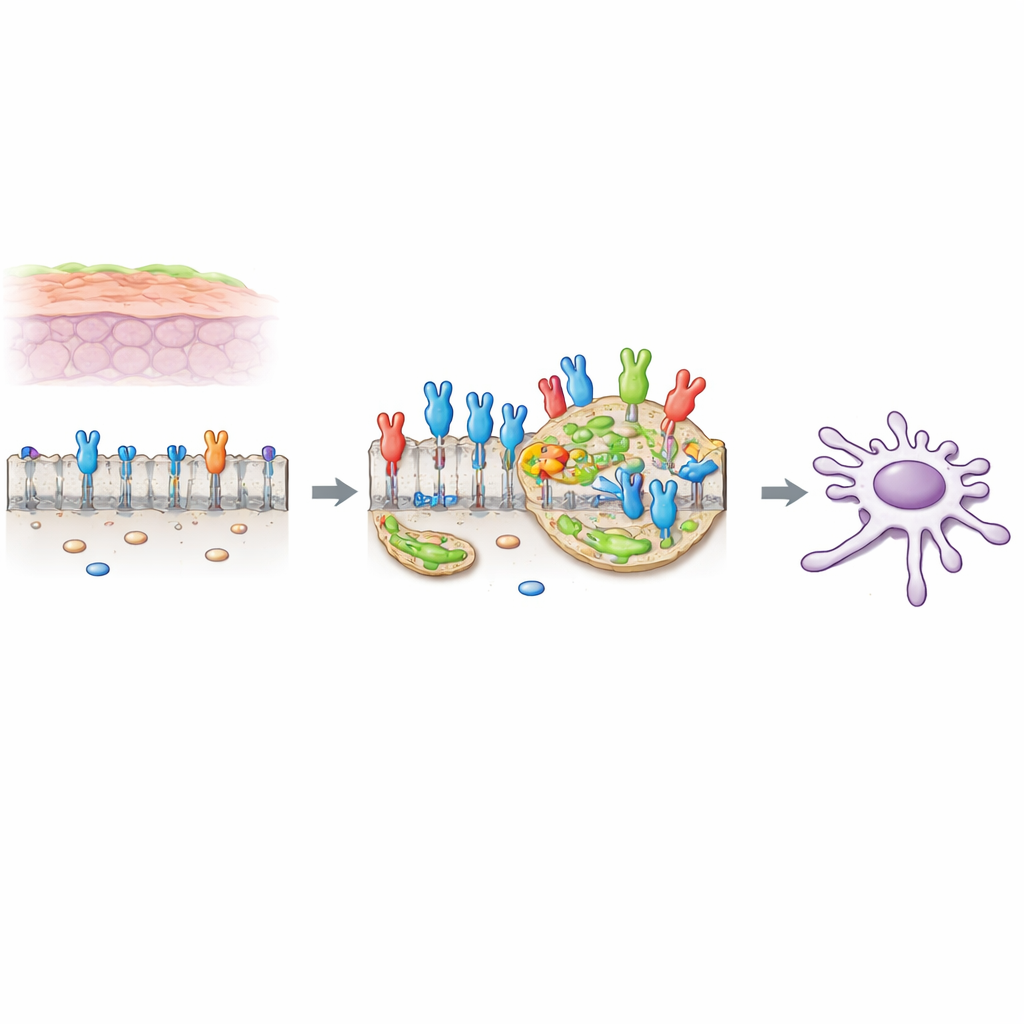
Ein krebsfördernder Schalter an der Zelloberfläche
Viele Zellen haben an ihrer Oberfläche Schalter, die auf Wachstumssignale reagieren. Einer dieser Schalter, FGFR2c genannt, ist eine Variante, die normalerweise in beweglicheren Zellen vorkommt, aber in duktalen Pankreasadenokarzinom-(PDAC-)Zellen ungewöhnlich stark vertreten ist. Wenn dieser Schalter durch sein äußeres Ligandenmolekül aktiviert wird, treibt er Veränderungen an, die als epithelial–mesenchymale Transition (EMT) bekannt sind und die Zellen weniger haftend und beweglicher machen. Frühere Arbeiten der Autor:innen zeigten, dass FGFR2c in PDAC-Zellen eine Kaskade intrazellulärer Botenstoffe aktiviert, an der das Protein PKCε und mehrere klassische Wachstumswege beteiligt sind, was Überleben, Bewegung und Invasion der Zellen fördert.
Cholesterinreiche Inseln als Signalverstärker
Die äußere Zellmembran ist nicht einheitlich. Sie enthält kleine, cholesterinreiche Bereiche, so genannte Lipidrafts, die als Miniaturplattformen fungieren, auf denen Signalmoleküle sich sammeln und effizienter kommunizieren können. Die Forscher fanden heraus, dass bei Aktivierung von FGFR2c durch seinen äußeren Stimulus mehr Rezeptor in diese Lipidrafts wandert. Mit fluoreszierenden Markern und biochemischer Fraktionierung zeigten sie, dass aktiviertes FGFR2c in diesen Bereichen konzentriert ist, während seine Verteilung außerhalb der Rafts sich von glatt zu punktiert verändert — was mit einer Rezeptorklusterbildung auf diesen Inseln übereinstimmt.
Das Aufbrechen der Inseln schwächt krebsfördernde Eigenschaften
Um zu prüfen, ob diese Lipidinseln für die krebsfördernden Effekte von FGFR2c essenziell sind, verwendete das Team eine Verbindung (Methyl-β-Cyclodextrin), die selektiv Cholesterin aus der Membran entfernt und Lipidrafts destabilisiert, ohne die Zellen abzutöten. In FGFR2c-reichen PDAC-Zellen reduzierte das Auflösen der Rafts deutlich die Aktivierung wichtiger nachgeschalteter Signalmoleküle und bremste das EMT-Programm: Gene und Proteine, die mit einem mobilen, invasiven Zustand assoziiert sind, nahmen ab, während epitheliale Merkmale teilweise wiederhergestellt wurden. Dieselbe Behandlung senkte auch die Spiegel invasionsassoziierter Proteine wie MCL-1, SRC und matrixabbauender Enzyme und verringerte die Fähigkeit der Krebszellen, sich zu bewegen und ein Gel zu durchdringen, das das umgebende Gewebe nachahmt. Zellen mit sehr wenig FGFR2c zeigten fast keine Reaktion, was die zentrale Bedeutung der Rezeptor–Raft-Partnerschaft in diesen Tumoren unterstreicht.
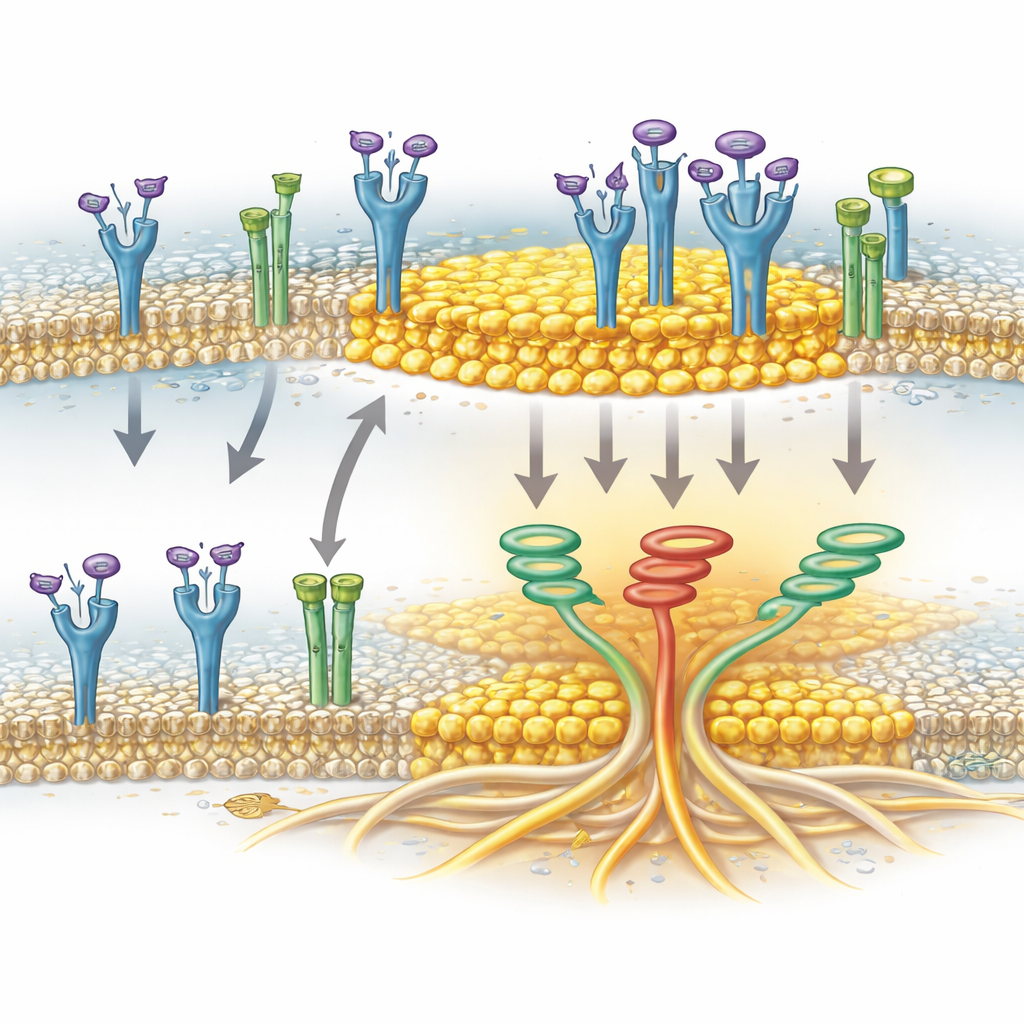
Ein Ionenkanal als Helfer bei der Clusterbildung
Die Studie identifiziert außerdem einen überraschenden Helfer: TRPA1, ein Kanalprotein, das vor allem dafür bekannt ist, Reizstoffe und oxidativen Stress in Nerven wahrzunehmen. In Pankreaskrebszellen ist TRPA1 an der Membran vorhanden und kann sich in Lipidrafts aufhalten. Die Autor:innen zeigten, dass TRPA1 physisch mit FGFR2c assoziiert, wenn der Rezeptor aktiviert ist, und dass diese Assoziation mit der Anreicherung von FGFR2c in den Raft-Fraktionen zusammenfällt. Wenn die TRPA1-Spiegel reduziert wurden, reicherte sich aktiviertes FGFR2c nicht mehr effizient in den Raft-Bereichen an, obwohl die Rafts selbst intakt blieben. Dies deutet darauf hin, dass TRPA1 nicht nur ein passiver Passagier ist, sondern aktiv hilft, FGFR2c in diesen cholesterinreichen Plattformen zu begleiten oder zu stabilisieren, wo der Rezeptor das invasive Signalisierungsnetzwerk effektiver auslösen kann.
Was das für künftige Therapien bedeutet
In der Gesamtsicht zeichnen die Ergebnisse das Bild eines kooperativen Verbandes aus FGFR2c, TRPA1 und Lipidrafts, der das invasive Verhalten von Pankreaskrebszellen stärkt. FGFR2c liefert das Wachstumssignal, Lipidrafts die physische Bühne, auf der Signalkomplexe sich zusammenfinden, und TRPA1 hilft, den Rezeptor auf diese Bühne zu bringen. Für Laien lautet die Kernbotschaft: Nicht nur die krebsfördernden Moleküle selbst, sondern auch die winzigen Membranslandschaften, die sie einnehmen, können bestimmen, wie gefährlich ein Tumor wird. Durch gezieltes Ansprechen von FGFR2c, TRPA1 oder der Stabilität dieser cholesterinreichen Inseln — allein oder in Kombination — könnten zukünftige Therapien in der Lage sein, die invasive Maschinerie von Pankreaskrebszellen präziser und tumorspezifischer zu schwächen.
Zitation: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Schlüsselwörter: Pankreaskrebs, Lipidrafts, FGFR2c, TRPA1-Kanal, Zellinvasion