Clear Sky Science · de
PRDM1 begrenzt das Fortschreiten von Blasenkrebs und erhöht die Chemosensitivität durch Unterdrückung der OTUD6A-vermittelten Deubiquitinierung von CDC6
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Blasenkrebs ist verbreitet und wird häufig mit Chemotherapeutika wie Gemcitabin und Cisplatin behandelt. Viele Tumoren sprechen jedoch nur schlecht an oder entwickeln schnell Resistenzen, sodass Betroffene wenige Optionen bleiben. Diese Studie beschreibt eine eingebaute Schutzbremse in Blasenzellen — ein Protein namens PRDM1 — das das Tumorwachstum bremst und die Wirksamkeit der Chemotherapie verbessert. Zu verstehen, wie diese Bremse funktioniert und wie Tumoren sie ausschalten, könnte neue Wege eröffnen, das Ansprechen auf Therapien vorherzusagen und gezieltere Behandlungen zu entwickeln.
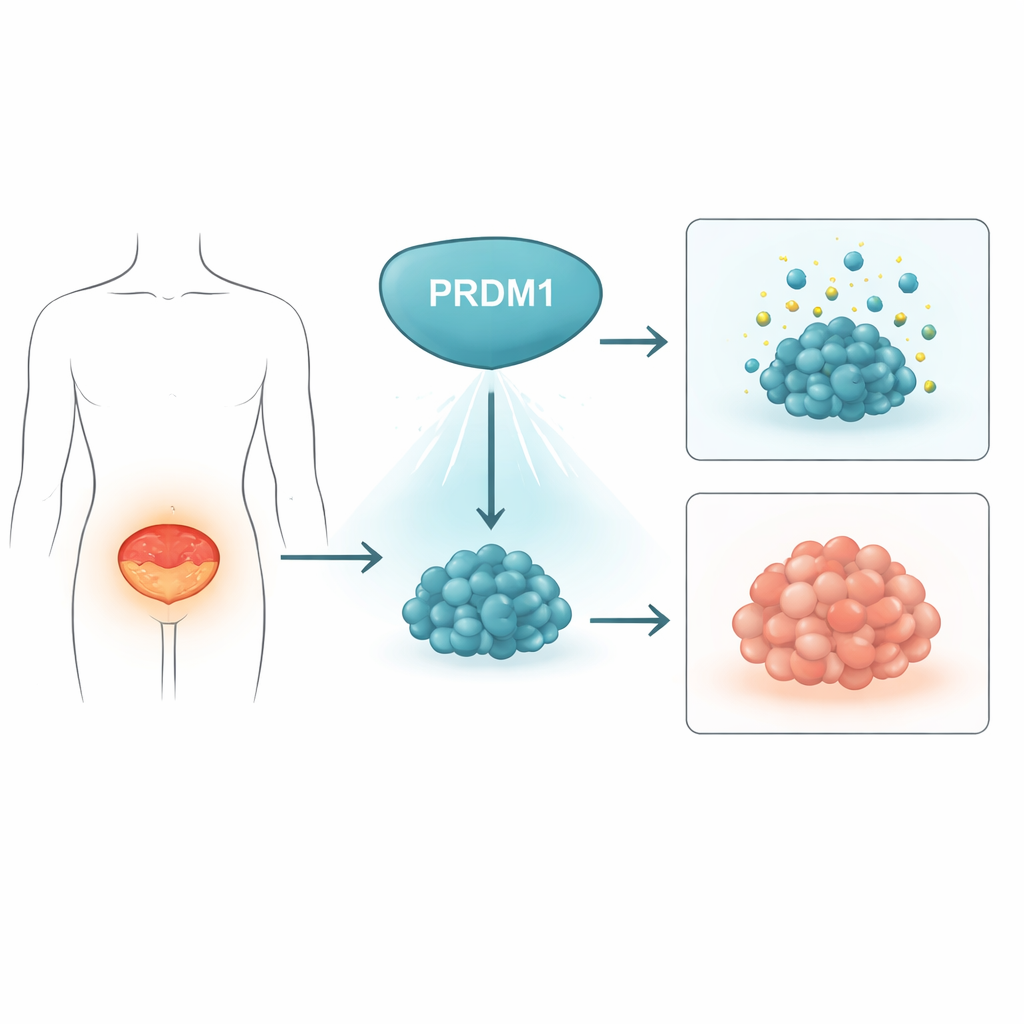
Eine natürliche Bremse gegen Blasentumoren
Die Forschenden fragten zunächst, ob PRDM1, ein Gen, das dafür bekannt ist, die Entwicklung von Immunzellen zu steuern, auch den Blasenkrebs beeinflussen könnte. Anhand von 48 Paaren aus menschlichen Blasentumoren und dem angrenzenden Normalgewebe fanden sie heraus, dass PRDM1-Proteinspiegel in Tumoren durchgehend niedriger waren als in gesunder Blasenschleimhaut. Große öffentliche Krebsdatensätze zeigten dasselbe Muster auf RNA-Ebene. In einem Mausmodell, in dem Blasenkrebs durch einen Chemikalienstoff im Trinkwasser über die Zeit ausgelöst wird, sanken die PRDM1-Level schrittweise, während normales Gewebe krebsartig wurde. Zusammen deuten diese Daten darauf hin, dass PRDM1 normalerweise als Bremse der Tumorentstehung wirkt und während der Entwicklung von Blasenkrebs abgeschaltet wird.
Verlangsamung von Tumorzellwachstum und Zellteilung
Um zu untersuchen, was PRDM1 in Blasenkrebszellen tatsächlich bewirkt, nutzte das Team genetische Werkzeuge, um das Gen herunter- oder hochzuregulieren. Wurde PRDM1 in Blasenkrebszelllinien reduziert, teilten sich die Zellen schneller, bildeten mehr Kolonien und erzeugten größere Tumoren in Mäusen. Ein vollständiges Entfernen von PRDM1 mittels CRISPR-Geneditierung zeigte ähnliche Effekte. Im Gegensatz dazu verlangsamte das erzwungene Überexprimieren von PRDM1 das Wachstum in Kultur und führte in Tiermodellen zu deutlich kleineren Tumoren sowie zu niedrigeren Werten des Zellteilungsmarkers Ki-67. Detaillierte Analysen des Zellzyklus zeigten, dass zusätzliches PRDM1 eine Verzögerung beim Übergang aus der Mitose in die nächste Wachstumsphase bewirkte, was darauf hindeutet, dass das Protein die Zellteilung kontrolliert.
Chemotherapie wirksamer machen
Da der Erfolg einer Chemotherapie stark davon abhängt, wie gut Medikamente die Tumor-DNA schädigen und Zelltod auslösen, untersuchten die Autoren, ob PRDM1 die Empfindlichkeit gegenüber Medikamenten beeinflusst. Zellen ohne PRDM1 ließen sich mit Gemcitabin oder Cisplatin schwerer abtöten und benötigten höhere Dosen, um denselben Effekt zu erzielen, während Zellen mit zusätzlichem PRDM1 empfindlicher wurden. PRDM1-defiziente Zellen zeigten nach Behandlung weniger DNA-Schäden und weniger sterbende Zellen, während PRDM1-überexprimierende Zellen mehr DNA-Brüche und höhere Werte apoptotischer Marker aufwiesen. Die Studie analysierte auch einen wichtigen DNA-Schadens-Signalweg, bekannt als ATR–Chk1-Pathway, der Zellen hilft, Chemotherapie zu überleben. Der Verlust von PRDM1 verstärkte dieses Überlebenssignal, während eine Erhöhung von PRDM1 es abschwächte. In Maus-Tumormodellen sprachen Tumoren mit hohem PRDM1 besser auf Gemcitabin an, und die Wiederherstellung von PRDM1 in medikamentenresistenten Zellen kehrte die Resistenz teilweise um.
Aufdeckung einer dreistufigen Kontrollkaskade
Bei tiefergehenden Untersuchungen identifizierten die Forschenden eine molekulare Kette, die PRDM1 mit Zellwachstum und Arzneimittelantwort verbindet. In früheren Arbeiten hatten sie gezeigt, dass ein Enzym namens OTUD6A ein anderes Protein, CDC6, stabilisiert — dieses spielt eine Rolle beim Start der DNA-Replikation und bei der Aktivierung von DNA-Schadenssignalen. Hier entdeckten sie, dass PRDM1 die CDC6-Nachricht nicht auf genetischer Ebene verändert, sondern stattdessen dessen Abbau durch die zellulären Proteinabbausysteme fördert. PRDM1 reduziert die OTUD6A-Level, was zu mehr chemischen Markierungen an CDC6 führt, die seinen Abbau kennzeichnen. Werden OTUD6A oder CDC6 experimentell gesenkt, wirkten sie dem Wachstums- und Resistenzvorteil durch niedrige PRDM1-Spiegel entgegen. Umgekehrt konnten erhöhte OTUD6A- oder CDC6-Level die Vorteile von hohem PRDM1 aufheben. Analysen von Patientenproben bestätigten diese Beziehung: Tumoren zeigten allgemein niedrige PRDM1-, aber hohe OTUD6A- und CDC6-Werte, und die Spiegel dieser Proteine korrelierten eng miteinander.
Was dies für zukünftige Behandlungen bedeuten könnte
Zusammengefasst skizziert die Studie einen klaren Weg, bei dem PRDM1 Blasenkrebs bremst und die Chemotherapieeffektivität erhöht, indem es OTUD6A herunterreguliert, was wiederum den Abbau von CDC6 ermöglicht. Ohne diese Bremse sammelt sich CDC6 an, die Zellteilung beschleunigt sich und Tumorzellen werden besser darin, DNA-schädigende Medikamente zu überleben. Für Patientinnen und Patienten deuten diese Befunde darauf hin, dass die Messung von PRDM1-, OTUD6A- und CDC6-Spiegeln in Tumoren helfen könnte, vorherzusagen, wie gut eine Chemotherapie wirkt. Mittelfristig könnten Wirkstoffe, die PRDM1-Aktivität wiederherstellen oder OTUD6A bzw. CDC6 blockieren, entwickelt werden, um resistente Blasenkrebsformen wieder empfindlich zu machen und die Behandlungsergebnisse zu verbessern.
Zitation: Cui, J., Chen, S., Liu, X. et al. PRDM1 restricts bladder cancer progression and enhances chemosensitivity by suppressing OTUD6A-mediated deubiquitination of CDC6. Cell Death Dis 17, 247 (2026). https://doi.org/10.1038/s41419-026-08498-3
Schlüsselwörter: Blasenkrebs, Chemoresistenz, PRDM1, CDC6, OTUD6A