Clear Sky Science · de
Die p53-Krebsmutanten Y220C, Y220N und Y220S mit dem kleinen Stabilisierungsmittel rezatapopt anvisieren
Warum das für künftige Krebstherapien wichtig ist
Krebs entwaffnet häufig p53, ein Protein, das man manchmal den „Wächter“ der Zelle nennt, indem er so mutiert wird, dass es gefährliche Zellen nicht mehr in Schach halten kann. Eine besonders häufige Veränderung in p53, bekannt als Y220C, tritt in soliden Tumoren auf und dient als Testfall für Wirkstoffe, die beschädigtes p53 reparieren sollen, statt Zellen einfach abzutöten. Diese Studie stellt eine praktische, patientenorientierte Frage: Kann ein vielversprechendes experimentelles Medikament, rezatapopt, das bereits in klinischen Studien für Y220C geprüft wird, auch Menschen helfen, deren Tumoren eng verwandte, aber seltener auftretende Mutationen an derselben Position in p53 tragen?
Ein Wirkstoff, der einen Riss in p53 zunäht
Viele p53-Mutationen lassen das Protein aufklappen und seine präzise Form verlieren. Bei der Y220C-Mutation entsteht durch die Veränderung eine kleine Vertiefung auf der Proteinoberfläche — ein Defekt, von dem Chemiker erkannten, dass er mit maßgeschneiderten kleinen Molekülen „verstopft“ werden kann, um p53 zu stabilisieren. Rezatapopt ist ein solches Molekül, entstanden aus früheren chemischen Reihen, die in diese Höhlung eindringen und wie eine molekulare Schiene wirken. Die Autoren konzentrieren sich auf zwei weitere Mutationen an derselben Aminosäureposition, Y220S und Y220N, die ebenfalls eine ähnliche Tasche schaffen, p53 aber noch stärker destabilisieren als Y220C. Wenn rezatapopt diese Varianten ebenfalls verschließen könnte, würde dies diesen Ansatz der Präzisionsmedizin auf jährlich tausende zusätzliche Patientinnen und Patienten ausdehnen. 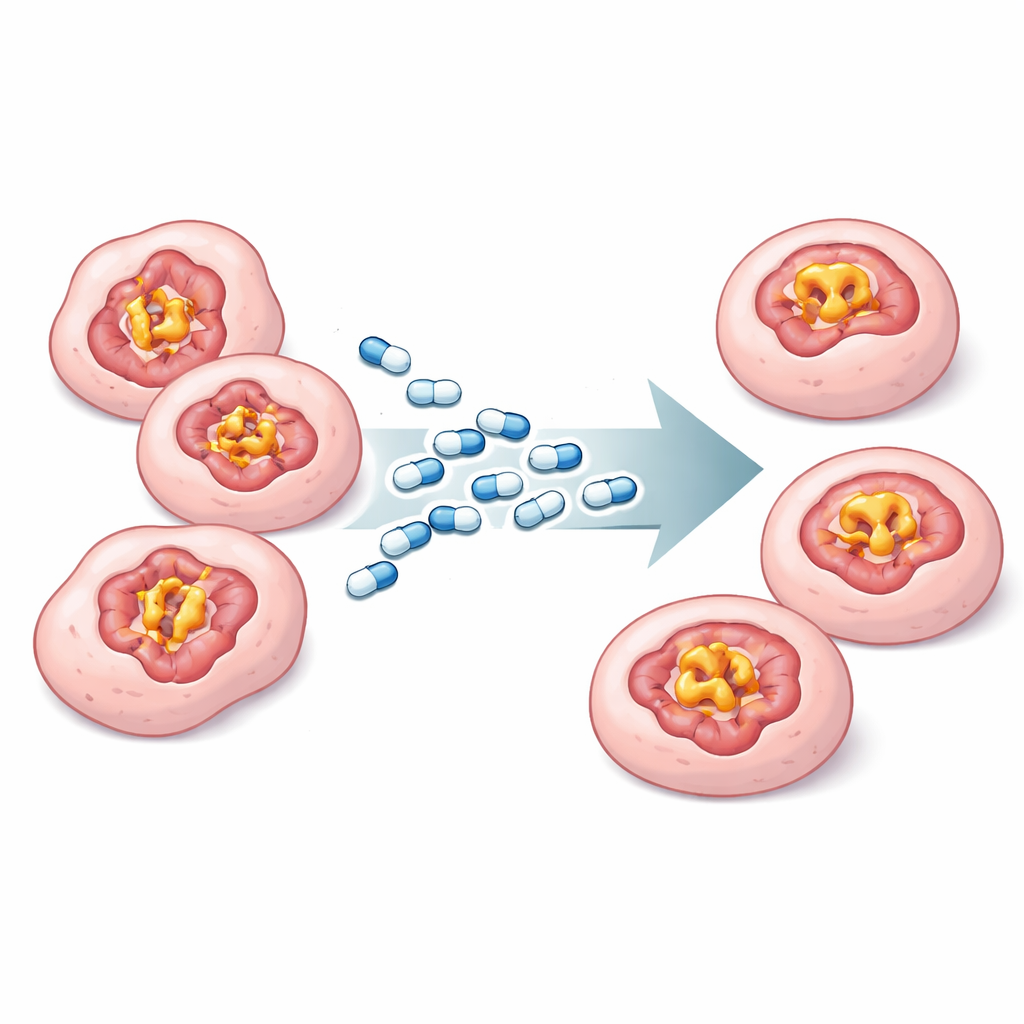
Messen, wie gut rezatapopt mutantem p53 Griff und Halt verleiht
Um das zu prüfen, reinigte das Team den DNA-bindenden Kern von p53 mit den Veränderungen Y220C, Y220S oder Y220N und setzte jede Variante rezatapopt (und nah verwandten Chemikalien) aus. Mit hitzebasierten Tests zeigten sie, dass alle drei mutierten Proteine stabiler wurden, wenn das Medikament band, wobei Y220C und Y220S praktisch wieder die Stabilität des Wildtyps erreichten. Im Gegensatz dazu erholte sich Y220N nur teilweise. Eine zweite Methode, die die bei der Bindung freigesetzte Wärme misst, erklärte das Warum: rezatapopt bindet sehr stark an Y220C (im Bereich weniger zehn Nanomolar), etwas schwächer an Y220S und noch schwächer an Y220N, wobei alle Bindungsstärken in Bereichen liegen, die für die medizinische Chemie vielversprechend sind.
Die molekulare Reparatur im atomaren Detail sehen
Hochaufgelöste Röntgenkristallstrukturen lieferten eine visuelle Erklärung. In allen drei Mutanten schmiegt sich rezatapopt in die durch die Mutation entstandene Spalte in einer konservierten Stellung: Sein zentrales Gerüst füllt die Höhlung, ein Ende reicht tief in die Tasche mit einem Cluster von Fluoratomen, und das andere Ende interagiert mit einer nahegelegenen Proteinschleife. Das Medikament bildet ein Netzwerk von Kontakten, einschließlich eines strategisch platzierten Fluoratoms, das mit dem Proteingerüst wechselwirkt. Bei Y220S bleiben diese Wechselwirkungen mit nur geringfügigen Verschiebungen erhalten, was eine starke Stabilisierung erlaubt. Bei Y220N jedoch zwingt die Bindung des Medikaments die Seitenkette Asparagin in den öligen Kern des Proteins auf eine energetisch ungünstige Weise, und einige Kontakte zum fluorierten „Anker“ des Wirkstoffs gehen verloren. Diese angespannte Passform erklärt sowohl die schwächere Bindung als auch die unvollständige Wiederherstellung der Stabilität. 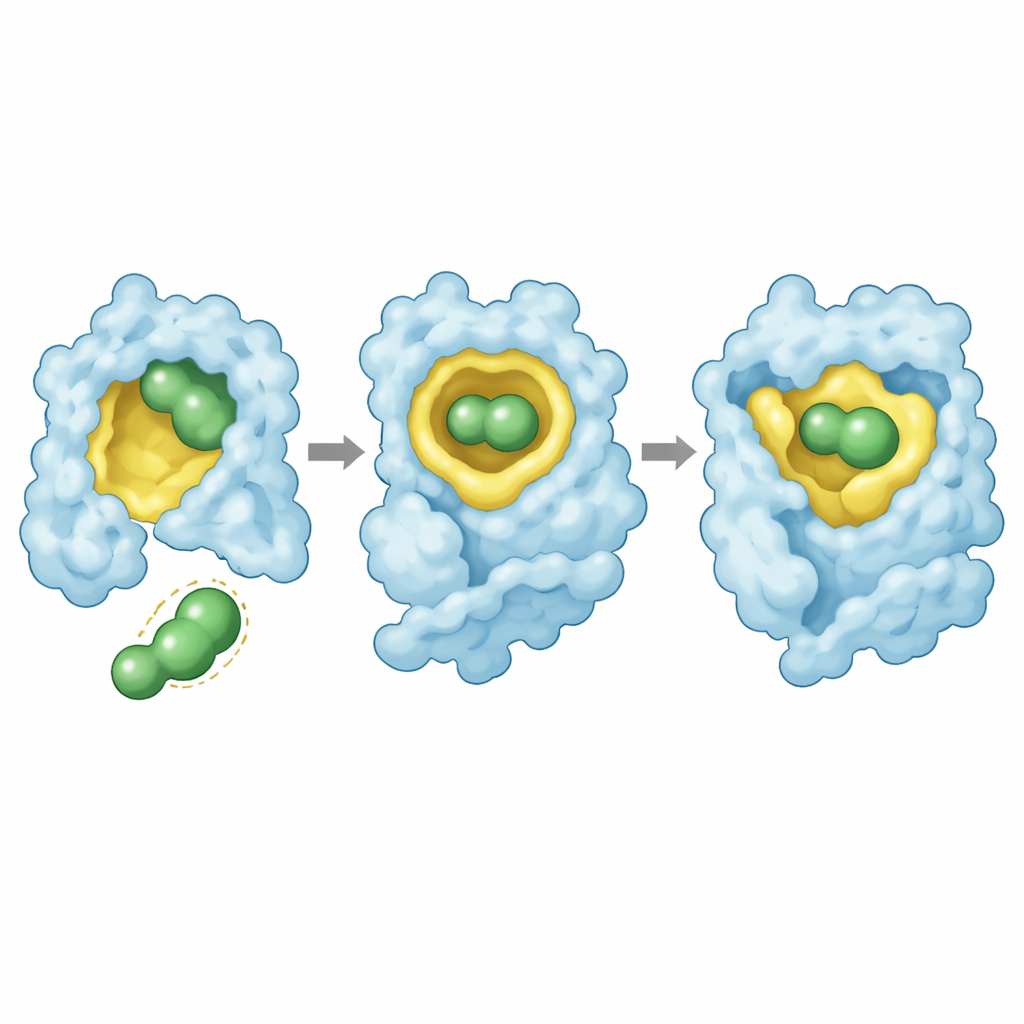
Von der Proteinreparatur zum Zellverhalten
Die entscheidende Prüfung ist, ob eine solche Stabilisierung p53s Schutzfunktion in lebenden Zellen wiederbelebt. Die Forschenden konstruierten Lungenkrebszellen ohne natürliches p53 so, dass sie entweder die Varianten Y220C, Y220S, Y220N oder Y220H exprimieren. Unter Behandlung mit rezatapopt zeigten Zellen mit Y220C eine starke Aktivierung klassischer p53-Zielgene, die an Zellzyklusstopp und dem Auslösen von Zelltod beteiligt sind. Die Y220S-Zellen zeigten ein sehr ähnliches Muster — Wiederherstellung der gefalteten, aktiven Form von p53, starke Genaktivierung, verlangsamte Proliferation und vermehrter Zelltod — jedoch nur bei Wirkstoffkonzentrationen, die mehr als zehnmal höher liegen als für Y220C erforderlich. Y220N-Zellen zeigten im Vergleich dazu bei verträglichen Dosen keine eindeutige Aktivierung von Zielgenen und blieben überwiegend in der fehlgefalteten Form, obwohl leichte spät auftretende Wachstumsveränderungen auf eine nur teilweise funktionelle Rettung hindeuten.
Was das für Patientinnen, Patienten und künftiges Wirkstoffdesign bedeutet
Für Menschen mit Tumoren, die die Y220S-Mutation tragen, sind diese Befunde vorsichtig ermutigend: rezatapopt kann prinzipiell p53s Schutzfunktionen wiederherstellen, jedoch nur bei deutlich höheren Dosen, die sich in der klinischen Praxis schwerlich sicher erreichen lassen. Für Y220N scheint das aktuell getestete Medikament unter realistischen Bedingungen nicht auszureichen, um p53 vollständig zu reparieren. Dennoch liefern die strukturellen Blaupausen in dieser Arbeit Hinweise darauf, warum das derzeitige Design weniger gut funktioniert und wie zukünftige Moleküle angepasst werden könnten, um alle drei mutierten Seitenketten einzufangen, ohne sie in ungünstige Positionen zu zwingen. Anders ausgedrückt: Die Entwicklung eines echten „Pan‑Y220“-p53-Reparaturmittels ist herausfordernd, aber erreichbar und würde die Zahl der potenziell Nutzenden dieser aufstrebenden Strategie, den körpereigenen Tumorsuppressor zu reparieren statt zu ersetzen, moderat vergrößern.
Zitation: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Schlüsselwörter: p53-Reaktivierung, rezatapopt, Y220C-Mutation, präzisionsmedizin bei Krebs, Proteinstabilisierung