Clear Sky Science · de
OTUD4-Deubiquitinierung stabilisiert EGFR und aktiviert den PI3K/AKT-Signalweg, um die Invasivität des triple-negativen Mammakarzinoms zu fördern
Warum diese Forschung für Brustkrebs wichtig ist
Das triple-negative Mammakarzinom ist eine der schwersten behandelbaren Formen von Brustkrebs, weil ihm die üblichen Hormon- und Wachstumsmarker fehlen, auf die viele Medikamente abzielen. Diese Studie deckt ein verborgenes „Schutz“-Molekül auf, das Krebszellen hilft, einen kräftigen Wachstums-Schalter eingeschaltet zu halten. Durch das Verständnis dieses unsichtbaren Unterstützungssystems könnten Wissenschaftler neue Wege finden, die Signale zu unterbinden, die Tumorwachstum und -ausbreitung antreiben.
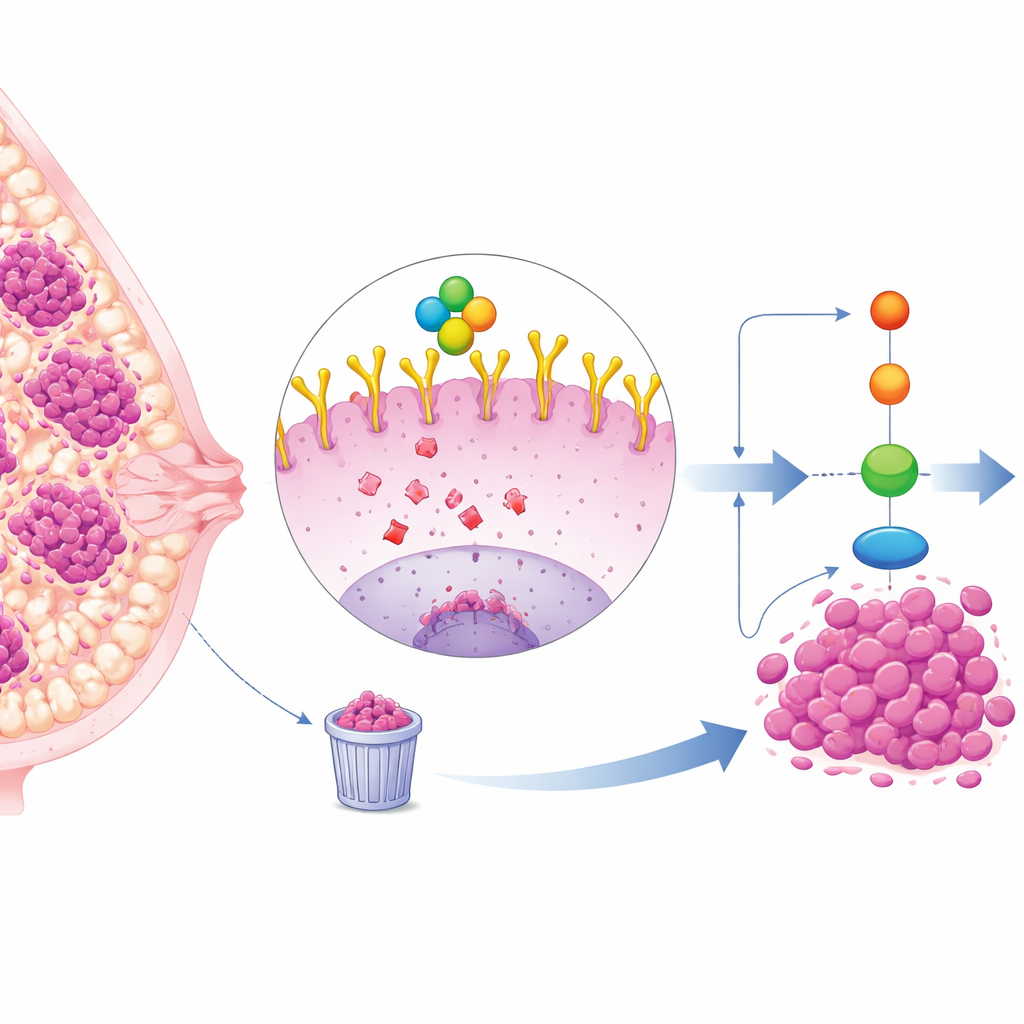
Ein schwer zu behandelnder Brustkrebs-Subtyp
Das triple-negative Mammakarzinom (TNBC) macht etwa ein Viertel der Brustkrebsfälle aus und neigt dazu, schneller zu wachsen und zu metastasieren als andere Subtypen. Da TNBC-Zellen keine Östrogen-, Progesteron- oder HER2-Rezeptoren tragen, sind standardmäßige zielgerichtete Therapien weniger wirksam, sodass Chemotherapie und Operation die Hauptoptionen bleiben. Viele TNBC-Tumoren weisen jedoch hohe Spiegel eines Zelloberflächenproteins namens EGFR auf, das wie eine Antenne wirkt, um Wachstums- und Überlebenssignale zu empfangen. Hohe EGFR-Spiegel sind mit schlechten Prognosen verbunden, doch Therapien, die EGFR direkt blockieren, zeigten in der Klinik enttäuschende Ergebnisse, was darauf hinweist, dass tiefere Regulationsebenen im Spiel sind.
Aufspüren eines verborgenen Helfers des Tumorwachstums
Die Forschenden konzentrierten sich auf OTUD4, ein Enzym, das kleine Proteinanhängsel namens Ubiquitin von anderen Proteinen entfernt. Diese Anhängsel fungieren oft als Abbausignale und markieren Proteine für den Abbau; das Entfernen kann das markierte Protein stabilisieren und schützen. Mithilfe großer Krebsdatenbanken und Gewebeproben von Patientinnen und Patienten zeigten die Forschenden, dass OTUD4 in TNBC-Tumoren und Zelllinien in höheren Mengen vorkommt als im normalen Brustgewebe. Patientinnen und Patienten mit Tumoren, die mehr OTUD4 enthielten, hatten tendenziell eine schlechtere Überlebenswahrscheinlichkeit, was darauf hindeutet, dass OTUD4 wie ein Onkogen wirkt — ein Gen, das die Krebsprogression fördert.
Wie OTUD4 Krebszellen aggressiver macht
Um zu testen, was OTUD4 in TNBC-Zellen tatsächlich bewirkt, reduzierten die Wissenschaftler*innen dessen Menge in zwei weit untersuchten TNBC-Zelllinien. Bei Herunterregulierung von OTUD4 wuchsen die Krebszellen langsamer, bildeten weniger Kolonien und konnten sich in Wundheilungs- und Transwell-Assays schlechter bewegen — alles Hinweise auf verminderte Aggressivität. Bei Überexpression von OTUD4 zeigte sich das Gegenteil: Die Zellen proliferierten schneller und bewegten sich leichter, was die Annahme stützt, dass OTUD4 maligne Eigenschaften antreibt. In Mäusen wuchsen Tumoren aus Zellen ohne OTUD4 langsamer und zeigten reduzierte Marker für Zellteilung und Wachstumssignale, wodurch diese Effekte auch in lebenden Organismen bestätigt wurden.
Ein molekularer Schutzschild für EGFR
Bei der Untersuchung des Mechanismus nutzte das Team Protein-Interaktions-Screens und biochemische Tests, um EGFR als direkten Bindungspartner von OTUD4 zu identifizieren. Sie fanden heraus, dass OTUD4 an eine spezifische Region von EGFR bindet und K48-verkettete Ubiquitin-Ketten entfernt — jene Ubiquitin-Art, die normalerweise Proteine für den Abbau durch das zelluläre Recyclingsystem markiert. Bei Reduktion von OTUD4 wurde EGFR schneller abgebaut, während die Genaktivität von EGFR unverändert blieb, was zeigt, dass OTUD4 nach der Herstellung von EGFR wirkt und nicht auf DNA- oder RNA-Ebene. Das Blockieren des zellulären Proteinasp-Abbaus stellte die EGFR-Spiegel wieder her, was unterstreicht, dass der Schlüsselschritt der Schutz vor dem Abbau ist. Mit stabilerem EGFR an der Zelloberfläche bleibt ein wichtiger innerer Signalweg, der PI3K/AKT/mTOR-Weg, dauerhaft aktiviert und treibt Zellwachstum und Überleben an.
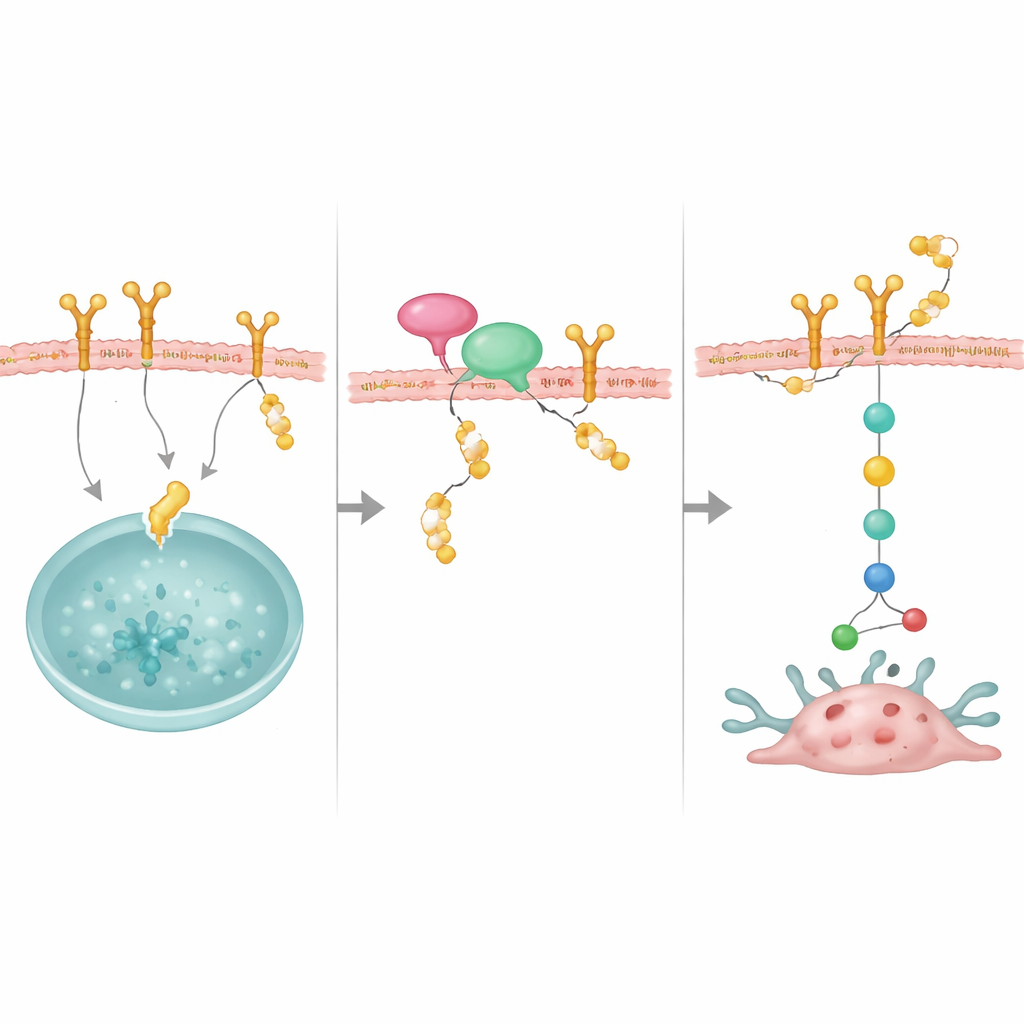
Ein Adapter, der den Beschützer zu seinem Ziel bringt
Die Studie entdeckte außerdem einen wichtigen Partner, NRP1, ein Membranprotein, das zuvor mit aggressiven Brustkrebserkrankungen in Verbindung gebracht wurde. NRP1 bindet sowohl OTUD4 als auch EGFR und hilft, OTUD4 in Position zu bringen, um EGFR vor dem Abbau zu bewahren. Bei Reduktion von NRP1 wurde EGFR weniger stabil und seine Wachstumssignale schwächer, obwohl die OTUD4-Spiegel unverändert blieben. Eine Überexpression von OTUD4 konnte den Verlust von NRP1 teilweise kompensieren, was nahelegt, dass NRP1 wie eine Andockplattform wirkt, die OTUD4 zu EGFR rekrutiert. Zusammen bilden diese Moleküle einen stabilisierenden Komplex, der EGFR an der Zelloberfläche in hoher Menge erhält.
Was das für künftige Behandlungen bedeutet
Indem gezeigt wird, wie OTUD4 und NRP1 zusammenarbeiten, um EGFR vor dem Abbau zu schützen, identifiziert diese Studie einen neuen Kontrollpunkt für ein zentrales Wachstumssignal im triple-negativen Mammakarzinom. Anstatt zu versuchen, die Aktivität von EGFR an seiner aktiven Stelle zu blockieren, könnten künftige Therapien darauf abzielen, die schützende Wirkung von OTUD4 oder seine Rekrutierung durch NRP1 zu stören, wodurch EGFR-Spiegel sinken und der PI3K/AKT-Weg, der das Tumorwachstum antreibt, gedämpft wird. Zwar sind weitere Arbeiten nötig, um sichere und wirksame OTUD4-Inhibitoren zu finden und mögliche Fluchtmechanismen der Krebszellen zu verstehen, doch die Ergebnisse eröffnen vielversprechende Ansätze für präzisere Behandlungen dieses herausfordernden Brustkrebs-Subtyps.
Zitation: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Schlüsselwörter: triple-negatives Mammakarzinom, EGFR-Signalgebung, OTUD4, PI3K AKT-Signalweg, Proteinabbau