Clear Sky Science · de
Humanes Papillomavirus16 E7 erhöht die Stammzell-Eigenschaften von Zellen durch Regulation der APC2/SPIN4/β-Catenin-Achse bei Gebärmutterhalskrebs
Warum diese Forschung wichtig ist
Gebärmutterhalskrebs bleibt weltweit eine wichtige Todesursache bei Frauen, insbesondere dort, wo Vorsorgeuntersuchungen und Impfungen eingeschränkt sind. Forscher wissen, dass bestimmte Typen des humanen Papillomavirus (HPV), vor allem HPV16, Treiber dieser Erkrankung sind; die genauen Mechanismen, mit denen das Virus Tumoren aggressiv und rezidivträchtig hält, werden jedoch weiterhin aufgeklärt. Diese Studie untersucht, wie ein virales Protein namens E7 eine kleine, aber potente Population von "Krebsstamm"-Zellen erhält, die Tumorwachstum, Ausbreitung und Therapieresistenz antreiben können — und damit Hinweise auf neue, präzisere Therapien liefert.
Vom verbreiteten Virus zum gefährlichen Krebs
Die meisten HPV-Infektionen klingen von selbst ab, doch eine persistierende Infektion mit Hochrisiko-Typen kann gesunde Zervixzellen in Krebszellen verwandeln. Das virale E7-Protein spielt dabei eine zentrale Rolle: Es schaltet wichtige Schutzmechanismen aus, die normalerweise die Zellteilung kontrollieren. Frühere Arbeiten dieser Forschungsgruppe zeigten, dass HPV16 E7 stammesähnliche Eigenschaften in Gebärmutterhalskrebszellen verstärkt und sie damit schwerer zu beseitigen macht. In der vorliegenden Studie wollte das Team die von E7 gesteuerten Gen-Netzwerke abbilden, um genau zu verstehen, wie es diese gefährlichen Zellen am Leben und funktionsfähig hält.
E7s Auswirkungen innerhalb der Tumorzellen verfolgen
Um den Einfluss von E7 nachzuverfolgen, verwendeten die Forschenden im Labor gezüchtete Gebärmutterhalskrebszelllinien und reduzierten E7 mit kleinen interferierenden RNAs, einem Werkzeug, das spezifische Gene vorübergehend ausschaltet. Anschließend bestimmten sie, welche Gene im gesamten Genom in ihrer Aktivität verändert waren. Diese Analyse kombinierten sie mit einer Reihe funktioneller Tests: wie schnell die Zellen wuchsen, wie gut sie migrierten und in künstlichen Membranen eindrangen und wie leicht sie im Kulturversuch kugelförmige Verbände bildeten — ein Kennzeichen von Krebsstammzellen. Sie untersuchten außerdem in Mäusen wachsende Tumoren und analysierten große öffentliche Krebsdatensätze, um zu prüfen, wie ihre Befunde mit Mustern in Patientenproben übereinstimmen.
Eine überraschende Rolle eines bekannten Signalwegs
Die Genkartierungs-Experimente wiesen stark auf den Wnt/β-Catenin-Signalweg hin, einen bekannten Regulator normaler Stammzellen und vieler Tumoren. Nach Abschalten von E7 sanken die β-Catenin-Spiegel, was darauf hindeutet, dass dieser Weg abgeschaltet wurde. Gleichzeitig fiel den Forschenden eine starke Veränderung des Gens APC2 auf. In vielen anderen Krebsarten wirken APC-verwandte Proteine als Bremse für die Wnt-Signalisierung und helfen, das Zellwachstum zu kontrollieren. Hier jedoch schienen Gebärmutterhalskrebszellen APC2 auf unerwartete Weise zu nutzen: Wurde APC2 reduziert, wuchsen die Krebszellen langsamer, waren weniger mobil und invasiv und verloren stammesähnliche Merkmale. In Mäusen blieben Tumoren mit langfristiger APC2-Reduktion deutlich kleiner, während die Tiere gesund blieben — ein Hinweis auf ein eventuell sicheres therapeutisches Fenster.
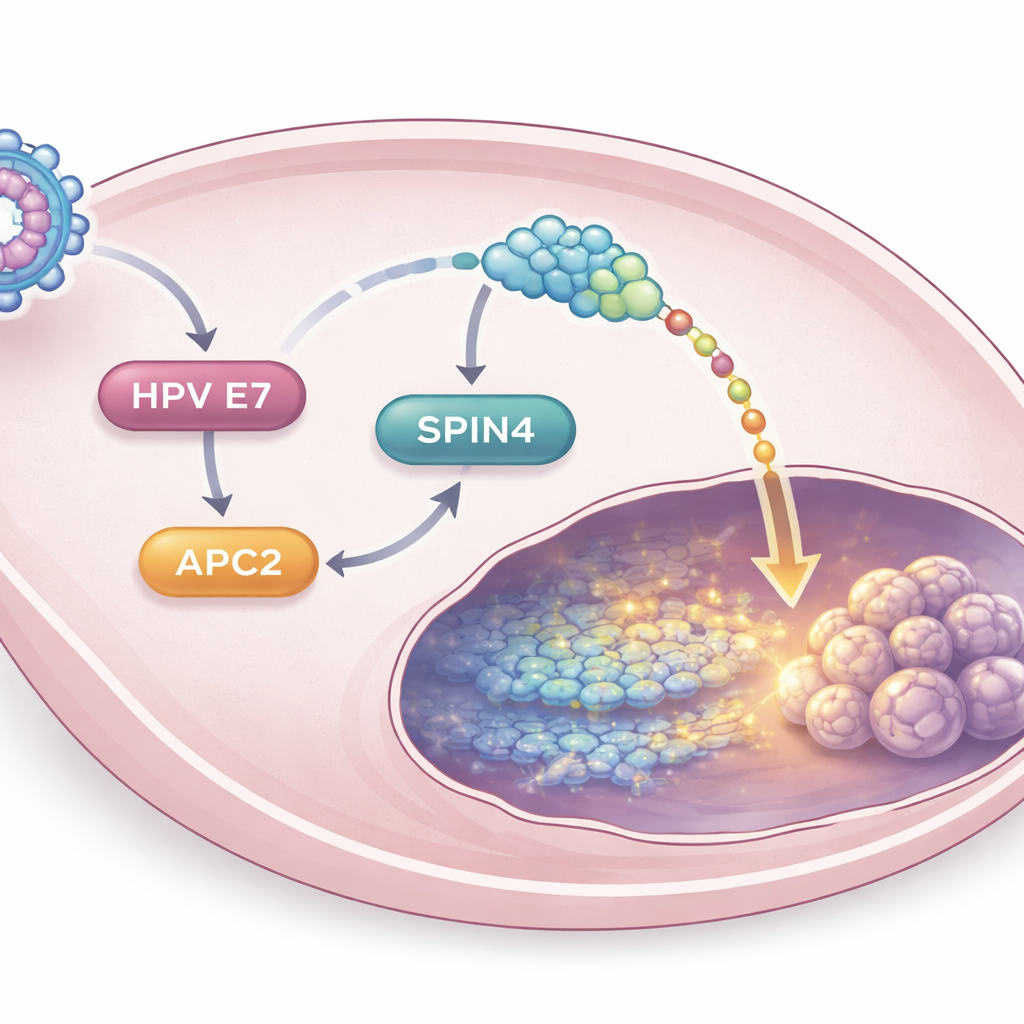
Aufdeckung einer neuen krebserhaltenden Signalkette
Bei tiefergehenden Untersuchungen zeigten die Forschenden, dass HPV16 E7 APC2 indirekt über ein weiteres Protein namens E2F1 erhöht, das die Aktivierung von wachstumsbezogenen Genen fördert. Einmal erhöht, steigert APC2 wiederum die Aktivität eines weniger bekannten Proteins namens SPIN4. Die Analyse menschlicher Tumordaten ergab, dass SPIN4 in Gebärmutterhalskrebserkrankungen stärker ausgeprägt ist als im normalen Gewebe und höhere Werte mit schlechterem Überleben korrelieren. Im Labor schwächte das Abschalten von SPIN4 die Fähigkeit von APC2, Zellwachstum, Invasion, Wnt/β-Catenin-Aktivität und krebsstammzellähnliches Verhalten zu fördern. In Mausversuchen waren Tumoren ohne SPIN4 kleiner und zeigten reduzierte Marker für Stemness. Zusammengenommen skizzieren diese Befunde eine schrittweise Kette — HPV16 E7 zu APC2 zu SPIN4 zu Wnt/β-Catenin — die gemeinsam Gebärmutterhalskrebszellen aggressiv und stammesähnlich erhält.
Blick voraus auf klügere Behandlungen
Für Nicht-Spezialisten lautet die Kernbotschaft: Diese Studie identifiziert eine bislang unerkannte Verschaltung innerhalb HPV-getriebener Gebärmutterhalskrebserkrankungen. Statt als einfacher Ein-/Ausschalter kapert das virale E7-Protein eine spezifische Abfolge von Wirtsproteinen — APC2 und SPIN4 — um einen gefährlichen Pool von Krebsstammzellen über den Wnt/β-Catenin-Weg am Leben zu erhalten. Diese Achse erklärt nicht nur, warum einige Tumoren so hartnäckig sind, sondern zeigt auch mehrere neue Ansätze, auf die Medikamente oder Kombinationstherapien abzielen könnten, insbesondere bei Patientinnen mit therapieresistenten Tumoren. Indem künftige Therapien die virusbedingte Schaltlogik angreifen, die die Tumor-"Samen"-Zellen erhält, könnten Rückfälle seltener werden und die Langzeitergebnisse verbessert werden.
Zitation: Shen, T., Ma, Y., Wu, T. et al. Human papillomavirus16 E7 enhances cell stemness by regulating the APC2/SPIN4/β-catenin axis in cervical cancer. Oncogenesis 15, 10 (2026). https://doi.org/10.1038/s41389-026-00602-8
Schlüsselwörter: Gebärmutterhalskrebs, humanes Papillomavirus, Krebsstammzellen, Wnt-β-Catenin-Signalweg, onkogenes Signalwesen