Clear Sky Science · de
Partielle Verkürzung der C-terminalen Domäne von PTCH1 bei Krebs fördert Tumorentstehung durch nicht-kanonische Aktivierung einer GLI-PI3K-Schleife
Warum eine winzige Proteinveränderung beim Darmkrebs wichtig ist
Darmkrebs entsteht meist durch eine langsame Anhäufung genetischer Fehler. Diese Studie fokussiert auf eine überraschend kleine Veränderung eines zelloberflächenständigen Proteins namens PTCH1 und zeigt, wie das Abschneiden eines Teils seines Schwanzes Darmkrebszellen schneller wachsen, leichter streuen und möglicherweise gegen einige bestehende Medikamente resistenter werden lässt. Das Verständnis dieses verborgenen Wachstums‑Schalters könnte Wege zu neuen, präziseren Therapien für eine Untergruppe von Patientinnen und Patienten eröffnen.
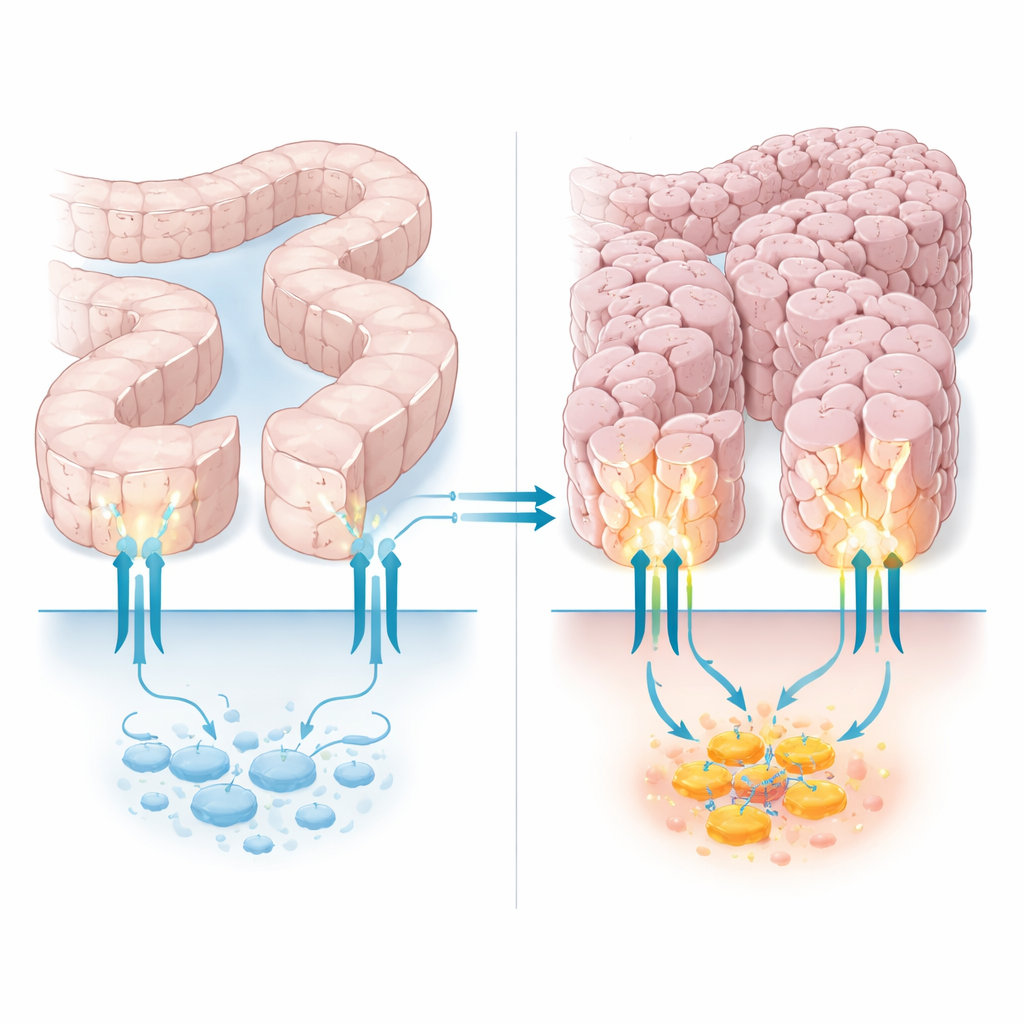
Ein Wächter der Zelle mit verstecktem Nebenjob
PTCH1 ist vor allem als Wächter des Hedgehog‑Signalwegs bekannt, einer Kommunikationsstrecke, die Zellen während der Entwicklung und der Gewebereparatur nutzen. In seiner klassischen Rolle hält PTCH1 ein Partnerprotein, Smoothened, in Schach und reguliert damit eine Familie von DNA‑Kontrollfaktoren namens GLI. PTCH1 besitzt jedoch auch einen langen, flexiblen Schwanz, der in die Zelle hineinragt und als Andockstreifen für andere Proteine dient, die den Zelltod, den Recycling‑Apparat der Zelle und weitere Prozesse beeinflussen. Frühere Arbeiten zeigten, dass einige Darm‑, Magen‑ und Gebärmuttertumoren Mutationen tragen, die einen Teil dieses inneren Schwanzes abschneiden. Diese Mutationen schienen den klassischen Hedgehog‑Schalter nicht zu zerstören, machten die Krebszellen aber besser darin, Stress zu überstehen, was darauf hindeutet, dass dieses Schwanzsegment still zur tumorrepressiven Funktion von PTCH1 beiträgt.
Krebszellen gezielt verändern, um die Wirkung zu prüfen
Um zu untersuchen, was diese Schwanz‑verkürzenden Mutationen tatsächlich bewirken, stellten die Forschenden sie mittels CRISPR/Cas9-Geneditierung in einer Darmkrebszelllinie nach. Sie verglichen zwei editierte Klone, von denen jeder eine andere Trunkierung im PTCH1‑Schwanz trug, mit ansonsten identischen Zellen mit normalem PTCH1. Die Mutanten teilten sich schneller, bildeten deutlich mehr Kolonien und gedeihen sogar, wenn sie ohne Anhaftung wachsen mussten – ein Verhalten, das mit der Fähigkeit zur Metastasierung verbunden ist. Nach Implantation in Mäuse bildeten die Schwanz‑mutierten Zellen innerhalb weniger Wochen deutlich größere Tumoren mit mehr in der Teilung befindlichen Zellen. Wichtig ist, dass die editierten Zellen weiterhin PTCH1 produzierten und seine Hauptwächterfunktion behielten, was zeigt, dass die verstärkte Aggressivität aus dem Verlust der spezialisierten inneren Aufgaben des Schwanzes stammt und nicht aus einem vollständigen Wegfall von PTCH1.
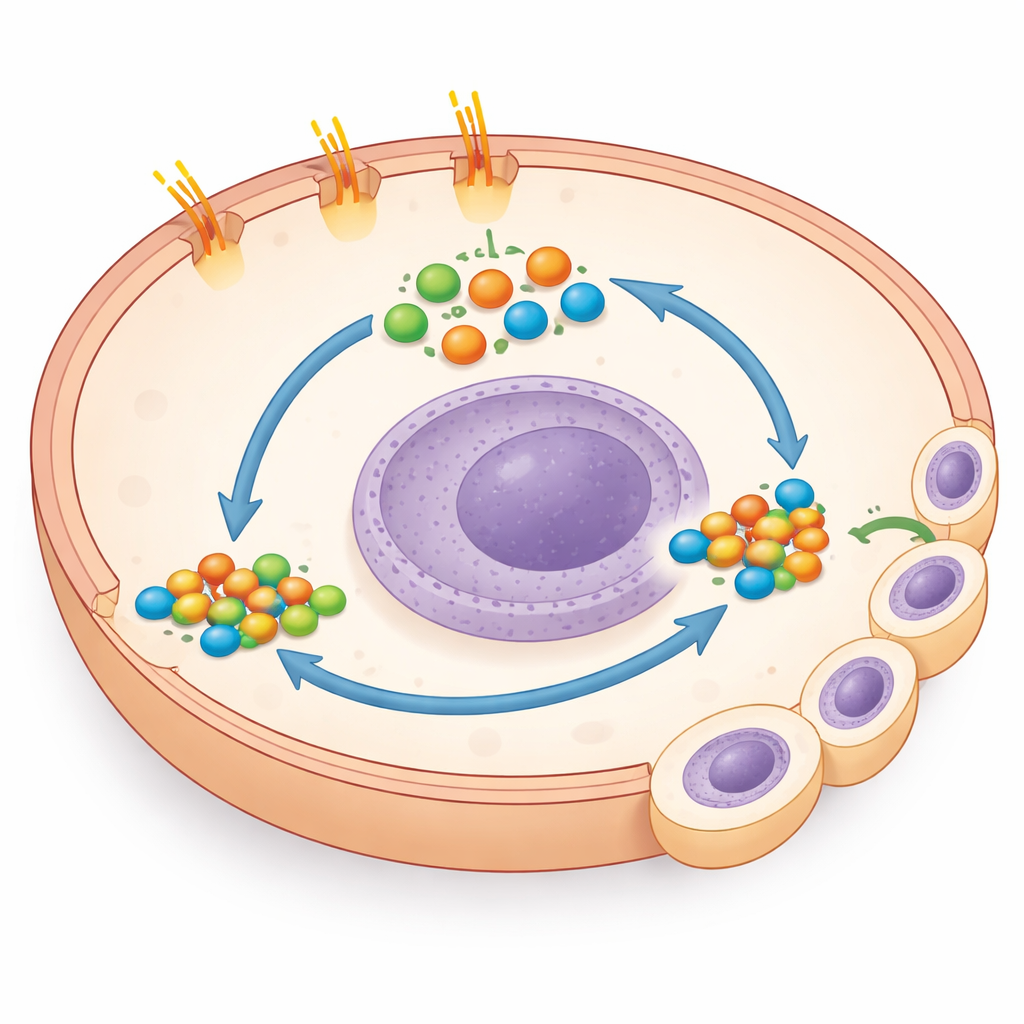
Eine überraschende Abkürzung zu einem starken Wachstumsschalter
Bei der Untersuchung der zugrundeliegenden Biologie machten die Forschenden eine unerwartete Entdeckung: Die schwanztrunkierten Zellen wiesen stark erhöhte Mengen von GLI1 und GLI2 auf, zentrale Treiber von Genprogrammen für Wachstum und Überleben. Normalerweise steigt die GLI‑Aktivität, wenn Smoothened aktiviert wird, doch das Blockieren von Smoothened hatte hier keinen Effekt. Stattdessen reduzierte das direkte Blockieren von GLI mit einem kleinen Wirkstoff oder das gezielte Senken von GLI1 mittels genetischer Werkzeuge das Wachstum der Mutanten in Zellkulturen deutlich — ebenso in zusätzlichen Darmkrebszelllinien, die natürlicherweise PTCH1‑Schwanzmutationen tragen. Das zeigte, dass der Verlust des Schwanzes GLI über einen „nicht‑kanonischen“ Weg aktiviert, der den üblichen Hedgehog‑Schalter umgeht, und dass die Krebszellen für ihr aggressives Verhalten stark von dieser Abkürzung abhängig werden.
Mehrere Wachstumswege werden aktiviert, doch eine Schleife dominiert
Durch RNA‑Sequenzierung fanden die Forschenden tausende Gene mit veränderter Aktivität nach der PTCH1‑Schwanztrunkierung. Viele gehören zu bekannten Krebsnetzwerken, einschließlich solcher, die vom epidermalen Wachstumsfaktor‑Rezeptor (EGFR), Ras und Signalwegen gesteuert werden, die Zellstoffwechsel und stamzellähnliche Eigenschaften regulieren. Die Mutanten zeigten erhöhte Aktivität von EGFR und dessen Liganden sowie gesteigerte Aktivität zweier großer downstream‑Wege: der MAPK‑ und der PI3K/Akt‑Pfade. Wenn allerdings EGFR oder dessen MAPK‑Ast blockiert wurden, verlangsamten sich die Mutanten nur teilweise. Dagegen setzten geringe Dosen von PI3K‑Inhibitoren ihr Wachstum und die Koloniebildung stark herab und reduzierten GLI1‑Spiegel — ein Hinweis darauf, dass PI3K/Akt ein kritischer Partner in diesem neuen GLI‑aktivierenden Mechanismus ist.
Eine sich selbst verstärkende Schleife, die Tumorwachstum antreibt
Weitere Experimente offenbarten einen Rückkopplungszyklus: Die Trunkierung des PTCH1‑Schwanzes erhöht GLI‑Aktivität; GLI wiederum trägt dazu bei, PI3K/Akt‑Signale hoch zu halten; und PI3K/Akt stabilisiert und aktiviert GLI. Das Unterbrechen von GLI oder PI3K brach diese Schleife und nahm den Mutanten ihren Wachstumsvorteil, während das einfache Hochfahren von PI3K/Akt eine direkte GLI‑Blockade nicht überwinden konnte. Die Zellen zeigten ferner eine gedämpfte Aktivität von PKA, einem Enzym, das GLI‑Proteine normalerweise zur Inaktivierung markiert — was die Balance zusätzlich zugunsten GLI‑gesteuerter Programme verschiebt.
Was das für künftige Behandlungen bedeuten könnte
Für Patientinnen und Patienten ist die zentrale Botschaft, dass einige Darmkrebse PTCH1‑Schwanzmutationen tragen, die still eine GLI–PI3K‑positive Rückkopplungsschleife verdrahten und Tumoren beim Wachsen helfen sowie der Wirksamkeit von Therapien entziehen können, die auf den bekannteren Hedgehog‑Schalter oder den EGFR–MAPK‑Weg abzielen. Solche Tumoren könnten stattdessen besonders empfindlich auf Behandlungen reagieren, die GLI direkt blockieren oder PI3K/Akt angreifen. Die Studie legt nahe, dass die Sequenzierung von PTCH1 in Darmtumoren — insbesondere von rechtsseitigen Tumoren, in denen solche Mutationen häufiger vorkommen — helfen könnte, Patientinnen und Patienten zu identifizieren, die von PI3K‑ oder GLI‑gerichteten Strategien profitieren, und macht aus einer subtilen Proteinkürzung einen potenziell nützlichen therapeutischen Hinweis.
Zitation: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Schlüsselwörter: Darmkrebs, Hedgehog-Signalgebung, PTCH1-Mutationen, GLI-Transkriptionsfaktoren, PI3K-Akt-Signalweg